Фармацевтическая продукция это: Товары медицинского назначения и фармацевтическая продукция
Товары медицинского назначения и фармацевтическая продукция
В чем заключается эта политика?Твиттер запрещает рекламу товаров медицинского назначения и фармацевтической продукции. Эти ограничения зависят как от конкретного продвигаемого продукта или услуги, так и от страны, для которой предназначена рекламная кампания. Чтобы определить, какая политика распространяется на ваш продукт или услугу и страну или страны, которые вы хотите охватить, см. информацию по конкретным странам ниже. За исключением нижеуказанного, реклама товаров медицинского назначения и фармацевтической продукции запрещена.
Примечание. В определенных случаях, которые указаны ниже, владельцам учетных записей разрешено рекламировать такую продукцию, только если у них есть соответствующее разрешение от Твиттера. Для получения разрешения необходимо обратиться к группе, отвечающей за учетные записи Твиттера. Для каждого случая приведены контактные данные Твиттера.
Какие товары и услуги подпадают под действие этой политики?Ниже перечислены некоторые из товаров и услуг, на которые распространяется действие этой политики.
- Аптеки
- Интернет-аптеки
- Традиционные аптеки
- Аптеки, изготавливающие лекарственные средства (отпускающие препараты по рецепту)
- Ветеринарные аптеки
- Товары медицинского назначения и фармацевтическая продукция
- Препараты строгого учета, рецептурные и безрецептурные препараты
- Производители фармацевтической продукции
- Информационные сайты и блоги, в центре внимания которых рецептурные препараты
- Изделия медицинского назначения, подпадающие под регулирование
- Дисконтные карты на приобретение рецептурных препаратов
- Клинические испытания
- Срочные контрацептивы, например противозачаточные лекарственные препараты и посткоитальные противозачаточные препараты
- Продукты, описание которых подразумевает или утверждает, что они предназначены для диагностики, лечения, облегчения симптомов или предотвращения заболеваний, медицинских проблем и зависимости, а также существенно влияют на настроение, скорость или степень восстановления, потери веса или роста мышц
- Оздоровительные добавки и вещества (также известные как добавки для поддержания здоровья, биологически активные, диетические и питательные добавки)
- Добавки, которые содержат анаболические стероиды или в рекламе которых упоминаются стероиды или стероидоподобные вещества
- Добавки, которые явно похожи на лекарственные средства, отпускаемые по рецепту (например, по внешнему виду или названию), вызывают сомнения в безопасности или соответствии требованиям одобренного медицинского препарата или продвигают чрезмерное или небезопасное употребление
- Медицинские и косметические услуги
- Операции искусственного прерывания беременности
- Реклама, связанная с правом на аборт
- Инъекции ботокса
- Товары и услуги для внутриутробного выбора пола ребенка
- Телемедицина
Эта политика в целом не применяется к следующим товарам и услугам.
Чтобы определить, какая политика распространяется на ваш продукт или услугу и страну или страны, которые вы хотите охватить, см. информацию по конкретным странам ниже. За исключением нижеуказанного, реклама товаров медицинского назначения и фармацевтической продукции запрещена.
Реклама безрецептурных препаратов
Реклама лицензированных безрецептурных лекарственных средств разрешена только для целевой аудитории в следующих странах:
- Африка и Ближний Восток: Алжир, Бахрейн, Египет, Ирак, Иордания, Йемен, Катар, Кувейт, Ливан, Ливия, Марокко, ОАЭ, Оман, Палестинские территории, Саудовская Аравия, Тунис.
- Азиатско-Тихоокеанский регион:
- Европа: Австрия, Бельгия, Болгария, Германия, Дания, Ирландия, Испания, Италия, Македония, Нидерланды, Норвегия, Польша, Португалия, Румыния, Сербия, Словения, Соединенное Королевство и территории под его юрисдикцией, Украина, Финляндия, Франция, Хорватия, Чехия, Швеция.

- Латинская Америка: Аргентина, Бразилия, Гватемала, Доминиканская Республика, Колумбия, Мексика, Панама, Уругвай, Чили.
- Северная Америка: Канада, США.
Ниже перечислены дополнительные требования к рекламе товаров медицинского назначения и фармацевтической продукции, охватывающей целевую аудиторию в соответствующих странах.
Алжир
- Реклама безрецептурных контрацептивов и лубрикантов запрещена.
Австралия
- Разрешается рекламировать только те безрецептурные препараты, реклама которых утверждена согласно Реестру лечебных товаров Австралии (ARTG).
- Реклама рецептурных препаратов запрещена.
- Разрешается рекламировать интернет-аптеки, зарегистрированные в фармацевтической гильдии Австралии или системе государственного медицинского страхования Австралии. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Австралии и только при наличии предварительного разрешения Твиттера.

Бахрейн
- Реклама безрецептурных контрацептивов запрещена.
Канада
Хорватия
- Запрещено рекламировать гомеопатические препараты.
Дания
- Реклама безрецептурных препаратов и лекарственных средств из растительного сырья разрешается при условии, что рекламируемый продукт утвержден Агентством здравоохранения Дании.
- Реклама препаратов, приготавливаемых в аптеке по рецепту врача, запрещена.
Египет
- Реклама безрецептурных контрацептивов запрещена.
Финляндия
- Разрешена реклама безрецептурных препаратов для людей и животных. Рекламируемые медицинские препараты должны быть утверждены государственной службой по лекарственным средствам Финляндии.
- Реклама биологически активных добавок разрешена при условии, что такие добавки обладают свойствами, предупреждающими возникновение заболевания, или исцеляющими свойствами.

Франция
- Реклама от производителей фармацевтической продукции разрешена с ограничениями. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории во Франции.
Германия
- Реклама от производителей фармацевтической продукции разрешена с ограничениями. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Германии.
- Реклама изделий медицинского назначения разрешена.
Гонконг
Индия
Индонезия
- Реклама товаров медицинского назначения и косметической продукции разрешена с ограничениями.
Ирак
- Реклама безрецептурных контрацептивов запрещена.
Ирландия
- Реклама от производителей фармацевтической продукции разрешена с ограничениями. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Ирландии.
Италия
- Реклама от производителей фармацевтической продукции разрешена с ограничениями.
 Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Италии.
Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Италии.
Япония
- Разрешена онлайн-продажа утвержденных правительством безрецептурных препаратов.
- Реклама товаров медицинского назначения и пищевых добавок разрешена, но с ограничениями.
- Производители фармацевтической продукции могут рекламировать информационные сайты и размещать социальную рекламу, но с ограничениями.
- Реклама утвержденных правительством медицинских приборов для домашнего использования разрешена с определенными ограничениями и при условии получения предварительного разрешения от Твиттера.
Иордания
- Реклама безрецептурных контрацептивов запрещена.
Кувейт
- Реклама товаров медицинского назначения и косметической продукции разрешена с ограничениями.
- Реклама безрецептурных контрацептивов запрещена.
Ливан
- Реклама безрецептурных контрацептивов запрещена.

Ливия
- Реклама безрецептурных контрацептивов запрещена.
Македония
Малайзия
- Реклама безрецептурных лекарственных средств разрешена, но содержание рекламы подлежит утверждению советом по рекламе медицинских препаратов.
- Содержание рекламы, размещаемой медицинскими работниками, ограничивается только указанием имени и специализации медицинского работника и места, где будут оказаны услуги. Рекомендации товара запрещены.
- Реклама частных лечебных учреждений может содержать только общую информацию (название, местоположение, контактные данные, часы работы, тип учреждения и цены). Рекомендации товара запрещены.
- Запрещено рекламировать средства для снижения веса, предназначенные как для приема внутрь, так и для наружного применения.
Мексика
- Запрещено рекламировать пищевые добавки (включая добавки для бодибилдинга и снижения веса).
Марокко
- Во всех применимых случаях рекламное объявление должно содержать номер разрешения, выданного министерством здравоохранения.

- Реклама безрецептурных контрацептивов запрещена.
Нидерланды
- Разрешена реклама безрецептурных медицинских устройств и медицинских устройств для диагностики в лабораторных условиях.
- Разрешена реклама и продажа безрецептурных препаратов с таргетингом на Нидерланды. Также разрешена онлайн-продажа в аптеках.
- Реклама от производителей фармацевтической продукции разрешена с ограничениями. Такие рекламодатели обязаны ограничить таргетинг территорией Нидерландов.
Новая Зеландия
- Реклама продукции, содержащая заявления о ее лечебных свойствах, разрешена с учетом ограничений.
Норвегия
- В рекламе безрецептурных лекарственных средств не должны упоминаться такие серьезные заболевания, как диабет, заболевания, передаваемые половым путем, и туберкулез.
Оман
- Реклама безрецептурных контрацептивов запрещена.
Палестинские территории
- Реклама безрецептурных контрацептивов запрещена.

Польша
Филиппины
- Реклама безрецептурных препаратов разрешена, но с ограничениями.
- Реклама товаров медицинского назначения и косметической продукции разрешена с ограничениями.
- Только лицензированные медицинские работники имеют право рекламировать медицинские услуги. Содержание рекламы, размещаемой медицинскими работниками, ограничивается указанием имени, адреса, часов приема и упомянутой в лицензии области специализации медицинского работника.
Португалия
- Реклама продукции, содержащая заявления о лечебных свойствах такой продукции, разрешена, но с учетом ограничений.
Катар
- Реклама безрецептурных контрацептивов запрещена.
Россия
- Реклама с таргетингом на Россию должна быть на русском языке.
- Разрешается продажа безрецептурных препаратов, утвержденных государственным реестром лекарственных средств.
- Реклама безрецептурных препаратов должна включать обязательный отказ от ответственности на русском языке: «Есть противопоказания.
 Посоветуйтесь с врачом».
Посоветуйтесь с врачом». - Запрещено рекламировать потребительский товар как эффективное лечебное средство или продукт, обладающий лечебными свойствами.
- Запрещено рекламировать медицинские услуги, в том числе размещать рекламные объявления, которые содержат название медицинских услуг, медицинского оборудования или слова, указывающие на медицинскую деятельность.
- Реклама от производителей фармацевтической продукции разрешена (за исключением лекарств рецептурного отпуска).
Саудовская Аравия
- Реклама безрецептурных препаратов разрешена с ограничениями. Рекламные объявления подлежат утверждению в управлении по контролю качества медикаментов и продуктов питания Саудовской Аравии (SFDA) и должны включать номер решения о таком утверждении.
- Реклама косметической продукции разрешена с ограничениями.
- Реклама безрецептурных контрацептивов запрещена.
Сингапур
- Реклама косметической продукции разрешена с ограничениями.

- Только лицензированные больницы, медицинские клиники, лаборатории и учреждения здравоохранения, включенные в список лицензированных учреждений здравоохранения, имеют право рекламировать медицинские услуги.
Словения
- Реклама и продажа безрецептурных препаратов и пищевых добавок разрешена, если рекламодатель получил лицензию от Агентства по лекарственным средствам и медицинским изделиям Республики Словения.
- Реклама должна быть на словенском языке и включать следующее заявление:
- «Всегда внимательно читайте инструкции. «Проконсультируйтесь с врачом или фармацевтом По поводу рисков и побочных действий препарата обращайтесь к врачу или фармацевту».) Это предупреждение должно занимать как минимум 10 % всей рекламной площади.
- Реклама не должна содержать заявлений или рекомендаций ученых, специалистов в области медицины и ветеринарии, а также публично известных персон.
Южная Корея
- Запрещена реклама медицинских и стоматологических услуг.

- Реклама санитарных средств и косметической продукции разрешена с ограничениями.
Испания
- Запрещена реклама продукции для лечения следующих заболеваний человека и животных:
- туберкулез;
- серьезные заболевания, передающиеся половым путем, и инфекционные заболевания;
- рак и другие опухолевые заболевания;
- хроническая бессонница;
- диабет и другие заболевания, связанные с обменом веществ.
- Реклама продукции, содержащая заявления о лечебных свойствах такой продукции, разрешена, но с учетом ограничений.
- Реклама от производителей фармацевтической продукции разрешена с ограничениями. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Испании.
Швеция
- Запрещены утверждения, связанные со здоровьем, включая заявления о пользе пищевых продуктов для здоровья, физического состояния и общего самочувствия.
- Реклама косметической продукции разрешена при условии соблюдения законов и нормативных требований.

Швейцария
- Реклама безрецептурных препаратов, лекарств из растительного сырья и средств альтернативной медицины для целевой аудитории Швейцарии разрешена.
Тунис
- Реклама безрецептурных контрацептивов запрещена.
Турция
- Реклама от производителей фармацевтической продукции разрешена с ограничениями. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Турции.
Украина
- Разрешена реклама безрецептурных препаратов. Однако существует ряд исключений. Список исключений для безрецептурных препаратов см. здесь.
ОАЭ
- Реклама товаров медицинского назначения и косметической продукции разрешена с ограничениями. Рекламировать указанные препараты и услуги имеют право только рекламодатели, лицензированные министерством здравоохранения.
- Реклама безрецептурных контрацептивов запрещена.
Соединенное Королевство и территории под его юрисдикцией
- Разрешена реклама безрецептурных медицинских устройств и медицинских устройств для диагностики в лабораторных условиях.

- Реклама от производителей фармацевтической продукции разрешена с ограничениями. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Соединенном Королевстве.
США
- Реклама традиционных аптек разрешается при условии, что они не рекламируют онлайн-продажи или второе и последующие получения лекарств по одному рецепту. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в США и только при наличии предварительного разрешения Твиттера.
- Реклама онлайн-аптек, аккредитованных советами национальной фармацевтической ассоциации, разрешается, но с ограничениями. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в США и только при наличии предварительного разрешения Твиттера.
- Реклама от производителей фармацевтической продукции разрешена с ограничениями. Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в США и только при наличии предварительного разрешения Твиттера.

- Реклама рецептурных изделий медицинского назначения разрешена.
- Продажа изделий медицинского назначения, которые требуют одобрения Медицинских комиссий по контролю за лекарствами и питательными веществами, осуществляется только при наличии предварительного разрешения Твиттера.
- Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в США.
- Реклама телемедицины с предоставлением услуг в формате «пациент — поставщик услуг» лицензированными поставщиками медицинских услуг разрешена. Такие рекламодатели могут осуществлять таргетинг только на те штаты США, на которые распространяется действие их лицензии, дающей право предоставлять такие услуги и рекламировать их. Такие рекламодатели могут размещать рекламу только при наличии предварительного разрешения Твиттера.
- Свяжитесь с Твиттером, если вы заинтересованы в рекламе такого рода.
Йемен
- Реклама безрецептурных контрацептивов запрещена.

Ознакомьтесь с нашими рекомендациями и убедитесь, что вам понятны требования к вашей торговой марке и компании. Вы несете ответственность за весь контент, который продвигаете в Твиттере. Это, в частности, подразумевает соблюдение применимого законодательства и нормативно-правовых актов в отношении рекламы.
Примечание. Рекламодатели данной вертикали, применяющие таргетинг по возрасту, не должны использовать размещение на платформе Twitter Audience Platform (TAP). В результате запуска компанией Apple функции обеспечения прозрачности при отслеживании действий приложениями Твиттер больше не применяет таргетинг по возрасту и полу на платформе TAP для устройств под управлением iOS, которые не разрешили отслеживание при появлении соответствующего запроса.
Какие еще ресурсы Твиттера относятся к этой политике?Руководство по COVID-19 для рекламодателей [Политика в отношении неприемлемого контента]
Наркотики и принадлежности для их употребления
Контент, запрещенный для несовершеннолетних
Таргетинг на основе категорий деликатного характера
Страница не найдена — Портал Продуктов Группы РСС
Сообщите нам свой адрес электронной почты, чтобы подписаться на рассылку новостного бюллетеня. Предоставление адреса электронной почты является добровольным, но, если Вы этого не сделаете, мы не сможем отправить Вам информационный бюллетень. Администратором Ваших персональных данных является Акционерное Общество PCC Rokita, находящееся в Бжег-Дольном (ул. Сенкевича 4, 56-120 Бжег-Дольный, Польша ). Вы можете связаться с нашим инспектором по защите личных данных по электронной почте: .
Предоставление адреса электронной почты является добровольным, но, если Вы этого не сделаете, мы не сможем отправить Вам информационный бюллетень. Администратором Ваших персональных данных является Акционерное Общество PCC Rokita, находящееся в Бжег-Дольном (ул. Сенкевича 4, 56-120 Бжег-Дольный, Польша ). Вы можете связаться с нашим инспектором по защите личных данных по электронной почте: .
Мы обрабатываем Ваши данные для того, чтобы отправить Вам информационный бюллетень — основанием для обработки является реализация нашей законодательно обоснованной заинтересованности или законодательно обоснованная заинтересованность третьей стороны – непосредственный маркетинг наших продуктов / продуктов группы PCC .
Как правило, Ваши данные мы будем обрабатывать до окончания нашего с Вами общения или же до момента, пока Вы не выразите свои возражения, либо если правовые нормы будут обязывать нас продолжать обработку этих данных, либо мы будем сохранять их дольше в случае потенциальных претензий, до истечения срока их хранения, регулируемого законом, в частности Гражданским кодексом.
В любое время Вы имеете право:
- выразить возражение против обработки Ваших данных;
- иметь доступ к Вашим данным и востребовать их копии;
- запросить исправление, ограничение обработки или удаление Ваших данных;
- передать Ваши персональные данные, например другому администратору, за исключением тех случаев, если их обработка регулируется законом и находится в интересах администратора;
- подать жалобу Президенту Управления по защите личных данных.
Получателями Ваших данных могут быть компании, которые поддерживают нас в общении с Вами и помогают нам в ведении веб-сайта, внешние консалтинговые компании (такие как юридические, маркетинговые и бухгалтерские) или внешние специалисты в области IT, включая компанию Группы PCC .
Больше о том, как мы обрабатываем Ваши данные Вы можете узнать из нашего Полиса конфиденциальности.
Лекарственные средства. Фармацевтические субстанции. АФС
В соответствии с Федеральным Законом N 61-ФЗ «Об обращении лекарственных средств», а так же в соответствии с ГОСТ Р 52249-2009. «Правила производства и контроля качества лекарственных средств»:
«Правила производства и контроля качества лекарственных средств»:
Фармацевтические субстанции (они же «Активные фармацевтические субстанции» или сокращенно «АФС») — лекарственные средства в виде действующих веществ биологического, биотехнологического, минерального или химического происхождения, обладающие фармакологической активностью, предназначенные для производства, изготовления лекарственных препаратов и определяющие их эффективность. [В соответствии с Федеральным Законом N 61-ФЗ «Об обращении лекарственных средств»]
Активные фармацевтические субстанции; АФС (active pharmaceutical ingredient; API): Любое вещество или смесь веществ, предназначенные для производства лекарственных средств, которые в процессе производства лекарственного средства становятся активным ингредиентом этого лекарственного средства. Такие вещества предназначены для проявления фармакологической активности или другого прямого эффекта при диагностике, лечении, облегчении симптомов или профилактике болезни или для воздействия на структуру или функцию организма. [В соответствии с ГОСТ Р 52249-2009. «Правила производства и контроля качества лекарственных средств»]
[В соответствии с ГОСТ Р 52249-2009. «Правила производства и контроля качества лекарственных средств»]
Термины «Активная фармацевтическая субстанция» (рус.: «АФС», анг.: «Active Pharmaceutical Ingredient» или «API»), «Активная субстанция», «Лекарственная субстанция» (drug substance) — являются синонимами.
Наши покупатели это не потребители лекарств, а предприятия, выпускающие конечную продукцию — готовые лекарственные средства (ГЛС). Конечно, фармацевтические субстанции, являющиеся сырьём для фармацевтической промышленности выпускают не только в России. Один из крупнейших поставщиков лекарственных субстанций – Китай. Стоимость фармацевтических субстанций китайского происхождения порою дешевле, но качество оставляет желать лучшего. Нашими потребителями являются как крупные Российские фармацевтические компании, так и некоторые зарубежные фармацевтические компании. Круг наших заказчиков достаточно широк. Для них очень важен имидж своего товарного знака, поэтому они используют качественное сырье, закупаемое у нашего предприятия. Мы уверены, что лекарства Российского производства не только качественные, могут конкурировать с импортными, но и лучшие!
Мы уверены, что лекарства Российского производства не только качественные, могут конкурировать с импортными, но и лучшие!
Группа 30 Фармацевтическая продукция — Справочник химика 21
Фармацевтическая продукция, упомянутая в примечании 4 к данной группе [c.262] Например, химические реактивы и высокочистые вещества ввиду их огромной номенклатуры выделены в самостоятельный класс 26, а химико-фармацевтическая продукция входит в класс 93, охватывающий всю медицинскую продукцию. Остальные продукты тонкого органического синтеза (синтетические красители, органические полупродукты, текстильно-вспомогательные вещества, химические добавки и т п.) вошли в класс 24 вместе с продуктами основного органического синтеза и нефте-, лесо-, коксохимии, а группа полупроводниковых материалов, редких и рассеянных элементов и их соединений высокой и специальной чистоты — в обширный класс 47 цветных металлов и их сплавов, другие продукты тонкого неорганического синтеза (катализаторы, сорбенты и т. п.) — в класс 21 продукции неорганической химии, горно-химического сырья и удобрений, малотоннажные специальные полимерные материалы — в обширный класс 22, охватывающий массовые многотоннажные продукты полимерной химии [68]. [c.51]
п.) — в класс 21 продукции неорганической химии, горно-химического сырья и удобрений, малотоннажные специальные полимерные материалы — в обширный класс 22, охватывающий массовые многотоннажные продукты полимерной химии [68]. [c.51]
ГРУППА 30 ФАРМАЦЕВТИЧЕСКАЯ ПРОДУКЦИЯ [c.249]
Основным направлением международного разделения труда в химической промышленности является специализация стран на производстве готовой химической продукции определенных групп, видов и марок. Номенклатура таких продуктов чрезвычайно широка— это пластические массы, синтетические смолы, химические волокна, синтетический каучук, фармацевтические товары. [c.139]
Витамины занимают одно из ведущих мест в продукции химико-фармацевтической промышленности нашей страны, по темпам роста производства эта группа уступает лишь антибиотикам , [c.5]
Наряду с общим увеличением производства лекарственных средств происходило изменение соотношения отдельных групп этих средств в общей выработке продукции заводов химико-фармацевтической промышленности (табл. 25). [c.168]
25). [c.168]
Анилинокрасочная промышленность представляет собой разветвленный и сложный комплекс производств тонкого органического синтеза. Основные группы продукции анилинокрасочной промышленности — органические полупродукты, синтетические органические красители и пигменты, текстильно-вспомогательные вещества, химические добавки для полимеров, химикаты для производства и обработки кинофотоматериалов. Наряду с этими профильными для отрасли продуктами на анилинокрасочных заводах вырабатывают органические химические реактивы, химико-фармацевтические препараты, товары бытовой химии. Структура производства товарной продукции анилинокрасочной промышленности приведена ниже (в %) [c.64]
В то же время нередко высказывается протквоположное мнение о том, что отдельные отрасли малой химии следует рассматривать как уникальную группу производств, не имеющих аналогов ни в других отраслях малой химии, ни в химической индустрии вообще. Это относится прежде всего к химико-фармацевтической промышленности [61-Специфичность фармацевтической продукции исключительно велика и для ее выпуска необходимы специализированные производства, однако обособление их от других производств тонкого органического синтеза неэффективно. Как показьшает зарубежный опыт, широкая (научная, технологическая, сырьевая кооперация) в развитии этих производств [c.8]
Как показьшает зарубежный опыт, широкая (научная, технологическая, сырьевая кооперация) в развитии этих производств [c.8]
По данным межотраслевого баланса США, где приведена разбивка химической продукции на 5 групп, рассчитана структура удельных затрат на каждую из них в отдельных отраслях промышленности США (табл. 22). Полученные данные позволяют в общих чертах установить, в каких отраслях преобладает использование химических методов переработки и вспомогательных химических материалов, а в каких — применение химической продукции в качестве сырья и основных материалов. С известной степенью условности вспомогательными химическими материалами можно считать группу основных неорганических и органических продуктов (включающую также красители, клей, желатин, взрывчатые вещества и др.), лакокрасочные материалы, а также ПАВ и моющие средства, объединяемые в одну группу с фармацевтическими и парфюмернокосметическими препаратами. К сырью и основным материалам правомерно отнести полимерные материалы и изделия из резины и пластмасс, применяемые в основных процессах (надо иметь в виду, что изделия из резины и пластмасс используют во всех отраслях промышленности и в виде комплектующих деталей оборудования, тары и упаковочных мате -риалов). [c.46]
[c.46]
II группа — химическая переработка каменного угля, торфа и нефти со следующими секциями химическая переработка нефти, гудрона, асфальта, сланцев производство взрывчатых веществ и норохов сухая перегонка каменного угля, коксование и газовые заводы (торф, нефть) производство продукции тонкой химической технологии (красящие вещества, фармацевтические, фотографические продукты). [c.248]
Одна группа продуктов характеризуется особыми технико-экономическими показателями (большая капиталоемкость продукции, высокие нормы затрат энергии, труда, а в ряде случаев и большие нормы расхода сырья и материалов). Это, как правило, предопределяет в конечном итоге высокую стоимость и цену получаемой продукции. В эту группу продуктов входит большинство видов полимерных материалов и некоторые продукты основной химии и промышленности органического син-теза. К ней относится и продукция таких отраслей хи-мической промышленности, как анилинокрасочная, фотохимическая, химико-фармацевтическая и некоторые другие. Данная группа продуктов отличается высокой эффективностью участия в межрайонном разделении труда. Каждый из ее продуктов является продуктом районной специализации, а отрасли и производства, вырабатывающие их, — специализирующими. Производство продуктов второй группы отличается малой и средней капиталоемкостью, в большинстве случаев невысокими нормами затрат энергии, труда, сырья и материалов. Себестоимость и цена, а также порайонные различия в затратах на производство продуктов этой группы (все виды минеральных удобрений, сырья и полупродуктов для их выработки и такие полупродукты органического синтеза, как формалин) также невелики. Все это предопределяет нецелесообразность концентрации их выработки по немногим районам. Каждый из продуктов этой группы, кроме некоторых видов горнохимической продукции, можно и экономически выгодно вырабатывать в любом районе страны. Производства, вырабатывающие продукты данной группы, имеют в комплексе отраслей промышленности районов обслуживающее или вспомогательное значение.
Данная группа продуктов отличается высокой эффективностью участия в межрайонном разделении труда. Каждый из ее продуктов является продуктом районной специализации, а отрасли и производства, вырабатывающие их, — специализирующими. Производство продуктов второй группы отличается малой и средней капиталоемкостью, в большинстве случаев невысокими нормами затрат энергии, труда, сырья и материалов. Себестоимость и цена, а также порайонные различия в затратах на производство продуктов этой группы (все виды минеральных удобрений, сырья и полупродуктов для их выработки и такие полупродукты органического синтеза, как формалин) также невелики. Все это предопределяет нецелесообразность концентрации их выработки по немногим районам. Каждый из продуктов этой группы, кроме некоторых видов горнохимической продукции, можно и экономически выгодно вырабатывать в любом районе страны. Производства, вырабатывающие продукты данной группы, имеют в комплексе отраслей промышленности районов обслуживающее или вспомогательное значение. Так, например, азотные удобрения предназначены для обеспечения нужд сельского хозяйства каждого района, а серная кислота имеет вспомогательное значение в ряде химических и других родственных ей отраслях промышленности в любом из районов страны. Участие продуктов этой группы в межрайонном обмене относительно невелико и с каждым годом, как показывают расчеты, будет сокращаться. [c.70]
Так, например, азотные удобрения предназначены для обеспечения нужд сельского хозяйства каждого района, а серная кислота имеет вспомогательное значение в ряде химических и других родственных ей отраслях промышленности в любом из районов страны. Участие продуктов этой группы в межрайонном обмене относительно невелико и с каждым годом, как показывают расчеты, будет сокращаться. [c.70]
Значительно расширились научные исследования по разработке и совершенствованию технологии и контроля качества стерильных лекарств. Утвержден ряд методических документов и НТД, регла-ментируюшзк требования к этой группе лекарств. ВОЗ ООН разработаны единые международные требования ОМР, предъявляемые к производству стерильных лекарств (соблюдаются более 80 странами мира). В фармацевтическую практику внедрены новые технологии, методы контроля и оборудование, обеспечивающие более высокое качество стерильной продукции. [c.117]
Некондиционная и фальсифицированная медицинская продукция
\n\nФальсифицированная медицинская продукция может не содержать действующего вещества, содержать другое действующее вещество или же правильное действующее вещество, но в неверной дозировке.
\nКроме того, такая продукция, как правило, содержит кукурузный и картофельный крахмал или мел.
\n\nОтмечались случаи токсичности некоторых видов некондиционной и фальсифицированной медицинской продукции, которые содержали либо неправильное действующее вещество в смертельной концентрации, либо другие токсичные химические вещества.
\n\nНекондиционная и фальсифицированная медицинская продукция часто производится в крайне неподходящих для этого и антисанитарных условиях неквалифицированным персоналом, содержит неизвестные примеси и иногда заражена бактериями.
\n\nНекондиционная и фальсифицированная медицинская продукция по своей природе трудно поддается выявлению. По своему внешнему виду она зачастую неотличима от подлинной продукции и может не всегда вызывать ярко выраженную нежелательную реакцию, однако нередко не позволяет провести надлежащее лечение заболевания, для которого она предназначалась, и может приводить к серьезным последствиям для здоровья, включая смерть.
Определение
\n\nНедоброкачественная продукция, также называемая «некондиционной». Такая медицинская продукция является разрешенной, но не соответствует либо стандартам качества, либо техническим условиям, либо ни тому, ни другому.
\n\nНезарегистрированная/нелицензированная медицинская продукция. Это медицинская продукция, не прошедшая процедуру оценки и/или утверждения со стороны национального или регионального органа регулирования для рынка, на котором эта продукция реализуется/распределяется или используется, при соблюдении допустимых условий в соответствии с национальными или региональными нормативно-правовыми требованиями.
\n\nФальсифицированная медицинская продукция. Медицинская продукция, сопровождающаяся заведомо ложной информацией о ее характере, составе или происхождении.
\nВыявление некондиционной или фальсифицированной медицинской продукции
\n\nНекоторые виды фальсифицированной медицинской продукции визуально практически неотличимы от оригинальных препаратов и с большим трудом поддаются выявлению. Тем не менее во многих случаях их можно распознать следующим образом:
Тем не менее во многих случаях их можно распознать следующим образом:
- \n
- внимательно изучить упаковку на предмет оценки ее состояния, наличия орфографических или грамматических ошибок; \n
- проверить, совпадают ли даты производства и истечения срока годности, указанные на внешней упаковке, с датами на первичной упаковке; \n
- оценить внешний вид препарата, его целостность и проверить, не имеет ли он нехарактерный цвет или запах; \n
- как можно скорее показать препарат фармацевту, врачу или другому медицинскому специалисту, если возникло подозрение в его неэффективности или появилась нежелательная реакция на его прием; \n
- сообщить о подозрительной медицинской продукции в национальный орган по регулированию лекарственных средств. \n
Некондиционная и фальсифицированная медицинская продукция и сеть Интернет
\n\nНерегулируемые веб-сайты, социальные сети и приложения для мобильных устройств могут также служить прямыми каналами сбыта некондиционной и фальсифицированной медицинской продукции. Приобретение медицинской продукции у нелицензированных и нерегулируемых поставщиков значительно увеличивает риски для потребителей.
Приобретение медицинской продукции у нелицензированных и нерегулируемых поставщиков значительно увеличивает риски для потребителей.
\nПотребителям следует проявлять осторожность в следующих случаях:
\n- \n
- при получении нежелательных сообщений по электронной почте с рекламой лекарственных препаратов; \n
- при отсутствии подтверждения подлинности продукции; при отсутствии логотипа или сертификата, позволяющего проверить ее законность; \n
- при наличии на упаковке грамматических или орфографических ошибок \n
- если на веб-сайте не указан физический адрес или номер стационарного телефона; \n
- если веб-сайт предлагает рецептурные препараты, не требуя рецепта; \n
- при подозрительно низкой цене на медицинскую продукцию. \n
Перечень контрольных вопросов для проверки лекарственных препаратов, приобретенных в сети Интернет
\n- \n
- Был ли получен именно заказанный препарат? \n
- Верна ли дозировка? \n
- В хорошем ли состоянии упаковка, не загрязнена ли она, имеется ли в ней информационный листок-вкладыш для пациента на том языке, на котором препарат рекламировался на сайте? \n
- Не имеет ли препарат нехарактерного вида, консистенции или запаха? \n
- Не нарушена ли целостность защитных ярлыков? \n
- Указано ли в налоговой декларации или почтовой описи, что речь идет о лекарственных препаратах? \n
- Совпадают ли номер партии и срок годности на первичной (внутренней) и на вторичной (внешней) упаковках? \n
- Не замечали ли вы необычных операций по вашей кредитной карте после оплаты товара? \n
Кто подвергается риску?
\n\nФальсифицированная медицинская продукция производится во многих странах и во всех регионах мира. Власти многих стран и СМИ часто сообщают о проведении успешных операций против производителей некондиционной и фальсифицированной медицинской продукции. В одних сообщениях говорится о пресечении деятельности крупных предприятий, в других — о борьбе с мелкими подпольными производителями. В условиях доступности таблетировочных машин, печей, специализированного оборудования, ингредиентов и упаковочных материалов можно быстро и легко наладить незаконное производство такой продукции.
Власти многих стран и СМИ часто сообщают о проведении успешных операций против производителей некондиционной и фальсифицированной медицинской продукции. В одних сообщениях говорится о пресечении деятельности крупных предприятий, в других — о борьбе с мелкими подпольными производителями. В условиях доступности таблетировочных машин, печей, специализированного оборудования, ингредиентов и упаковочных материалов можно быстро и легко наладить незаконное производство такой продукции.
\nЭтот вопрос затрагивает все страны во всех регионах мира от Северной Америки и Европы до Африки к югу от Сахары, Юго-Восточной Азии и Латинской Америки. То, что раньше считалось проблемой развивающихся стран и стран с низким уровнем дохода, сегодня касается всех. В условиях экспоненциального расширения доступа к сети Интернет лица, занимающиеся изготовлением, распространением и продажей некондиционной и фальсифицированной медицинской продукции, получили доступ к глобальному рынку, включая как отдельных потребителей, так и бизнес-сообщества.
\nКультура самодиагностики и самолечения привела к появлению тысяч нерегулируемых веб-сайтов, бесконтрольно распространяющих некондиционную и фальсифицированную медицинскую продукцию. Тем не менее наибольшее бремя проблемы некондиционной и фальсифицированной медицинской продукции ложится на страны с низким и средним уровнями доходов и страны, переживающие конфликты или гражданские беспорядки, где системы здравоохранения ослаблены или отсутствуют.
\n\nНекондиционная и фальсифицированная медицинская продукция чаще попадает к пациентам в условиях ограниченного доступа к качественным и безопасным медицинским изделиям, ненадлежащего управления и слабости технического потенциала
\n\nСогласно оценкам, в странах с низким и средним уровнями доходов каждая десятая единица медицинской продукции является некондиционной или фальсифицированной.
\nДеятельность ВОЗ
\nМеханизм государств– членов ВОЗ
\n\nМеханизм государств – членов ВОЗ — это глобальный форум, позволяющий странам организовывать совещания, координировать деятельность, принимать решения и проводить мероприятия по борьбе с некондиционной и фальсифицированной медицинской продукцией.
\nМеханизм был создан в целях охраны здоровья населения и содействия доступу к недорогостоящей, безопасной, эффективной и качественной медицинской продукции посредством эффективного сотрудничества между государствами-членами и ВОЗ в сфере предотвращения и пресечения оборота некондиционной и фальсифицированной медицинской продукции и сопутствующих видов деятельности.
\nСистема ВОЗ по надзору и мониторингу
\n\nГлобальная система ВОЗ по надзору и мониторингу начала работать в 2013 г. с целью побудить страны направлять сообщения об инцидентах с некондиционной и фальсифицированной медицинской продукцией в систематизированном и упорядоченном виде и помочь им в проведении более точной и обоснованной оценки этой проблемы. Данная система позволяет:
\n- \n
- оказывать экстренную техническую поддержку, сопоставлять информацию об инцидентах в разных странах и регионах, публиковать предупреждения ВОЗ в отношении медицинской продукции; \n
- формировать корпус подтвержденных фактических данных для более точного отражения глубины и масштаба проблемы некондиционной и фальсифицированной медицинской продукции и причиняемого ею вреда, а также выявлять уязвимые места, недостатки и тенденции.
 \n
\n
\nПо состоянию на ноябрь 2017 г., ВОЗ выпустила 20 глобальных предупреждений в отношении медицинской продукции и многочисленные региональные предупреждения и предоставила техническую поддержку в более чем 100 случаях.
\n\nВОЗ обучила 550 сотрудников регулирующих органов в 141 государстве-члене, сформировав из них всемирную сеть для направлений сообщений о некондиционной и фальсифицированной медицинской продукции в Глобальную систему ВОЗ по надзору и мониторингу. ВОЗ также поддерживает взаимодействие с 18 крупнейшими международными органами по закупкам.
\n\nУпорядоченная система направления сообщений позволяет оперативно реагировать на экстренные ситуации и в самых серьезных случаях публиковать предупреждения. Она также позволяет тщательно анализировать наиболее подверженные риску виды медицинской продукции, уязвимые места и недостатки систем здравоохранения, ущерб, наносимый здоровью населения, и потребности в инвестициях, подготовке кадров и ужесточении мер регулирования и стандартов.
«,»datePublished»:»2018-01-31T14:54:00.0000000+00:00″,»image»:»https://www.who.int/images/default-source/imported/injector.jpg?sfvrsn=388b91f2_0″,»publisher»:{«@type»:»Organization»,»name»:»World Health Organization: WHO»,»logo»:{«@type»:»ImageObject»,»url»:»https://www.who.int/Images/SchemaOrg/schemaOrgLogo.jpg»,»width»:250,»height»:60}},»dateModified»:»2018-01-31T14:54:00.0000000+00:00″,»mainEntityOfPage»:»https://www.who.int/ru/news-room/fact-sheets/detail/substandard-and-falsified-medical-products»,»@context»:»http://schema.org»,»@type»:»Article»};
Рассказы об осуществлении мечты
Западноафриканские страны, как правило, не сформировали полную цепочку фармацевтической промышленности, здесь не только нет местных фармацевтических заводов, но и не в состоянии производить сырье и вспомогательные материалы, необходимые для фармацевтических препаратов. Правительство Мали надеется, что Renfu Africa Pharmaceutical Co., Ltd. сможет активизировать процесс индустриализации фармацевтической промышленности в Мали и создать целостную цепочку фармацевтической промышленности.
После создания Renfu Africa Pharmaceutical, не только решили вопрос локализации фармацевтического производства, но и активно способствовали локализации цепи поставок. В настоящее время осуществляются локальные закупки материалов для внешней упаковки, такие как картонные коробки, этикетки, бутылочки для сиропа и т.п., кроме того привлекаются производители упаковочных материалов для инвестирования в Мали. Поскольку лекарства необходимо доставлять по Мали и в соседние страны, это также в определенной степени способствует развитию логистической отрасли Мали.
Локализация работников также имеет решающее значение. Местные работники не имеют навыков работы в фармацевтической сфере, техническая база тоже относительно слабая, поэтому компания Renfu Africa Pharmaceutical Co., Ltd. стала наращивать подготовку кадров из местных жителей.
Малийская сотрудница изучает фармацевтические технологии
В свои тридцать с лишним лет Гармат был строителем, много работал, зарабатывал мало и нестабильно. Когда он услышал, что Renfu Africa Pharmaceutical Co., Ltd. собирается построить в Мали фармацевтический завод, сразу же пошел и записался. Пройдя обучение и испытательный срок, Гармат официально стал членом компании Renfu. Фармацевтический завод дал ему много возможностей для обучения: всего за три года он вырос из рабочего в менеджера низового звена, хорошо разбирающегося в технологии и знающего китайский язык.
Когда он услышал, что Renfu Africa Pharmaceutical Co., Ltd. собирается построить в Мали фармацевтический завод, сразу же пошел и записался. Пройдя обучение и испытательный срок, Гармат официально стал членом компании Renfu. Фармацевтический завод дал ему много возможностей для обучения: всего за три года он вырос из рабочего в менеджера низового звена, хорошо разбирающегося в технологии и знающего китайский язык.
В настоящее время он является менеджером первого звена в компании Renfu Africa Pharmaceutical, отвечающим за управление процессами и техническое обслуживание оборудования. Его ежедневный график всегда плотен:
07:50‒08:00 Дать поручения работникам, организовывать ремонт и чистку оборудования;
08:00‒08:30 Пойти в энергетическую компанию, чтобы получить и уточнить счет за электроэнергию;
08:30‒10:00 Пойти в аппаратную, чтобы проверить состояние оборудования и контролировать начало работы;
10:00‒11:30 Отключить некоторые механизмы, и контролировать процесс последовательной остановки оборудования;
11:30‒12:00 Отключить все оборудование;
12:00‒12:45 Обеденный перерыв;
12:50‒13:00 Перезагрузка оборудования;
13:30‒15:00 Проследить за очисткой использованной воды;
15:30‒16:30 Записать расход топлива и время работы оборудования, записать состояние при эксплуатации котла и транспортного средства;
16:30‒17:00 Проверить результаты труда работников, подтвердить посещаемость, закрыть дверь и отключить электропитание.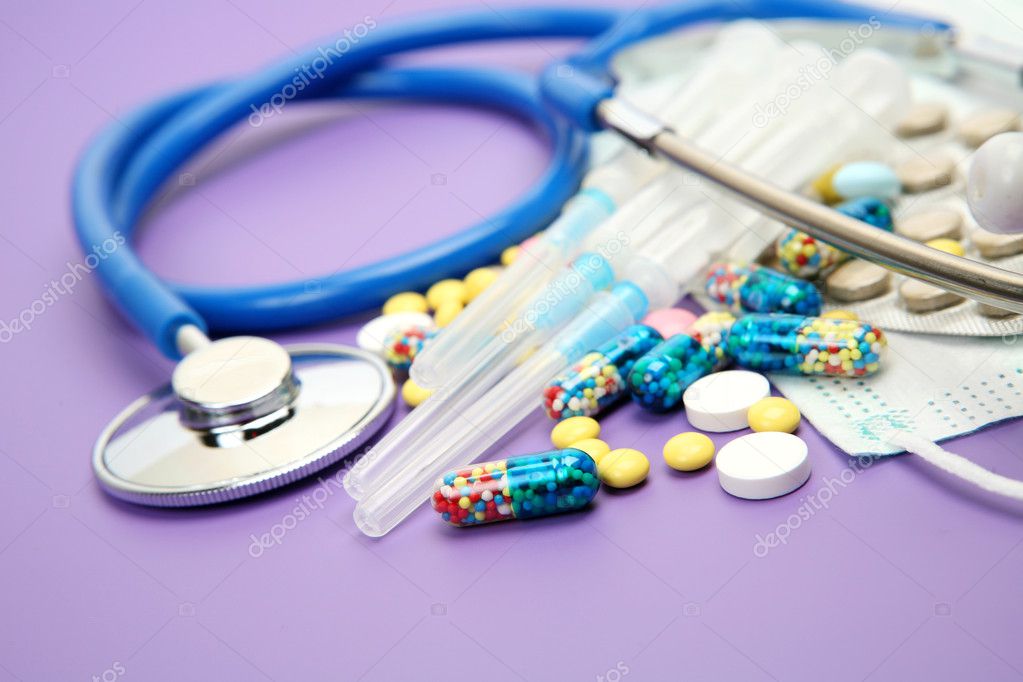
Он всегда говорит о своей работе с гордостью: «Мы производим высококачественные лекарства, которые каждый может себе позволить купить».
Сейчас на фабрике работает более 200 сотрудников из местных жителей, как и Гармат, и более 40 видов производимых их руками лекарств действительно «сделаны в Мали».
В Повестке дня ООН в области устойчивого развития на период до 2030 года было принято к 2030 году обеспечить всеобщую охрану здоровья, в том числе осуществить цель, когда «каждый человек может получить безопасные, эффективные, качественные и доступные основные лекарственные средства и вакцины». По мере успешного производства лекарственных средств «сделано в Мали» малийцы больше не «смотрят на лекарства с испугом», а поспешно устремляются к этой цели.
Код 30 — ТН ВЭД ЕАЭС
ФАРМАЦЕВТИЧЕСКАЯ ПРОДУКЦИЯ
РАЗДЕЛ VI.
 Продукция химической и связанных с ней отраслей промышленности
Продукция химической и связанных с ней отраслей промышленности30 ФАРМАЦЕВТИЧЕСКАЯ ПРОДУКЦИЯ
3001 Железы и прочие органы, предназначенные для органотерапии, высушенные, не измельченные или измельченные, в том числе в порошок; экстракты желез или прочих органов или их секретов, предназначенные для органотерапии; гепарин и его соли; прочие вещества человеческого или животного происхождения, подготовленные для использования в терапевтических или профилактических целях, в другом месте не поименованные или не включенные:
3002 Кровь человеческая; кровь животных, приготовленная для использования в терапевтических, профилактических или диагностических целях; сыворотки иммунные, фракции крови прочие и иммунологические продукты, модифицированные или немодифицированные, в том числе полученные методами биотехнологии; вакцины, токсины, культуры микроорганизмов (кроме дрожжей) и аналогичные продукты:
3003 Лекарственные средства (кроме товаров товарной позиции 3002, 3005 или 3006), состоящие из смеси двух или более компонентов, для использования в терапевтических или профилактических целях, но не расфасованные в виде дозированных лекарственных форм или в формы или упаковки для розничной продажи:
3004 Лекарственные средства (кроме товаров товарной позиции 3002, 3005 или 3006), состоящие из смешанных или несмешанных продуктов, для использования в терапевтических или профилактических целях, расфасованные в виде дозированных лекарственных форм (включая лекарственные средства в форме трансдермальных систем) или в формы или упаковки для розничной продажи:
3005 Вата, марля, бинты и аналогичные изделия (например, перевязочный материал, лейкопластыри, припарки), пропитанные или покрытые фармацевтическими веществами или расфасованные в формы или упаковки для розничной продажи, предназначенные для использования в медицине, хирургии, стоматологии или ветеринарии:
3006 Фармацевтическая продукция, упомянутая в примечании 4 к данной группе:
Фармацевтический продукт – обзор
1 Постановка проблемы
Производство фармацевтических продуктов должно быть одобрено регулирующим органом при условии, что имеется достаточно доказательств, демонстрирующих безопасность и эффективность лекарственного препарата, и что производственный процесс «контролирует», чтобы гарантировать его качество. Эти «контроли» представляют собой набор «допустимых условий эксплуатации», обеспечивающих гарантию качества с учетом различий в материалах и производственных процессах.Их обычно называют Design Space (DS) (Министерство здравоохранения и социальных служб США, 2006 г.).
Эти «контроли» представляют собой набор «допустимых условий эксплуатации», обеспечивающих гарантию качества с учетом различий в материалах и производственных процессах.Их обычно называют Design Space (DS) (Министерство здравоохранения и социальных служб США, 2006 г.).
Идентификация вероятностных DS является сложной задачей, и для типичной практической задачи традиционный подход, основанный на исчерпывающей выборке, требует дорогостоящих вычислений (García-Muñoz et al, 2015). Новая теоретическая и численная основа для определения вероятностного DS с использованием метамоделирования и адаптивной выборки была предложена в Kucherenko et al, 2020. Она была основана на многоэтапном адаптивном методе с использованием метамодели карты вероятностей в качестве критерия принятия-отклонения для оптимизации выборки. для идентификации ДС.
Рассмотрим модель fx→θ→, а вектор функций ограничений g→x→θ→, где x→ — вектор параметров процесса, заданных в ящичной области Hd,θ→, — вектор неопределенных параметров модели, заданных в м -мерном реальном пространстве R м с заданной PDF φθ→. Определить вероятность px→ возникновения нежелательного (анализ оценки надежности) или желательного (фармацевтическая/химическая технология) события как
Определить вероятность px→ возникновения нежелательного (анализ оценки надежности) или желательного (фармацевтическая/химическая технология) события как
(1)px→=Pg→x→θ→≥g→∗=∫Ωx→φθ→dθ→
Здесь g→∗ — вектор заданных порогов, область Ωx→ определяется как Ωx→=θ→:g→x→θ→≥g→∗.Вероятность (1) можно представить в удобном виде:
(2)px→=∫RmIg→x→θ→≥g→∗φθdθ=EθIg→x→θ→≥g→∗,
, где I — индикаторная функция. Определить пространство проектирования (DS) как DSx→px→≥p∗, где p ⁎ — критическое (приемлемое) значение вероятности выполнения ограничений. Для численной оценки грубой силы px→ of требуется N x × N θ прогонов модели, где N x — количество точек процесса в x→ ,Nθ — количество точек выборки в θ→ -пространстве.Для типичной практической задачи это число может быть очень большим, что приводит к дорогостоящим вычислениям. Для таких моделей глобальный анализ чувствительности (GSA) является эффективным практическим инструментом, который может значительно сократить вычислительные затраты и предоставить полезную дополнительную информацию о важности параметров и структуре модели.
GSA — это широко используемый инструмент для определения ключевых параметров, неопределенность которых больше всего влияет на выходные данные модели. В контексте идентификации DS GSA может применяться для определения неопределенных параметров, способствующих принятию наложенных ограничений с потенциальным дальнейшим сокращением модели.Эта проблема связана с проблемой выявления критических областей входов θ→, ответственных за «экстремальные» значения (значения, для которых выполняются ограничения) отклика модели. Он известен как параметр сопоставления факторов GSA. Обычно для этого требуются довольно сложные методы, такие как фильтрация Монте-Карло. Мы предлагаем эффективную формулировку GSA с использованием индикаторной функции Ig→x→θ→≥g→∗ в качестве «выходных данных модели», которая позволяет применять хорошо разработанный метод GSA индексов Соболя.
Для иллюстрации разработанного подхода была рассмотрена задача одноступенчатого реактора периодического действия с двумя «ограниченными» переменными./cdn.vox-cdn.com/uploads/chorus_image/image/63534860/medicaid_bill_37700424.0.jpg) Эта система была представлена Samsatli et al. 1999 и использовано в Kucherenko et al., 2020. Предполагается, что в сосуде фиксированного объема при заданной начальной загрузке раствора А (1 м 3 раствора А с концентрацией 2000моль/м 3 ) протекают следующие реакции. ): 2 A k 1 → B k 2 → C . Профили времени обработки и температуры могут быть скорректированы для поддержания чистоты и скорости производства желаемого продукта B выше определенных уровней (представляющих ограничения в форме g→x;→θ→≥g→∗).Кинетические параметры этой модели θ→ (две энергии активации E и два предэкспоненциальных фактора k ) считаются неопределенными.
Эта система была представлена Samsatli et al. 1999 и использовано в Kucherenko et al., 2020. Предполагается, что в сосуде фиксированного объема при заданной начальной загрузке раствора А (1 м 3 раствора А с концентрацией 2000моль/м 3 ) протекают следующие реакции. ): 2 A k 1 → B k 2 → C . Профили времени обработки и температуры могут быть скорректированы для поддержания чистоты и скорости производства желаемого продукта B выше определенных уровней (представляющих ограничения в форме g→x;→θ→≥g→∗).Кинетические параметры этой модели θ→ (две энергии активации E и два предэкспоненциальных фактора k ) считаются неопределенными.
Идентификация фармацевтической продукции | FDA
Идентификация фармацевтических продуктов (PhPID) ISO 11616 может использоваться для связывания продуктов с таким же или подобным фармацевтическим составом. PhPID — это уникальный идентификатор, рассчитываемый с помощью алгоритма, основанного на идентификации вещества (ISO 11238), лекарственной формы (ISO 11239) и дозировки с единицами измерения (ISO 11240), чтобы связать группу соответствующих лекарственных средств на определенных уровнях. PhPID генерируются на четырех уровнях для конкретного фармацевтического продукта по веществам и указанным веществам на двух уровнях.
PhPID — это уникальный идентификатор, рассчитываемый с помощью алгоритма, основанного на идентификации вещества (ISO 11238), лекарственной формы (ISO 11239) и дозировки с единицами измерения (ISO 11240), чтобы связать группу соответствующих лекарственных средств на определенных уровнях. PhPID генерируются на четырех уровнях для конкретного фармацевтического продукта по веществам и указанным веществам на двух уровнях.
Слой активного вещества PhPID:
- Уровень 1 — термин вещество(а) (ISO 11238)
- Уровень 2 — термин(ы) вещества + концентрация + контрольная концентрация (ISO 11238, ISO 11240)
- Уровень 3 — термин(ы) вещества + лекарственная форма (ISO 11238, ISO 11239)
- Уровень 4 — термин вещество(а) + концентрация + эталонная концентрация + лекарственная форма (ISO 11238, ISO 11239, ISO 11240)
PhPID Слой указанного вещества:
- Уровень 1 — термин «определенное вещество (вещества)» (ISO 11238)
- Уровень 2 — указанный(е) термин(ы) вещества + концентрация + эталонная концентрация (ISO 11238, ISO 11240)
- Уровень 3 — указанный(е) термин(ы) вещества + лекарственная форма (ISO 11238, ISO 11239)
- Уровень 4 — обозначение определенного вещества (веществ) + концентрация + эталонная концентрация + лекарственная форма (ISO 11238, ISO 11239, ISO 11240)
Пример уровней PhPID:
Уровень PhPID 1Вещество: ацетаминофен
Уровень PhPID 2
Вещество: Ацетаминофен
Сила действия: 500
Единица измерения: мг
Вещество: ацетаминофен
Лекарственная форма: Таблетка
Уровень PhPID 4
Вещество: Ацетаминофен
Лекарственная форма: Таблетка
Дозировка: 500
В настоящее время FDA может генерировать региональные идентификаторы PhPID, чтобы связать отечественные лекарственные препараты с использованием терминологии структурированной маркировки продуктов (SPL). Согласованная центральная терминология для лекарственных форм (DF) и путей введения (RoA) необходима для создания глобально уникальных PhPID. Долгосрочной целью FDA является гармонизация и внедрение PhPID на международном уровне.
Согласованная центральная терминология для лекарственных форм (DF) и путей введения (RoA) необходима для создания глобально уникальных PhPID. Долгосрочной целью FDA является гармонизация и внедрение PhPID на международном уровне.
Текущее содержание:
фармацевтическая промышленность | Британика
Фармацевтическая промышленность , открытие, разработка и производство лекарств и медикаментов (фармацевтических препаратов) государственными и частными организациями.
Считается, что современная эра фармацевтической промышленности — выделения и очистки соединений, химического синтеза и компьютерной разработки лекарств — началась в 19 веке, спустя тысячи лет после того, как интуиция, пробы и ошибки привели людей к мысли, что что растения, животные и минералы обладают лечебными свойствами. Объединение исследований в 20-м веке в таких областях, как химия и физиология, расширило понимание основных процессов открытия лекарств.Определение целей для новых лекарств, получение одобрения регулирующих органов от государственных органов и совершенствование методов открытия и разработки лекарств — это одни из задач, стоящих перед фармацевтической промышленностью сегодня. Постоянное развитие и развитие фармацевтической промышленности имеет основополагающее значение для контроля и ликвидации болезней во всем мире.
Объединение исследований в 20-м веке в таких областях, как химия и физиология, расширило понимание основных процессов открытия лекарств.Определение целей для новых лекарств, получение одобрения регулирующих органов от государственных органов и совершенствование методов открытия и разработки лекарств — это одни из задач, стоящих перед фармацевтической промышленностью сегодня. Постоянное развитие и развитие фармацевтической промышленности имеет основополагающее значение для контроля и ликвидации болезней во всем мире.
В следующих разделах приводится подробное объяснение эволюции открытия и разработки лекарств на протяжении всей истории, процесса разработки лекарств в современной фармацевтической промышленности и процедур, которые соблюдаются для обеспечения производства безопасных лекарств.Для получения дополнительной информации о лекарствах см. наркотиков. Подробное описание медицинской практики и роли исследований лекарственных средств в отрасли здравоохранения см. в разделе «Медицина».
История
Происхождение лекарств
Лекарства древних цивилизаций
Самые старые записи о лекарственных препаратах, сделанных из растений, животных или минералов, относятся к ранней китайской, индуистской и средиземноморской цивилизациям. Травяной сборник, который, как говорят, был написан в 28 веке до н. содержат противомалярийные алкалоиды (щелочные органические химические вещества, содержащие азот).Рабочие школы алхимии, процветавшей в Александрии, Египет, во 2 веке до н.э. подготовили несколько относительно чистых неорганических химикатов, включая карбонат свинца, мышьяк и ртуть. Согласно De materia medica , написанному греческим врачом Педанием Диоскоридесом в I веке нашей эры, медь-медь (основной ацетат меди) и сульфат меди прописывались в качестве лекарственных средств. Хотя были предприняты попытки использовать многие минеральные препараты в качестве лекарств, большинство из них оказались слишком токсичными, чтобы их можно было использовать таким образом.
Многие лекарства растительного происхождения, использовавшиеся древними, используются и сегодня. Египтяне лечили запоры стручками сенны и касторовым маслом, а несварение желудка — мятой перечной и тмином. Различные растения, содержащие соединения, подобные наперстянке (сердечные стимуляторы), использовались для лечения ряда заболеваний. Древние китайские врачи использовали ма хуанг, растение, содержащее эфедрин, для различных целей. Сегодня эфедрин используется во многих фармацевтических препаратах, предназначенных для лечения симптомов простуды и аллергии.Греческий врач Гален ( ок. 130– ок. 200 ад) включил в свою аптекарскую лавку (аптеку) в число лекарств опиум и лук. Сегодня производные алкалоидов опия широко используются для облегчения боли, и, хотя лук некоторое время использовался в качестве сердечного стимулятора, он более известен как крысиный яд. Хотя многие лекарственные препараты, используемые Галеном, устарели, он внес важный концептуальный вклад в современную медицину. Например, он был одним из первых практикующих, которые настаивали на чистоте наркотиков.Он также признал важность использования ботанических образцов правильного сорта и возраста для изготовления лекарств.
Например, он был одним из первых практикующих, которые настаивали на чистоте наркотиков.Он также признал важность использования ботанических образцов правильного сорта и возраста для изготовления лекарств.
Фармацевтическая наука в XVI и XVII веках
Фармацевтическая наука заметно улучшилась в 16-м и 17-м веках. В 1546 г. в Нюрнберге появилась первая фармакопея, или собранный список лекарств и лекарственных химикатов с инструкциями по изготовлению фармацевтических препаратов. До этого времени медицинские препараты различались по концентрации и даже по составу.Другие фармакопеи последовали в Базеле (1561 г.), Аугсбурге (1564 г.) и Лондоне (1618 г.). Лондонская фармакопея стала обязательной для всей Англии и, таким образом, стала первым примером национальной фармакопеи. Еще одно важное достижение было инициировано Парацельсом, швейцарским врачом-химиком 16-го века. Он увещевал своих современников не использовать химию, поскольку до него она широко использовалась в спекулятивной науке алхимии и производстве золота. Вместо этого Парацельс выступал за использование химии для изучения приготовления лекарств.
Вместо этого Парацельс выступал за использование химии для изучения приготовления лекарств.
В Лондоне в 1617 году было основано Общество аптекарей (фармацевтов). Это ознаменовало появление фармации как отдельной и отдельной организации. Отделение аптекарей от бакалейщиков было санкционировано королем Яковом I, который также постановил, что только член общества может содержать аптекарскую лавку и производить или продавать фармацевтические препараты. В 1841 году было основано Фармацевтическое общество Великобритании. Это общество курировало образование и подготовку фармацевтов, чтобы обеспечить научную основу профессии.Сегодня профессиональные общества во всем мире играют видную роль в контроле за образованием и практикой своих членов.
В 1783 году английский врач и ботаник Уильям Уизеринг опубликовал свою знаменитую монографию о применении наперстянки (экстракт из цветущей пурпурной наперстянки, Digitalis purpurea ). В его книге «Отчет о наперстянке и некоторых ее лекарственных применениях: с практическими замечаниями о водянке и других заболеваниях» подробно описано использование препаратов наперстянки и включены предложения о том, как можно уменьшить их токсичность. Растения, содержащие соединения, подобные наперстянке, использовались древними египтянами тысячи лет назад, но их использование было неустойчивым. Уизеринг считал, что первичное действие наперстянки оказывалось на почки, тем самым предотвращая водянку (отек). Позже, когда было обнаружено, что вода транспортируется в кровотоке, было обнаружено, что первичное действие наперстянки заключалось в улучшении работы сердца с уменьшением отека в результате улучшения сердечно-сосудистой функции.Тем не менее, наблюдения в монографии Уизеринга привели к более рациональному и научно обоснованному использованию наперстянки и, в конечном итоге, других лекарств.
Растения, содержащие соединения, подобные наперстянке, использовались древними египтянами тысячи лет назад, но их использование было неустойчивым. Уизеринг считал, что первичное действие наперстянки оказывалось на почки, тем самым предотвращая водянку (отек). Позже, когда было обнаружено, что вода транспортируется в кровотоке, было обнаружено, что первичное действие наперстянки заключалось в улучшении работы сердца с уменьшением отека в результате улучшения сердечно-сосудистой функции.Тем не менее, наблюдения в монографии Уизеринга привели к более рациональному и научно обоснованному использованию наперстянки и, в конечном итоге, других лекарств.
Различные фармацевтические продукты нуждаются в сходной терминологии
Abstract
В последнее десятилетие широкое внимание привлекли дискуссии о разработке нормативно-правовой базы для дженериков сложных препаратов, таких как биологические и небиологические сложные препараты. Используемая терминология далека от согласованной и может привести к многочисленным интерпретациям юридических текстов, аналитических документов и руководящих документов, касающихся выхода на рынок, а также возмещения расходов. В этой статье описывается значение соответствующих терминов в различных регионах мира (Европа, США, ВОЗ) и предлагается предложение по общепринятой терминологии в отношении (не)биологических комплексных лекарственных средств.
В этой статье описывается значение соответствующих терминов в различных регионах мира (Европа, США, ВОЗ) и предлагается предложение по общепринятой терминологии в отношении (не)биологических комплексных лекарственных средств.
Электронный дополнительный материал
Электронная версия этой статьи (doi:10.1208/s12248-013-9532-0) содержит дополнительные материалы, доступные авторизованным пользователям.
КЛЮЧЕВЫЕ СЛОВА: биоаналоги, дженерики, небиологические комплексные лекарственные средства, замена, терминология системы дженериков в США (1).Закон Хэтча-Ваксмана привел к развитию индустрии дженериков в результате политики регулирования, разработанной FDA, для которой Закон дал правовую основу. Базовый непатентованный подход, сформулированный FDA и позже принятый другими регулирующими органами, рассматривает копии лекарственных средств, терапевтически эквивалентные их оригинальным продуктам, если они фармацевтически эквивалентны и биоэквивалентны, что означает, что их биодоступность (скорость и степень всасывания) после приема в одинаковые молярные дозы сопоставимы.
Определение биоэквивалентности основано на статистическом сравнении логарифмически преобразованных фармакокинетических характеристик дженерика и оригинального препарата, где оба односторонних 90% доверительных интервала степени всасывания препарата у здоровых добровольцев (AUC 0-t ) и C max находятся в пределах 80 и 125% от эталонного продукта. Фармакокинетический подход является наиболее надежным и предпочтительным способом установления биоэквивалентности и применим для системно активных препаратов.
Целью исследований биоэквивалентности является демонстрация отсутствия статистически значимой разницы в скорости и степени всасывания между тестируемым и эталонным продуктом. Когда тестируемые и референтные продукты фармацевтически эквивалентны и биоэквивалентны, они считаются терапевтически эквивалентными и терапевтически взаимозаменяемыми.
Однако введение концепции биоаналогов для класса крупных, сложных белковых препаратов, производимых в рамках сложного и запутанного производственного процесса, привело к возникновению новых вопросов, касающихся взаимозаменяемости препаратов для отдельных пациентов, и вопросов возмещения расходов, таких как ссылка ценовые системы и терминология, используемая в научных публикациях. Для биоаналогов требуются доклинические и/или клинические исследования в дополнение к физико-химическим анализам (качеству). Кроме того, с 2010 года определена группа небиологических комплексных лекарственных средств (НБПК): небиологический комплексный лекарственный препарат – лекарственное средство, не являющееся биологическим лекарственным средством, где действующее вещество не имеет гомомолекулярной структуры, но состоит из различных (близкородственных и часто наночастиц) структур, которые не могут быть выделены и полностью количественно оценены, охарактеризованы и/или описаны средствами физико-химического анализа.Также неизвестно, какие структурные элементы могут повлиять на терапевтическую эффективность. Состав, качество и эффективность in vivo NBCD в значительной степени зависят от производственных процессов как активного ингредиента, так и состава (2).
Для биоаналогов требуются доклинические и/или клинические исследования в дополнение к физико-химическим анализам (качеству). Кроме того, с 2010 года определена группа небиологических комплексных лекарственных средств (НБПК): небиологический комплексный лекарственный препарат – лекарственное средство, не являющееся биологическим лекарственным средством, где действующее вещество не имеет гомомолекулярной структуры, но состоит из различных (близкородственных и часто наночастиц) структур, которые не могут быть выделены и полностью количественно оценены, охарактеризованы и/или описаны средствами физико-химического анализа.Также неизвестно, какие структурные элементы могут повлиять на терапевтическую эффективность. Состав, качество и эффективность in vivo NBCD в значительной степени зависят от производственных процессов как активного ингредиента, так и состава (2).
В этой статье мы предлагаем стандартизированную терминологию для «дженериков» [(предполагаемых) копий] малых молекул с низким молекулярным весом и аналогичных биологических препаратов и НБЦД. Предлагаемая нами терминология основана на анализе использования терминов в нормативных руководствах по биоаналогам Европейского агентства по лекарственным средствам (EMA), ВОЗ и FDA, а также на вопроснике, который мы разослали различным заинтересованным сторонам, в том числе регулирующим органам, экспертам по регулированию фармацевтическая промышленность, академические исследователи и торговые организации.Ответы этих заинтересованных сторон в этом опросе были анонимизированы или перефразированы и использовались для составления этой рукописи.
Предлагаемая нами терминология основана на анализе использования терминов в нормативных руководствах по биоаналогам Европейского агентства по лекарственным средствам (EMA), ВОЗ и FDA, а также на вопроснике, который мы разослали различным заинтересованным сторонам, в том числе регулирующим органам, экспертам по регулированию фармацевтическая промышленность, академические исследователи и торговые организации.Ответы этих заинтересованных сторон в этом опросе были анонимизированы или перефразированы и использовались для составления этой рукописи.
Нашей конечной целью является достижение глобального консенсуса в отношении терминологии среди всех заинтересованных сторон: новаторов, последующих производителей и регулирующих органов. Это может быть достигнуто, например, с помощью процесса ICH.
EMA
В Европе EMA сыграло ключевую роль в определении научно обоснованного инструмента принятия решений для выдачи регистрационных удостоверений на «аналогичные биологические лекарственные средства». Термин «аналогичный биологический лекарственный препарат» определен в статье 10(4) Директивы 2001/83/ЕС, что является правовой основой системы регулирования, разработанной EMA (3), «где биологический лекарственный препарат, аналогичный референтному биологическому лекарственному препарату, не соответствует условиям определения воспроизведенных лекарственных препаратов, в частности, из-за различий, связанных с сырьем или различиями в процессах производства биологического лекарственного препарата и референтного биологического лекарственного препарата, результатов должны быть проведены соответствующие доклинические испытания и/или клинические испытания, относящиеся к этим состояниям.Тип и количество дополнительных данных, которые должны быть предоставлены, должны соответствовать соответствующим критериям, указанным в Приложении и соответствующих подробных руководящих принципах. Результаты других испытаний и испытаний из досье референтного лекарственного средства не предоставляются».
Термин «аналогичный биологический лекарственный препарат» определен в статье 10(4) Директивы 2001/83/ЕС, что является правовой основой системы регулирования, разработанной EMA (3), «где биологический лекарственный препарат, аналогичный референтному биологическому лекарственному препарату, не соответствует условиям определения воспроизведенных лекарственных препаратов, в частности, из-за различий, связанных с сырьем или различиями в процессах производства биологического лекарственного препарата и референтного биологического лекарственного препарата, результатов должны быть проведены соответствующие доклинические испытания и/или клинические испытания, относящиеся к этим состояниям.Тип и количество дополнительных данных, которые должны быть предоставлены, должны соответствовать соответствующим критериям, указанным в Приложении и соответствующих подробных руководящих принципах. Результаты других испытаний и испытаний из досье референтного лекарственного средства не предоставляются».
Таким образом, аналогичный биологический лекарственный препарат, также известный как «биоаналог», представляет собой продукт, аналогичный уже зарегистрированному биологическому лекарственному средству, так называемый «референтный продукт». В дополнение к современной физико-химической ( in vitro ) характеристике, ключом к тому, чтобы считаться биоаналогом, является наличие достаточных данных клинических испытаний.Это подтверждается недавней статьей членов Рабочей группы по биоаналогам лекарственных препаратов в EMA, в которой говорится, что «любая копия терапевтического белка, которая не была разработана и оценена в соответствии с научными принципами строго сравнительной программы разработки по сравнению с эталонным продуктом, не следует называть биоаналогом. Мы не хотим подразумевать, что другие продукты имеют более низкое качество, эффективность или безопасность, а просто то, что они могут не квалифицироваться как биоаналоги в соответствии с пониманием этого термина в ЕС и, возможно, в других регионах, и, таким образом, могут требовать других терминология, позволяющая проводить четкое различие между различными продуктами (4).
В дополнение к современной физико-химической ( in vitro ) характеристике, ключом к тому, чтобы считаться биоаналогом, является наличие достаточных данных клинических испытаний.Это подтверждается недавней статьей членов Рабочей группы по биоаналогам лекарственных препаратов в EMA, в которой говорится, что «любая копия терапевтического белка, которая не была разработана и оценена в соответствии с научными принципами строго сравнительной программы разработки по сравнению с эталонным продуктом, не следует называть биоаналогом. Мы не хотим подразумевать, что другие продукты имеют более низкое качество, эффективность или безопасность, а просто то, что они могут не квалифицироваться как биоаналоги в соответствии с пониманием этого термина в ЕС и, возможно, в других регионах, и, таким образом, могут требовать других терминология, позволяющая проводить четкое различие между различными продуктами (4).
Другим важным термином, который следует учитывать, является «терапевтическая эквивалентность» двух лекарственных средств: формального определения этого термина в законодательстве EMA нет. Его можно понимать как эквивалент свойств безопасности и эффективности двух лекарственных средств, вводимых в одинаковой дозе и одним и тем же путем.
Его можно понимать как эквивалент свойств безопасности и эффективности двух лекарственных средств, вводимых в одинаковой дозе и одним и тем же путем.
«Прослеживаемость» определяется как возможность проследить каждую отдельную единицу лекарственного средства от источника до конечного пункта назначения и наоборот .Директива 2010/84/ЕС также гласит, что «государства-члены ЕС должны обеспечить, с помощью методов сбора информации и, при необходимости, путем отслеживания сообщений о подозреваемых побочных реакциях, принятие всех соответствующих мер для четкого выявления любых биологических лекарственное средство, прописанное, отпускаемое или продаваемое на их территории, в отношении которого поступил отчет о предполагаемой нежелательной реакции, с должным учетом названия лекарственного средства в соответствии со Статьей 1(20) и номера серии (5).»
Определения терминов «взаимозаменяемый», «заменяемый», «заменяемый (способный)» и «переключаемый» не предоставлены EMA, поскольку оценка этих понятий не входит в компетенцию EMA. Решения о взаимозаменяемости или замене принимаются национальными компетентными органами. Европейские национальные компетентные органы по-разному относятся к взаимозаменяемости инновационных продуктов и их биоаналогов. Основные государства-члены Европейского союза (включая Францию, Германию, Великобританию, Италию и Испанию) отказались от практики замены биопрепарата фармацевтом без согласия врача («автоматическая замена»).
Решения о взаимозаменяемости или замене принимаются национальными компетентными органами. Европейские национальные компетентные органы по-разному относятся к взаимозаменяемости инновационных продуктов и их биоаналогов. Основные государства-члены Европейского союза (включая Францию, Германию, Великобританию, Италию и Испанию) отказались от практики замены биопрепарата фармацевтом без согласия врача («автоматическая замена»).
Наконец, ответы в опросе ясно показали различное толкование респондентами терминов замещающий (заменяемый) и переключаемый.
FDA
Закон о ценовой конкуренции и инновациях в отношении биологических препаратов, закон BPCI (2009 г.) описывает общую политику регулирующих органов США в отношении биоаналогов (6). В феврале 2012 г. были опубликованы три проекта документов, в которых более подробно предлагались протоколы, которым необходимо следовать: «Научные соображения при демонстрации биоподобия эталонному продукту (7)», «Соображения качества при демонстрации биоподобия эталонному белковому продукту (8)». и «Биоаналоги: вопросы и ответы, касающиеся реализации закона BPCI» (9).Раздел 351(i) Закона о службе общественного здравоохранения определяет биоподобие как означающее, что «биологический продукт очень подобен эталонному продукту, несмотря на незначительные различия в клинически неактивных компонентах» и что «нет клинически значимых различий между биологическими продукт и эталонный продукт с точки зрения безопасности, чистоты и эффективности продукта».
и «Биоаналоги: вопросы и ответы, касающиеся реализации закона BPCI» (9).Раздел 351(i) Закона о службе общественного здравоохранения определяет биоподобие как означающее, что «биологический продукт очень подобен эталонному продукту, несмотря на незначительные различия в клинически неактивных компонентах» и что «нет клинически значимых различий между биологическими продукт и эталонный продукт с точки зрения безопасности, чистоты и эффективности продукта».
Закон о BPCI признает два уровня: биоподобие и «взаимозаменяемость». Для взаимозаменяемости требуется более высокий уровень доказательств сходства, чем для биоподобия, и это дает дополнительное преимущество продукту: «термин «взаимозаменяемость» или «взаимозаменяемость» в отношении биологического продукта, который, как показано, соответствует описанным стандартам. в подразделе (k) (4), означает, что биологический продукт может быть заменен эталонным продуктом без вмешательства поставщика медицинских услуг, который прописал эталонный продукт (закон BPCI). На этикетке продукта должна быть указана информация о том, что он является биоаналогичным или взаимозаменяемым с эталонным продуктом.
На этикетке продукта должна быть указана информация о том, что он является биоаналогичным или взаимозаменяемым с эталонным продуктом.
Термины «переключение» и «назначение» используются в контексте биосимиляров, где возможность переключения относится к изменению продукта (со ссылки на биоаналог или наоборот ) у пациента в ходе курса лечения. Назначаемость — это термин, используемый для выбора препаратов в начале терапии (10).
Другие регионы
В сентябре 2011 г. проведен анализ Konski et al .было опубликовано сравнение нормативных правил в США, Европе, Китае и Индии (11). Система биоаналогов ЕС была принята Австралией и послужила основополагающими принципами для путей распространения в Канаде (2010 г.), Японии (2009 г.), Малайзии, Южной Африке (2010 г.) и других странах.
Позиция ВОЗ
В 2009 г. ВОЗ выпустила руководство по оценке «аналогичных биотерапевтических продуктов» (SBP), предназначенное для предоставления рекомендаций по разработке и оценке таких биотерапевтических средств (12). Вакцины, продукты, полученные из плазмы, и их рекомбинантные аналоги исключены из области применения этого документа.
Вакцины, продукты, полученные из плазмы, и их рекомбинантные аналоги исключены из области применения этого документа.
В соответствии с рекомендациями ВОЗ, СБП должен быть аналогичен лицензированному биотерапевтическому продукту, для которого имеются существенные доказательства безопасности и эффективности. Лекарственная форма и способ введения СБП должны быть такими же, как и для референтного биологического препарата (РБП). Биотерапевтические препараты, сходство которых с RBP не доказано, как указано в данном руководстве, не следует описывать как «похожие» или называть «SBP».Традиционно национальные регулирующие органы требовали использования эталонного продукта, имеющего национальную лицензию, для лицензирования непатентованных лекарственных средств. Эта практика может оказаться неприемлемой для стран, в которых отсутствуют лицензированные на национальном уровне ОДП. ВОЗ использует следующее определение «взаимозаменяемости»: «Взаимозаменяемый фармацевтический продукт — это продукт, который терапевтически эквивалентен препарату сравнения и может быть заменен препаратом сравнения в клинической практике». Автоматическая замена не упоминается.
Автоматическая замена не упоминается.
СПИСОК ТЕРМИНОЛОГИЙ
Предлагаемый нами список терминов основан на анализе нормативных указаний в мире и ответов на разосланный нами вопросник.
Непатентованный лекарственный препарат
Лекарственный препарат, сравнимый с референтным лекарственным препаратом по лекарственной форме, силе действия, способу введения, качеству и эксплуатационным характеристикам, а также по назначению.
Биологический продукт
Биологический продукт представляет собой продукт, полученный из живого материала (такого как клетки или ткани), который используется для лечения или лечения болезней.Биологические продукты включают широкий спектр продуктов, таких как вакцины, кровь и компоненты крови, аллергены, соматические клетки, генные терапевтические препараты, ткани и рекомбинантные терапевтические белки. Биологические продукты могут состоять из сахаров, белков или нуклеиновых кислот или сложных комбинаций этих веществ или, возможно, из живых существ, таких как клетки и ткани. Биологические продукты выделяют из различных природных источников — человека, животных или микроорганизмов — и могут быть получены методами биотехнологии.
Биологические продукты выделяют из различных природных источников — человека, животных или микроорганизмов — и могут быть получены методами биотехнологии.
Биоподобный продукт/Аналогичный биологический лекарственный препарат
Аналогичный биологический лекарственный препарат (также известный как биоаналог) – это биологический продукт, разрешенный в соответствии с сокращенным регламентом, требующим сходства с уже лицензированным биологическим продуктом (эталонным препаратом) в физико-химическом отношении, в vitro и биологические характеристики in vivo и клинические данные, показывающие сходство эффективности, безопасности и иммуногенности.
Небиологический комплексный лекарственный препарат (НБЦД)
Лекарственный препарат, не являющийся биологическим лекарственным средством, в котором действующее вещество не имеет гомомолекулярной структуры, а состоит из различных (близкородственных и часто наночастиц (13,14 )) структуры, которые не могут быть выделены и полностью количественно оценены, охарактеризованы и/или описаны средствами физико-химического анализа. Также неизвестно, какие структурные элементы могут повлиять на терапевтическую эффективность. Состав, качество и эффективность in vivo NBCD в значительной степени зависят от производственных процессов как активного ингредиента, так и состава (2). Примерами NBCD являются, среди прочего, липосомы, железо-углеводные («железо-сахар») препараты и глатирамоиды.
Также неизвестно, какие структурные элементы могут повлиять на терапевтическую эффективность. Состав, качество и эффективность in vivo NBCD в значительной степени зависят от производственных процессов как активного ингредиента, так и состава (2). Примерами NBCD являются, среди прочего, липосомы, железо-углеводные («железо-сахар») препараты и глатирамоиды.
Терапевтический эквивалент
Два лекарственных препарата с системным действием являются терапевтически эквивалентными, если они фармацевтически эквивалентны и если их биодоступность после введения в одной и той же молярной дозе аналогична до такой степени, что их эффекты в отношении как эффективности, так и безопасности будут одинаковыми. быть по существу одинаковым.Это считается доказанным, если 90% доверительные интервалы отношений для log AUC 0-t и C max между двумя препаратами лежат в диапазоне 80,00–125,00%. Фармацевтическая эквивалентность подразумевает одинаковое количество одного и того же активного вещества (веществ) в одной и той же лекарственной форме для одного и того же пути введения и соответствия одним и тем же или сопоставимым стандартам.
Лекарственные препараты, классифицируемые как терапевтически эквивалентные, могут быть взаимозаменяемы с полным расчетом на то, что замененный продукт будет давать такой же клинический эффект и профиль безопасности, что и прописанный препарат.
Взаимозаменяемость
Терапевтическая эквивалентность двух различных продуктов позволяет производить взаимозаменяемость продуктов. Взаимозаменяемость может быть на уровне популяции, что означает, что оба продукта могут использоваться для лечения одного и того же состояния в одной и той же популяции. Взаимозаменяемость на индивидуальном уровне означает, что у отдельного пациента продукты можно чередовать или переключать. Взаимозаменяемость на индивидуальном уровне является условием замены.
Замена
Политика, разрешающая замену на индивидуальном уровне лекарственного препарата на аналогичный/биоэквивалентный продукт.
Возможность переключения
Смена препарата ( e . g . , с эталонного препарата на биоаналог или наоборот ) у пациента в процессе лечения.
, с эталонного препарата на биоаналог или наоборот ) у пациента в процессе лечения.
Прослеживаемость
Возможность проследить каждую отдельную единицу лекарственного средства от источника до конечного пункта назначения и наоборот .
Экстраполяция
Возможность использовать клинические данные, показывающие безопасность и эффективность по одному показанию ( эталонное показание ), чтобы заявить о безопасности и эффективности по другим показаниям.Экстраполяция касается экстраполяции четырех различных аспектов: эффективности, безопасности, иммуногенности и взаимозаменяемости, и может касаться показаний, популяции или того и другого.
Фармацевтическая промышленность — реальная стоимость здравоохранения
Дэвид Белк, доктор медицины и
Пол Белк, доктор философии
Моя новая книга
Великая американская афера в сфере здравоохранения: как откаты, сговор и пропаганда резко увеличили расходы на здравоохранение в США
Теперь можно купить на Amazon. Вот ссылки:
Вот ссылки:
Мягкая обложка
Электронная книга
Введение
В предыдущих разделах этого веб-сайта я писал о странной двухуровневой системе ценообразования на лекарства, отпускаемые по рецепту. Большинство непатентованных лекарств обычно стоят всего несколько копеек за дозу. К ним относятся многие из наших самых полезных лекарств. Но фирменные лекарства, которые обычно являются новейшими препаратами, могут стоить в сотни раз дороже — слишком дорого для некоторых людей даже со страховкой.
Конечно, двухуровневые системы ценообразования не являются уникальными для отпускаемых по рецепту лекарств.Мы все знаем, что можем получить «бренд супермаркета» за меньшие деньги, чем известный бренд для большинства продуктов. А в отделе безрецептурного отпуска в аптеке мы знаем, что платим за аспирин Bayer на несколько долларов больше, чем за точно такое же лекарство с этикеткой Walgreens. Но в этих случаях разница в цене никогда не бывает в сотни раз больше. Кроме того, мы гораздо лучше осведомлены о точных ценах на эти продукты, чем о ценах на лекарства, отпускаемые по рецепту.
Итак, вопрос в том, почему?» Как система дошла до того, что многие из наших лекарств, отпускаемых по рецепту, дешевле молока, а некоторые дороже, чем роскошные автомобили? И почему мы позволили этому случиться?
Наша «сделка» с фармацевтическими компаниями
Как и все в медицине, в этом вопросе есть сложности, но в центре все сводится к чему-то довольно простому: фармацевтические компании сказали нам, что мы должны платить сверхвысокие цены за запатентованные лекарства, чтобы у них были деньги для разработки новых чудо-лекарств. .И мы сказали что-то вроде: «Хорошо, бери, что тебе нужно».
Итак, здесь я хотел бы задать два вопроса: что мы получаем в обмен на эти чрезвычайные расходы? И не пора ли пересмотреть сделку?
Во-первых, давайте поговорим о том, сколько мы платим. Как почти все в медицине, «мы» в США платим за лекарства, отпускаемые по рецепту, гораздо больше, чем почти кто-либо еще в мире. Известные бренды всегда стоят дороже, чем дженерики, но препараты известных брендов стоят в США гораздо дороже, чем в остальном мире.
Фармацевтические компании с этим не поспорят. График ниже взят из финансовых отчетов 13 крупнейших фармацевтических компаний мира. Это показывает, что 45% их общего совокупного дохода с 2011 года приходилось исключительно на продажи в США
.
Рисунок 1: Доля общей выручки 13 крупнейших фармацевтических компаний от продаж в США по сравнению с продажами во всех других странах за период 2011–2018 гг.
Итак, здесь, в У.С., имея 4-5% населения земного шара и 33% населения развитого мира, мы покрываем 45% всей фармацевтической выручки?
Давайте посмотрим на это с другой стороны. Рассмотрим следующую таблицу, в которой сравниваются цены, которые аптеки в США платят за некоторые часто назначаемые лекарства, с национальным страхованием Британской Колумбии для тех же лекарств.
| Лекарства и дозы | Цена в США | Цена в Канаде |
| Брилинта 90 мг | 5 долларов. 99 за таблетку 99 за таблетку | $1,67 за таблетку |
| Гиленья 0,5 мг | 265,03 $ за капсулу | $91,30 за капсулу |
| Хумалог Инсулин 100 ЕД/мл | 26,14 $ за мл | 2,78 $ за мл |
| Прадакса 150 мг | $6,92 за капсулу | $1,78 за капсулу |
| Спирива 18 мкг | $13,72 за капсулу | $1,91 за капсулу |
| Ксарелто 20 мг | 14 долларов.37 за таблетку | 3,07 доллара США за таблетку |
Таблица 1: Сравнение цен на оригинальные лекарства в США и Канаде.
Разница даже больше, чем кажется. Во-первых, потому что цены для Канады указаны в канадских долларах и, во-вторых, потому что цены для США — это цены, которые аптеки платят за эти лекарства.
Почему разница? Потому что, хотя аптеки в других странах покупают лекарства у тех же поставщиков и фармацевтических компаний, что и наши аптеки, они платят лишь часть цены, которую платят наши аптеки.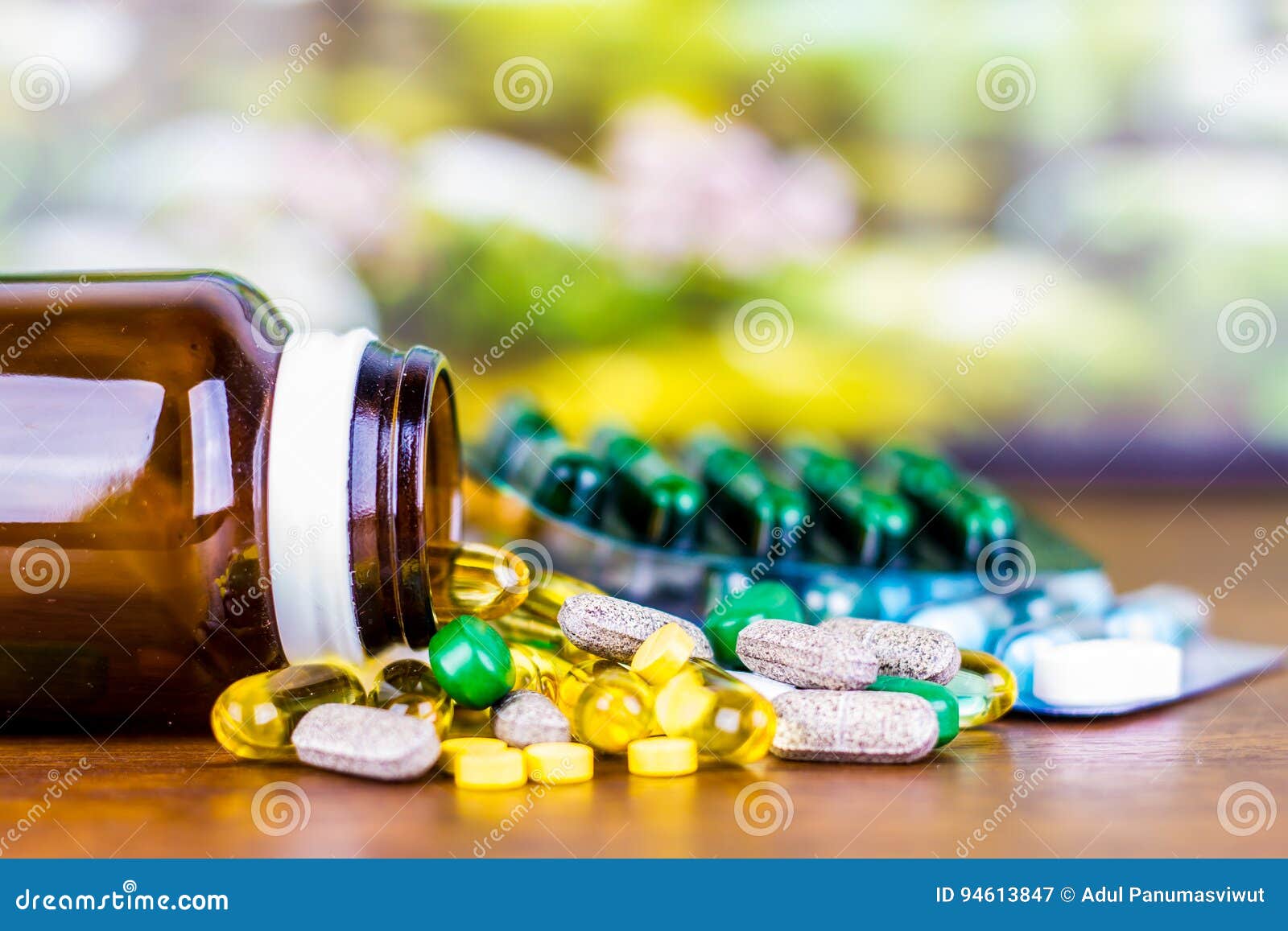
Их часть сделки
Итак, мы в США просто болваны, платя во много раз больше за ту же таблетку, что и пациент в Ванкувере? Возможно, но прежде чем мы углубимся в это, нам нужно взглянуть на другую часть сделки. Фармацевтические компании говорят нам, что они превращают эти высокие цены в исследования новых лекарств от болезней. Это правда, мы в США, похоже, берем на себя большую часть исследований для остального мира, но если мы лечим болезни, возможно, это того стоит.
Другими словами, давайте посмотрим, действительно ли фармацевтические компании выполняют свою часть сделки, а затем вернемся и решим, сколько мы должны им заплатить.
Итак, теперь мы рассмотрим исследовательский вопрос: действительно ли фармацевтические исследования стоят так дорого, что даже при тех ценах, которые они устанавливают, у них почти не остается денег в конце каждого года? Хороший способ узнать это — посмотреть их годовую финансовую отчетность. Каждый год каждая публично торгуемая компания должна подавать годовой финансовый отчет в SEC, в котором перечислены годовые доходы, детализированы затраты, прибыль и т. д.
д.
Я изучил годовые финансовые отчеты 13 крупнейших фармацевтических компаний за 8 лет (2011-2018).Это были одни из крупнейших в мире фармацевтических компаний, на долю которых приходилось в общей сложности почти половина всех мировых фармацевтических продаж тех лет.
Я загрузил каждый из просмотренных здесь отчетов и перечислил страницы, содержащие всю информацию, которую я использовал, рядом с каждой ссылкой. Я также подготовил четырех-пятистраничное резюме того, что, по моему мнению, было моим самым важным выводом о каждой компании. Я связал эти резюме с названием каждой фармацевтической компании на веб-странице.
Начнем с одного из этих отчетов. Хорошим примером является годовой отчет Pfizer за 2011 год. Сам отчет состоит из 117 страниц, но не волнуйтесь, многое из того, что нам нужно знать, можно найти на странице 17, которую я показываю ниже. (страница документа в формате PDF).
Таблица 2: Финансовый обзор Pfizer за 2011 год.
На странице 17 вы найдете приведенную выше таблицу, которая представляет собой анализ консолидированных отчетов о прибылях и убытках Pfizer. Из первой строки видно, что выручка Pfizer в 2011 году составила чуть более 67 миллиардов долларов.Несколькими строками ниже вы можете увидеть, что в том же году они потратили чуть более 9 миллиардов долларов на исследования и разработки. Хорошо, 9 миллиардов долларов — это большие деньги. Это было почти 14% от их общего дохода.
Но что действительно интересно, так это то, что вы можете видеть, что Pfizer потратила более чем в два раза больше на маркетинг (коммерческие, информационные и административные расходы), чем на исследования; более 19 миллиардов долларов! И посмотрите на их прибыль за этот год. Они получили чуть более 10 миллиардов долларов чистой прибыли (после уплаты налогов), что, кстати, больше, чем они потратили на свои исследования за тот год.
Таким образом, затраты на исследования не съели весь пирог доходов Pfizer в 2011 году. Но это финансовый отчет одной фармацевтической компании за один год. Как насчет остальных?
Но это финансовый отчет одной фармацевтической компании за один год. Как насчет остальных?
Как я уже говорил, я просмотрел финансовые отчеты 13 крупных фармацевтических компаний за семь лет и вот некоторые из них:
— Совокупный общий доход всех 13 компаний за 8 лет составил около 3,78 трлн долларов.
— Совокупная общая прибыль этих компаний составила около 744 миллиардов долларов.
— Все 13 фармацевтических компаний потратили в общей сложности 643 миллиарда долларов на исследования.
— Общая сумма, которую они потратили на маркетинг, была примерно на 60% больше, чем на исследования: 1,04 триллиона долларов.
Вот та же информация на двух графиках:
Рисунок 2: Общая совокупная прибыль, полученная всеми 13 крупными фармацевтическими компаниями в период с 2011 по 2018 год, по сравнению с суммами, потраченными на маркетинг и исследования за тот же период времени. Доля общего дохода, выделенная для каждого из них, приведена ниже (рис. 3).
3).
Рисунок 3
Как видите, фармацевтические компании много тратят на исследования, но их бюджеты на исследования ничтожны по сравнению с их маркетинговыми бюджетами. Они также получали в среднем больше прибыли каждый год, чем тратили на исследования.
Итак, давайте сделаем некоторые оценки. Просто в качестве примера возьмем ту дозу Xarelto, которую мы получаем за 14,37 доллара, а канадцы — около 3 долларов. Производство таблетки, скорее всего, стоит всего несколько центов (мы знаем это по стоимости дженериков), поэтому 14 долларов.37 в основном прибыль. Но они берут (с нас в США) 14,37 доллара, чтобы покрыть расходы на его обнаружение.
Тем не менее, по их собственным заявлениям, только около 2,44 доллара из 14,37 доллара (17%) идут на исследования. Еще 2,73 доллара — это чистая прибыль после уплаты налогов, а колоссальные 27%, или около 3,88 доллара, из этой 14,37-долларовой таблетки идут не ученым из фармацевтических компаний, а на покупку рекламы всех тех лекарств, которые вы так любите. Таким образом, большая часть того, что мы «покупаем», когда платим самые высокие в мире цены на лекарства, — это высокие прибыли корпораций и множество телевизионных рекламных роликов мужчин средних лет с очень красивыми женами.
Таким образом, большая часть того, что мы «покупаем», когда платим самые высокие в мире цены на лекарства, — это высокие прибыли корпораций и множество телевизионных рекламных роликов мужчин средних лет с очень красивыми женами.
Что это значит, когда говорят «исследование»?
Но мы пока не можем остановиться. По их собственным отчетам, фармацевтические компании вложили около 17% высоких затрат на лекарства обратно в исследования. Давайте посмотрим, действительно ли эти деньги идут туда, куда мы думаем. И пока мы ищем, мы получим некоторое представление о другом вопросе о фармацевтических исследованиях, а именно: «Почему многие новые лекарства оказываются не лучше, чем старые, и почему так много отзывается из-за проблем с безопасностью». ?»
Когда мы думаем об исследованиях, мы можем думать об ученых в белых халатах, умело синтезирующих новые соединения и добросовестно измеряющих их эффекты.Это действительно происходит при разработке и тестировании новых лекарств, и, конечно же, деньги, потраченные на это, поступают из бюджета исследований. Но деньги на исследования также идут во многие места, которых вы, возможно, не ожидаете.
Но деньги на исследования также идут во многие места, которых вы, возможно, не ожидаете.
Во-первых, исследования покупают исследования лекарств. Это то, что делают фармацевтические компании, когда лекарство уже разработано, и они хотят увидеть, действительно ли оно лечит болезнь, которую должно лечить. Обычно в этих исследованиях существует довольно высокий стандарт успеха, и компании очень тяжело, когда кто-то терпит неудачу.
Так что же произойдет, если лекарство почти подействует? Во-первых, это означает, что препарат, вероятно, мало что добавляет к медикаментозной терапии. Но слишком часто фармацевтическая компания просто повторяет исследование. Эти повторные исследования дают слепому шансу еще одну возможность представить лекарство полезным. Так что часть денег, потраченных на «исследования», на самом деле используется для того, чтобы посредственные продукты выглядели лучше, чем они есть на самом деле.
Он также покупает «незавершенные» исследования, за которые компания платит за поглощение другой компании, надеясь, что у новой компании могут быть какие-то ценные лекарства в разработке. Другими словами, эта часть исследовательского бюджета может быть использована в основном для корпоративных поглощений.
Другими словами, эта часть исследовательского бюджета может быть использована в основном для корпоративных поглощений.
Но вот где идея фармацевтических «исследований» действительно переворачивается с ног на голову: фармацевтические исследования иногда практически неотличимы от маркетинга.
В лучшие времена грань между «исследованиями» и «маркетингом» довольно размыта. В конце концов, что такое исследование и что такое маркетинг? Ответы на эти вопросы не так очевидны, как вы думаете.Многое из того, что определяет затраты на исследования и маркетинг, является решением, оставленным на усмотрение фармацевтических компаний, и они могут быть довольно творческими в том, как они распределяют эти затраты.
В своем финансовом отчете за 2007 год компания «Рош» перераспределила почти 800 миллионов швейцарских франков из своего маркетингового бюджета в отчете за 2006 год на исследовательский бюджет (PDF, стр. 138). Это показывает, как даже фармацевтические компании не могут определиться с определением «исследования». Кроме того, у Bristol-Myers Squibb недавно были отдельные списки для маркетинга и рекламы.Это означает, что по какой-то причине Bristol-Myers Squibb не считала рекламу составной частью маркетинга до 2014 года.
Кроме того, у Bristol-Myers Squibb недавно были отдельные списки для маркетинга и рекламы.Это означает, что по какой-то причине Bristol-Myers Squibb не считала рекламу составной частью маркетинга до 2014 года.
Почему такая путаница? Во-первых, многие исследования должны проводиться за пределами лаборатории, а в медицине вам, очевидно, нужно ходить к врачам и смотреть, насколько хорошо новые лекарства действуют на больных пациентов. Но врачи также являются вашими основными клиентами — именно они решают, прописывать ли вам лекарства. И они ваши главные защитники — люди доверяют им, когда они решают, стоит ли принимать лекарство.
Таким образом, наем практикующих врачей для оценки новых лекарств создает потенциальный конфликт интересов для этих врачей, еще больше размывая линию исследований и маркетинга. Подумайте вот о чем: многие из тех самых врачей, которые в конечном итоге будут прописывать эти новые лекарства своим пациентам, сначала нанимаются фармацевтическими компаниями для оценки лекарств. И именно их оценка представляется FDA как часть решения о том, стоит ли одобрять препарат для использования пациентами.
И именно их оценка представляется FDA как часть решения о том, стоит ли одобрять препарат для использования пациентами.
Есть ли в этом проблема? Что ж, рассмотрим следующий сценарий:
Классы в школьном округе слишком велики, и хотя учителя английского языка могут готовить и проводить уроки, у них нет времени достаточно быстро оценить все работы своих учеников.Решение: наймите внешних оценщиков, чтобы они читали и оценивали работы. Это не проблема — в городе полно английских специалистов, добросовестных и более чем квалифицированных. Проблема в том, что у школы нет денег, чтобы платить учащимся (это причина, по которой классы стали такими большими).
Тем не менее, это богатый город, и Директору приходит в голову очень умная идея. Просто позвольте студентам нанять своих собственных оценщиков. Конечно, оценщик должен иметь степень по английскому языку и соответствующий опыт, но в остальном студент может выбрать (и заплатить) кого пожелает.И, конечно же, если его не устраивает его первоклассник, он может нанять другого оценщика для своих следующих работ. Как вы думаете, много ли действительно суровых оценщиков возьмут на работу, не говоря уже о повторном приеме на работу? Хотите угадать, сколько из этих работ получат оценку ниже «А»?
Как вы думаете, много ли действительно суровых оценщиков возьмут на работу, не говоря уже о повторном приеме на работу? Хотите угадать, сколько из этих работ получат оценку ниже «А»?
Теперь этим врачам платят не за то, чтобы они игнорировали явные недостатки в исследованиях, финансируемых фармацевтическими компаниями. Но от них ожидается, что они будут действовать по своему усмотрению, и им, как правило, платят довольно хорошо (какая компания рискнет заплатить меньше людям, которые будут определять, будут ли одобрены их продукты на рынке?).Они также знают, что только фармацевтическая компания решает, просить ли их оценивать будущие исследования. И деньги, которые компания платит каждому из этих врачей, поступают непосредственно из бюджета исследований.
Кроме того, на фармацевтическую промышленность приходится около 65% бюджета FDA на надзор за лекарствами для людей. С 1992 года фармацевтическим компаниям было разрешено платить FDA сборы с потребителей рецептурных препаратов, чтобы «помочь» FDA в процессе утверждения лекарств для продажи и распространения в США. S. Эти сборы с пользователей, уплачиваемые FDA, теперь составляют большую часть денег, которые FDA получает для надзора за фармацевтическими компаниями, и, конечно же, они также являются частью исследовательского бюджета фармацевтических компаний.
S. Эти сборы с пользователей, уплачиваемые FDA, теперь составляют большую часть денег, которые FDA получает для надзора за фармацевтическими компаниями, и, конечно же, они также являются частью исследовательского бюджета фармацевтических компаний.
Возвращаясь к этой «сделке», которую мы заключили
Теперь, когда мы поближе рассмотрели, как тратятся деньги после того, как их получили фармацевтические компании, давайте вернемся к сделке — той, по которой мы в США согласились платить за те же лекарства гораздо больше, чем кто-либо другой в весь мир — и спросите: «Как мы вообще пришли к этой сделке?»
На любом рынке реальная сделка может состояться только тогда, когда у каждой из сторон есть возможность уйти.Если вы считаете, что гамбургер слишком дорог в одном магазине, вы можете купить его в другом магазине. Или вы решили вместо этого купить курицу. Если владелец ранчо не может заработать на продаже вам говядины, он продаст ее кому-то другому. Или, может быть, он решит разводить кур. Где-то там вы двое соглашаетесь, сколько стоит продукт, и это то, что вы платите.
Где-то там вы двое соглашаетесь, сколько стоит продукт, и это то, что вы платите.
Но можно ли действительно «торговаться» при покупке лекарств, отпускаемых по рецепту? Подумайте об этом, когда врач выписывает рецепт, это единственный препарат, который вы можете купить на законных основаниях.Ваш единственный выход — вообще не принимать лекарства и оставаться больным. И если болезнь, которая у вас есть, может убить вас, то у вас есть выбор буквально «ваши деньги или ваша жизнь». Большинство людей не решат умереть, чтобы сэкономить деньги, даже если это их большая часть. Итак, поскольку пациент действительно не может просто уйти, у него нет реальной возможности торговаться.
Но тогда почему остальной мир платит гораздо меньше, чем мы? Ответ заключается в том, что, хотя отдельные пациенты практически не имеют права торговаться при покупке лекарств, отпускаемых по рецепту, это совсем не относится к правительствам.Практически любое другое правительство в мире считает, что фармацевтические компании скорее значительно снизят цены, чем просто не будут продавать свою продукцию в той или иной стране. Таким образом, другие правительства торгуются с фармацевтическими компаниями от имени своих граждан, и такой тип торга значительно снижает цены на оригинальные лекарства в этих странах.
Таким образом, другие правительства торгуются с фармацевтическими компаниями от имени своих граждан, и такой тип торга значительно снижает цены на оригинальные лекарства в этих странах.
Единственным исключением является правительство США. Как крупнейший рынок лекарств в развитом мире, вы можете себе представить, что наше правительство находится в лучшем положении, чтобы торговаться от нашего имени.И хотя эта стратегия работает для всех других правительств, наше правительство этого не сделает. Законодательство США запрещает нашему правительству принимать активное участие в переговорах о ценах, взимаемых фармацевтическими компаниями.
Вместо этого мы используем менеджеров по льготам аптек, чтобы торговаться за нас, и, как я показал в предыдущих главах, PBM, как правило, на стороне фармацевтических компаний и фактически предпочитают более высокие цены на лекарства. И с практической точки зрения именно по этой причине мы платим больше (намного больше), чем кто-либо другой в мире, за лекарства, отпускаемые по рецепту. Вот такую «сделку» мы (точнее, наш Конгресс) заключили.
Вот такую «сделку» мы (точнее, наш Конгресс) заключили.
Тот факт, что наше правительство является единственным крупным правительством мира, которое отказывается вести переговоры с фармацевтическими компаниями, привело к довольно отчаянному движению в США. Большое количество людей и несколько политиков предложили реимпортировать лекарства из других, более мелких стран, которые удалось договориться о снижении цен на эти лекарства. Эта стратегия привела бы к снижению цен на лекарства для нас, но подумайте на минуту, насколько это нелепо?
Наше правительство отказывается вести переговоры напрямую с фармацевтическими компаниями, поэтому вместо этого мы будем использовать правительства других, более мелких стран для выполнения работы, которую мы могли бы сделать лучше и эффективнее, если бы нам позволили? Действительно? Это еще раз показывает, что наше собственное правительство изо всех сил старается сделать нашу систему здравоохранения не просто неэффективной, а откровенно сюрреалистичной.
Почему наше правительство намеренно отказалось от этой задачи? Часто называют две причины. Во-первых, есть аргумент, что правительство не должно вмешиваться, потому что у нас есть «свободный рынок» наркотиков. Американцы очень верят в нашу рыночную систему, но в данном случае наш «свободный рынок» не дает абсолютно никакой свободы при покупке рецептурных лекарств. Как мы уже говорили, вы не выбираете, какие лекарства вам прописывают; и люди не ходят по магазинам (часто не могут) и не сравнивают цены на лекарства известных марок.Другими словами, это свободный рынок без каких-либо признаков свободы (или рынка).
Что мы действительно получаем взамен?
Но наше обсуждение здесь в основном касается второго оправдания, которое часто приводится для отказа от всякого контроля над ценами на лекарства. Нам говорят, что высокие цены, которые американцы платят за лекарства, необходимы для получения денег, необходимых для лечения болезней. Мы долго думали, куда уходят деньги.
Вкратце, много маркетинга, много прибыли и «исследований», которые представляют собой комбинацию разработки новых лекарств, неоднократных попыток получить одобрение старых лекарств, больше маркетинга и корпоративных поглощений.Но даже если большая часть денег, которые мы платим, идет на маркетинг и прибыль, все же разумно спросить, добиваются ли фармацевтические компании результатов. Другими словами, разрабатывают ли они новые лекарства для лечения болезней? Вот куда мы пойдем сейчас.
Золотой век фармацевтической промышленности
Не так давно многие новые фармацевтические продукты оказали революционное влияние на здравоохранение. Между 1970 и серединой 1990-х годов десятки новых лекарств изменили то, как мы, врачи, практикуем медицину.Пептическая язва, хроническое болезненное состояние желудка, часто требующее хирургического вмешательства и длительной госпитализации, может быть вылечена без госпитализации с помощью новых классов антацидов, а затем вылечена новым курсом пероральных антибиотиков.
Новые препараты для лечения злокачественного высокого кровяного давления до того, как оно привело к инсультам, сердечной недостаточности и повреждению почек. Лекарства от болезней сердца и диабета продлевали жизнь пациентов на годы и даже десятилетия. Новые классы пероральных антибиотиков были более эффективны, чем лекарства, которые раньше можно было назначать только в больнице, и поэтому пациентов с тяжелыми инфекциями (пневмония, дивертикулит, тяжелый целлюлит) теперь можно было отправить домой с таблетками.
В 1993 году Барбара Брэдфилд стала первой женщиной, излечившейся от метастатического рака молочной железы. Лечением был Герцептин™, первый из другого нового класса лекарств, называемых моноклональными антителами. Вскоре было разработано несколько других моноклональных антител для таргетного лечения других видов рака и тяжелых ревматологических заболеваний.
Когда в 1995 году был представлен первый ингибитор протеазы, он оказался ключом к остановке эпидемии СПИДа, которая ускорялась более десяти лет. СПИД, чума, о которой до 1982 года не знали и почти гарантированная смертная казнь, ежегодно уносил жизни десятков тысяч человек в США в 1995 году. К 1999 году фармацевтические компании практически положили конец этим смертям.
СПИД, чума, о которой до 1982 года не знали и почти гарантированная смертная казнь, ежегодно уносил жизни десятков тысяч человек в США в 1995 году. К 1999 году фармацевтические компании практически положили конец этим смертям.
Это была эпоха, когда медицинские чудеса были настолько обычным явлением, что врачи стали воспринимать их как должное. Благодаря тому, что произвела фармацевтическая промышленность, многие заболевания, которые в прошлом требовали длительной госпитализации и/или серьезных операций, теперь можно лечить дома с помощью нескольких таблеток.Золотой век фармацевтической промышленности длился около двух десятилетий, и было создано множество новых лекарств, которые лечили ранее неизлечимое и лечили ранее неизлечимое.
Финансовый риск и конец эпохи
С тех пор прошло почти два десятилетия. Ингибиторы протеазы были одними из последних действительно революционных классов лекарств, появившихся в фармацевтической промышленности. С тех пор почти все новые лекарства были вариациями старых лекарств с небольшим улучшением (если даже таковым) или новыми показаниями. Мало новых классов лекарств, почти никаких медицинских чудес, ничего, что существенно изменило бы то, как мы практикуем медицину, не пришло из фармацевтической промышленности с конца девяностых.
Мало новых классов лекарств, почти никаких медицинских чудес, ничего, что существенно изменило бы то, как мы практикуем медицину, не пришло из фармацевтической промышленности с конца девяностых.
Так как же получилось, что индустрия, которая дала нам столько революционных чудодейственных лекарств, спасающих жизни в прошлые десятилетия, теперь сводится к продаже уловок и многократному повторному использованию старых идей?
«Золотой век фармацевтической промышленности» подходил к концу еще в 1990 году, когда фармацевтические компании начали уставать от новых идей.Новые идеи всегда дороги и рискованны. Даже самые блестяще звучащие идеи часто ни к чему не приводят при клинической проверке.
Эта усталость от инноваций стала настолько серьезной к началу 1990-х годов, что герцептин, моноклональное антитело, которое впервые вылечило метастатический рак молочной железы, почти даже не тестировалось. В своей книге «Император всех болезней» Сиддхартха Мукерджи описывает трудности, с которыми ученые Genentech убедили своих руководителей финансировать испытания Герцептина после того, как он уже был разработан в 1990 году:
«… но Genentech опасалась, что вложение денег в разработку еще одного неудачного лекарства нанесет ущерб финансам компании. Наказанный чужим опытом — «аллергией на рак», как описал это один исследователь Genentech, — Genentech прекратила финансирование большинства своих онкологических проектов». (стр. 418)
Наказанный чужим опытом — «аллергией на рак», как описал это один исследователь Genentech, — Genentech прекратила финансирование большинства своих онкологических проектов». (стр. 418)
Herceptin уже был разработан, но руководителей Genentech это не волновало. Проверять, работает ли это, было рискованно напрасной тратой денег, и эти руководители становились очень не склонными к риску. Руководители Genentech были не одиноки в своем неприятии риска. С 1995 по 1997 год руководители Novartis столь же упорно пытались убить Гливек — еще одно чудодейственное лекарство, подавляющее смертельную форму лейкемии на неопределенный срок, — потому что они опасались, что испытания, необходимые для очистки Гливека, обойдутся слишком дорого (стр. 436).
К счастью, и Гливек, и Герцептин получили необходимое финансирование и принесли миллиарды долларов прибыли фармацевтическим компаниям, пытавшимся их убить. Однако они были одними из последних новых идей, получивших финансирование от фармацевтических компаний. К тому времени, когда Гливек появился на рынке в 2000 году, дверь для новых фармацевтических исследований была в основном закрыта.
К тому времени, когда Гливек появился на рынке в 2000 году, дверь для новых фармацевтических исследований была в основном закрыта.
К 1990 году фармацевтическая промышленность знала, что у них уже есть много очень эффективных продуктов, которые приносили им много денег каждый год.У них были патенты, которые приносили миллиарды долларов в год и будут приносить еще много лет вперед. Они также знали, что, вероятно, смогут найти ряд новых применений для классов лекарств, которые у них уже были. Самый выгодный курс, который они видели в тот момент, состоял в том, чтобы просто двигаться по инерции; больше не вкладывать средства в новые фундаментальные исследования и просто продолжать продвигать то, что уже работало на них. Это именно то, что они сделали, и это сработало!
Прибыль, полученная фармацевтическими компаниями за последнее десятилетие, резко возросла, но они не выпустили никаких новых продуктов, которые хотя бы отдаленно были инновационными.Но эта стратегия может работать только некоторое время. Спустя два десятилетия после того, как они закрыли дверь для реальных инноваций, доходы от старых идей начинают иссякать.
Спустя два десятилетия после того, как они закрыли дверь для реальных инноваций, доходы от старых идей начинают иссякать.
Рисунок 4: (Из статьи по ссылке выше.) Новые лекарства, выпускаемые каждый год с 2001 года фармацевтическими компаниями, становятся все менее популярными.
Итак, мы в США продолжаем переплачивать за фирменные лекарства, отпускаемые по рецепту, но фармацевтическая промышленность почти не предоставила нам новых важных методов лечения за более чем 15 лет.Несколько неожиданным результатом этого является то, что общий доход от фармацевтической продукции с 2010 г. практически не изменился. Из приведенного выше графика видно, что общий доход тринадцати крупнейших фармацевтических компаний практически не увеличился с 2010 года. Фактически он немного снизился с 2011 года, несмотря на более чем 50-процентное увеличение стоимости фирменных рецептурных препаратов в США с 2012 года. Что изменилось? На рынок обрушился поток непатентованных лекарств. Поскольку рынок непатентованных лекарств действительно существует, мы платим за большинство непатентованных лекарств не больше, чем люди в других странах. В 2003 году большинство прописываемых лекарств все еще были запатентованы. Сегодня все наоборот. Эффект легко увидеть на следующем графике, который показывает резкое снижение доходов, когда срок действия патента, принадлежащего Bristol-Myers Squibb на Plavix, истек. Фармацевтические компании не брали на себя все эти потери патентов. Они ввели ряд мер, чтобы помочь компенсировать сумму, которую они теряют из-за потери патентной защиты: 1) Они очень упорно и всеми возможными способами боролись за отсрочку истечения срока действия эксклюзивных прав на наркотики, когда это было возможно. 2) В 2013 году фармацевтические компании добились от Верховного суда США разрешения им платить производителям непатентованных лекарств за отсрочку выпуска непатентованных эквивалентов лекарств на время после истечения срока действия патента на лекарство. 3) Фармацевтические компании ежегодно выплачивают огромные суммы денег поставщикам и управляющим аптеками (PBM) в виде скидок и возвратных платежей.Скидки и возвратные платежи, выплаченные 13 крупнейшими фармацевтическими компаниями, только в 2017 году составили 150 миллиардов долларов. 4) Они подняли цены на все свои лекарства, продаваемые в США.С. существенно в последние годы. В следующей таблице четко показана эта закономерность: В таблице 3 показаны средние (NADAC) цены, которые аптеки платят за 15 лекарств. Основной целью такого повышения цен является финансирование скидок, указанных в пункте 3. Другими словами, большая часть денег, потраченных на эти высокие цены на лекарства, идет не фармацевтическим компаниям, а скорее на оплату посредников (PBM и поставщиков), которые отвечают за выбор рецептурных препаратов, покрываемых вашей страховкой. Эти методы, которые фармацевтические компании используют для сокращения своих потерь, как правило, не дают новых терапевтических преимуществ — они просто восстанавливают свою способность требовать очень высоких цен (по крайней мере, в США). Начиная с 1970-х годов фармацевтическая промышленность производила невероятные лекарства от болезней так быстро, что, казалось, у них была фабрика чудес. Разрешив фармацевтическим компаниям брать за свои лекарства столько, сколько они хотят, у них будут инструменты и стимул продолжать создавать новые и более качественные лекарства. вопросы. Но теперь мы видим, что чудодейственные фабрики, похоже, были заколочены уже много-много лет — руководители отрасли, кажется, решили, что слишком рискованно держать их открытыми, когда у них уже было так много денег. Прошло много времени с тех пор, как мы видели много новых методов лечения. Мы продолжали присылать деньги, но в ответ получили в основном телевизионную рекламу, платных промоутеров врачей и симпатичных молодых фармацевтических представителей, которые тратят время вашего врача, пытаясь убедить его прописать дорогие запатентованные лекарства вместо дженериков, которые просто работают. Короче говоря, мы получили маркетинговую и корпоративную прибыль, которая по-прежнему остается одной из самых высоких в любой отрасли.«Исследования», которые мы закупали, часто сводились не к поиску лучших лекарств, а к поиску того, как заставить лекарства выглядеть лучше. Или расширить их патентную защиту по причинам, которые не делают их лучше. Конечно, некоторые законные исследования все еще проводятся, но они имеют гораздо меньшее влияние в отрасли, которая несколько десятилетий назад стала избегать риска. И как ни странно, из-за того, что они не выполнили свою часть сделки по предоставлению новых и инновационных методов лечения, сами фармацевтические компании начали страдать.У девяти из тринадцати компаний, финансовые отчеты которых я изучил, выручка за последние несколько лет не изменилась или снизилась. Эта тенденция, вероятно, сохранится и даже ухудшится в отрасли, которая продолжает жить прошлым. А что же остальные? Мы слепо влили триллионы долларов в отрасль, предполагая, что они продолжат превращать эти деньги в медицинские чудеса. Ниже резюмируются качественные результаты, полученные в результате подробного интервью, взаимодействия между поставщиком медицинских услуг и МРТ и обсуждения за круглым столом. Крупный фармацевтический рынок в основном управлялся рецептами врачей. Таким образом, успех фармацевтических компаний зависел от действенности и эффективности их МР. Категоризация врачей на основе их «истории» и того, как к ним обращаться, также была тем, чему обучали МР. Например, одна из известных транснациональных компаний классифицировала врачей (которых они называют клиентами) в зависимости от того, кто что ценит (описание согласно интервью MR): Тип режиссуры : Врачи, которые имеют сильные ценности и сохраняют свое достоинство.Они предпочитают только иметь информацию, связанную с наркотиками, и не говорить ни о чем другом, и не заинтересованы в других выгодах. Думающий тип : Спокойные по своей природе, им нужно время, чтобы подумать, прежде чем принять какое-либо решение. Они просят ссылки/доказательства по рекламным бюллетеням. Они обычно назначают лекарства только тогда, когда они убеждены. Аффилиативный тип : Эти врачи приветствуют MR, им нравится их слушать, а также высказывать свое мнение. «С такими врачами работать проще», — сказал MR. Выражение типа : Эти врачи часто доминируют в беседе при общении с МР, почти не слушают внимательно, что говорят МР и обычно не назначают предлагаемые продукты. «Они высказывают свои требования совершенно откровенно». Это только один пример того, как MR были ориентированы на то, чтобы иметь дело со своими клиентами в реальной жизни.Эта ориентация МР на удовлетворение своих клиентов использовалась для выполнения требований врачей и в конечном итоге убедила их выписывать рецепты в качестве ответной услуги (политика «отдавать и брать», по словам одного МР). Врачей поощряли к общению с врачами на личном уровне, что также ценится врачами. Регулярные визиты к врачам были одним из стратегических способов поддержания этих отношений, и иногда в этих отношениях происходило «размывание профессиональных границ».Для иллюстрации: «Иногда за одно посещение врач убеждается…иногда требуется четыре-пять посещений…если перерыв между двумя визитами большой, то врач забывает о препарате, поэтому приходится часто приезжать, чтобы выделить нашу продукцию… — Один МР Комментарий врача-специалиста по тому же вопросу поддержал требование МР: «Я автоматически создаю мягкий уголок для MR, которые регулярно посещают меня.Потом пробую прописать 2-3 его продукта. Я думаю, что большинство врачей думают так же».– Врач-специалист Не все врачи посещали МРТ с одинаковой периодичностью. МР всегда отдавали предпочтение врачам с высокой загруженностью пациентами. Согласно MR, они классифицировали врачей на основе их «потенциала», определяемого количеством пациентов, посещающих врача в любой день, что зависит от рецептов, которые могут быть выписаны.Кроме загруженности пациентов важным фактором, определяющим частоту визитов М.Р., также была «лояльность» врачей к компании (т.е. склонность выписывать препараты конкретной фирмы). В часы пик заходили врачи, чтобы обменяться приветствиями с врачами в качестве эффективного напоминания о бренде, что вскоре могло привести к выписке рецепта: «В учреждениях врачи начинают выписывать лекарства с утра, но нам разрешают посещать их после 11 часов, когда у врачей почти закончился рабочий день.Поэтому, хотя я не могу навестить его, я каждый день хожу к нему и передаю ему салям, чтобы он помнил мои клейма» — An MR Наши наблюдения показали, что МР разных компаний предпочитали посещать врачей рано утром: «…если мы сможем посещать врачей рано утром, у него будет больше возможностей прописать нашу марку, которая более выгодна для нас» — An MR Результаты также показывают, что МР предпочитают государственные учреждения частным, поскольку врачи в первых давали им больше времени и позволяли посещать их, пока врачи посещали пациентов.Чем выше загруженность пациентов в этих учреждениях, тем выше была и вероятность получения доли рецепта. «Работать в государственных медицинских учреждениях намного проще… мы можем зайти туда в любое время и работать, даже когда врач обслуживает пациентов. А вот в частных больницах и клиниках приходится строго следовать их графику… ограничений много! Обычно в эти места приезжают богатые люди, и они тоже не хотят нас видеть в больницах…» – An MR Вторую половину рабочего дня МР проводили в кабинетах частнопрактикующих врачей.Все МР в глубинных интервью сказали, что им нравится общаться с врачами во время их частной практики и развивать отношения. Один MR сказал, «В плане посещения нам предпочтительнее частная палата. Потому что в учреждениях иногда нам приходится посещать многих врачей одновременно, и мы должны следить за тем, чтобы все врачи получили одинаковое количество образцов или подарков. Но в частной практике врачи сидят в отдельной комнате… так что с ними легко иметь дело, и мы можем мотивировать их выписывать наши лекарства.— МР Однако, как и в большинстве случаев, отношения между MR и врачом являются отношениями «взаимных уступок», и они нуждаются в постоянном развитии. «Цель» очень важна для МР; у каждой фармацевтической компании была индивидуальная цель (ежемесячная, ежеквартальная, годовая) для своих MR. Они получали прибавку или стимул в зависимости от достигнутых целей, которые варьировались от компании к компании.Таким образом, в конце каждого квартала МР вынуждены выполнять эти задачи любыми способами. По сообщениям, врачи, то ли из сочувствия, то ли из раздражения, в конечном итоге прописали некоторые лекарства под постоянным давлением со стороны МР, особенно в конце кварталов. Для иллюстрации: «Г-н всегда беспокоится о достижении своих целей… есть несколько Г-дов, с которыми у меня хорошие отношения. На днях один из этих мальчиков подошел ко мне и попросил: «Сэр, мне нужна ваша помощь в выполнении моей задачи.Если я успею на этот раз, я смогу поехать в Китай», – врач . В то время как врачи, поддавшиеся на уговоры МР, были обычным явлением, есть исключения, когда непоколебимая решимость врача посылала другое сообщение представителям: «…были случаи, когда MR появлялись с незаполненными чеками.Я сказал им: «Не балуйте так врачей. Они тоже люди и тоже могут поддаться искушению, так что не делайте этого с нами». – Врач Фармацевтические компании приняли несколько стратегий для достижения всех «всеобъемлющих» целей. Одним из них был мониторинг назначений старших профессоров и очень успешных частнопрактикующих врачей. По словам MR, они всегда отслеживали врачей и предоставляли самую свежую информацию для поддержания базы данных компаний в актуальном состоянии: «Когда мы посещаем врача, мы проверяем, действительно ли это сделал врач, который согласился выписать наш продукт,… иногда наша компания покупает данные обследования рецептов у других компаний.Обычно мы проверяем рецепт у пациента… если наш продукт не прописан, мы продолжаем напоминать им посредством частых посещений…» – An MR Этот мониторинг рецептов, проводимый MR, также служил и другим целям: «… наблюдая за рецептами, мы можем выявить привычки врача к выписыванию рецептов. Во-первых, мы можем определить, какие лекарства обычно нравятся врачу, чтобы продвигать их для увеличения продаж.Мало того, если у врача есть какие-то особые отношения с компанией, мы можем определить это, увидев большинство продуктов этой компании в рецепте, и можем сформировать нашу стратегию, чтобы [заставить их изменить свои предпочтения]». — МР Исследование также показало, что ведущие фармацевтические компании покупают базу данных рецептов у третьих лиц, таких как Intercontinental Marketing Services (IMS), по высокой цене. Из этой базы данных рецептов они получают региональный список предпочтительных брендов каждого врача, который помогает настраивать стратегии, соответствующие схемам назначения. Наиболее часто используемые рекламные материалы, предлагаемые фармацевтическими компаниями, — это литература о лекарствах, журналы, блокноты, ручки и образцы лекарств. Но у фармацевтических компаний усилилась тенденция дарить врачам практически все: «Фармацевтические компании предоставляют все, кроме каача-базара.Даже на прошлый Курбан-байрам давали ароматный рис (полао эр чал), сахар, вермишель (семай) и т. д. Так что трудно сказать, чего они нам не предлагают». – Врач Подарки включали предметы как для профессионального, так и для личного пользования. Профессиональные услуги включают спонсорство посещения медицинских конференций и семинаров; медицинское оборудование и книги; предметы для зоны ожидания врачей (стулья, фильтр для воды, телевизор и т. д.), именные визитки, блокноты и папки с рецептами; и наличными за продукты по рецепту.Предметы личного пользования включают стоимость авиабилетов и проживания в гостинице для увеселительных поездок с семьей и друзьями; украшение для дома; эксклюзивные подарки, такие как дом, квартира, автомобиль и т. д. Другие подарки включают в себя продукты питания, мобильные карты пополнения счета, интернет-модем, наличные деньги или спонсорство для личных программ, таких как свадьба, день рождения, церемония имянаречения ( Akika ) и т. д. фармацевтические компании использовали два подхода к предложению подарков. В рамках проактивного подхода врачам ежемесячно вручались недорогие подарки вместе с бесплатными образцами лекарств во время регулярных рекламных визитов МР.На этих подарках обычно были написаны торговые марки, чтобы они служили напоминанием для врачей. Другой подход заключался в том, чтобы предлагать поощрения, основанные на требованиях врачей, то есть «все, что он / она хочет в качестве подарков». Эта культура побуждения распространилась даже на членов семей врачей, особенно на более молодых членов. Как показано двумя MR: «Иногда врачи хотят взять с собой членов семьи в зарубежную поездку, и мы их тоже спонсируем.Помимо спонсирования семинаров и мастер-классов, мы также дарим врачам различную электронику и предметы домашнего обихода. Мы даем все, что они просят…» — An MR «Некоторые врачи требуют компьютер, телевизор, холодильник, кондиционер, мобильный телефон, ноутбук и т. д. Счет за мобильную связь, счет за электричество, счет за обслуживающего персонала, зарплату водителя, бумажный счет и т. д. — на все, что у них есть договор с компаниями…» — Ан МР Это также подтверждает врач, который напомнил: «Авиабилеты Дакка-Сингапур, автомобили, дома и даже семейные или бытовые вещи — это то, что получают врачи.… Доктор Икс купил участок в Дханмонди. Таким образом многие люди становятся владельцами автомобилей и домов. В наши дни это даже можно назвать соревнованием [кто больше получит подарков].» – Врач Изменение характера рекламной деятельности повлияло на рецептурные привычки врачей, что было признано врачом: «Рекламная деятельность влияет на нашу привычку выписывать рецепты.Я думаю, что врачи это понимают, но все же делают. Когда врач принимает подарок от компании, он знает, почему ему предлагают то, что… возникает определенное обязательство перед этой компанией…» Но есть и исключения. Профессор частного медицинского колледжа объяснил: «…врачи разочарованы этой коррумпированной системой и тем, как она вынуждает их становиться ее частью. Исследование показывает, что врачи, как правило, не заинтересованы в получении литературы о продуктах от МР, их больше интересуют образцы лекарств, которые МР приносят в качестве рекламных материалов. Распространены жалобы на то, что значительная часть образцов лекарств для врачей в конечном итоге попадает в розничные аптеки. Вот две цитаты из MRs: «…мы обычно кладем образцы на стол (врача)…нехорошо такие продавать.Но мы не можем опрашивать врачей по этому поводу, и компания не предпринимает никаких действий в связи с этим». – МР «Фармацевтическое продвижение дошло до стадии подкупа. Раньше врачам давали образцы лекарств для бедных пациентов. На упаковках лекарств было написано «Не для продажи», и врачи раздавали его своим пациентам. Но сегодня врачи продают лекарства… они сделали свою профессию бизнесом».– МР МР крупных и средних компаний в первую очередь нацелены на врачей для продвижения своей продукции, в то время как МР небольших компаний обычно нацелены на сельских врачей и им подобных для продажи своей продукции. МР единогласно согласились с тем, что они тратили больше времени на подробные консультации с сельскими врачами, а не с врачами MBBS, потому что сельские врачи были менее осведомлены о наркотиках и с большим энтузиазмом относились к посещениям МР.Сельские врачи также выражали заинтересованность в поддержании дружеских отношений с МР и часто покупали лекарства только у МР, которые были с ними «друзьями». МР не были осведомлены о существующем кодексе практики продвижения и маркетинга лекарств. Многие врачи также упомянули, что не знали о коде: «Я не очень разбираюсь в CPMP.Мне непонятно, какие практики считаются неэтичными в нашей стране. Об этом необходимо четко сообщить врачам, а также фармацевтическим компаниям. Затем Департамент по контролю за лекарственными средствами должен играть активную роль в предотвращении этих неэтичных действий. Я не думаю, что они играют какую-либо роль в этом отношении в настоящее время». – Врач MR считали «этичным врачом» человека, лояльного к одной конкретной компании, а «неэтичного врача» — человека, заключившего контракты с несколькими компаниями. По мнению руководителей фармацевтических компаний, Кодекс является добровольным. В своих интересах они стараются его соблюдать. Они сказали, что получили предварительное разрешение от властей (DGDA) на литературу (включая другие рекламные материалы), прежде чем представить ее врачам. MR используются только для детализации литературы врачам. Они утверждали, что врачи слишком заняты, чтобы самостоятельно просматривать литературу, и большая часть литературы попала в мусорное ведро.Они утверждали, что компании не ставят перед MR необоснованные цели, поскольку это заставит их прибегнуть к недобросовестным средствам. Высшее руководство фармацевтических компаний также утверждало, что недостаточные возможности DGDA (как технические, так и человеческие ресурсы) для мониторинга и регулирования рынка являются причиной неэтичных методов продвижения. Однако, поскольку рынок очень конкурентный, они подчеркнули необходимость саморегулирования, которое, по их мнению, осуществляется в интересах отрасли.Руководители также указали, что незарегистрированные/нерегулируемые торговые точки по продаже наркотиков (аптеки) являются местами, где свирепствует неэтичная рекламная практика, и на них следует обратить внимание, чтобы положить конец такой практике. Они также подтвердили необходимость официального списка безрецептурных препаратов для проверки неэтичных действий неофициальных поставщиков медицинских услуг. Вас может удивить, насколько большую роль играют контроль и регулирование температуры в вашей жизни.В конце концов, вы хотите, чтобы ваши продукты были свежими, чтобы ваши цветы цвели, а шоколад таял только во рту, верно? Чтобы поддерживать стабильную температуру, эти типы продуктов требуют особого обращения и хранения на протяжении всего процесса. Стандартные отраслевые правила и необходимая документация в значительной степени усложняют стандартные процедуры доставки. Как только вы добавите все предметы, требующие температурной защиты, вы получите целый контрольный список правил, которым необходимо соответствовать. Именно поэтому материалы с фазовым переходом так важны. Некоторые лекарства, подвергающиеся воздействию экстремальных температур, могут стать неэффективными или даже вредными, по этой причине PCM являются важным решением, которое следует учитывать в мире цепочки поставок фармацевтической продукции. И важность своевременной и правильной доставки всех лекарств и других лекарств их получателям действительно нельзя недооценивать. Важно знать, какие продукты являются скоропортящимися, потому что, очевидно, не все, что отправляется, требует строгого температурного режима.Международная ассоциация воздушного транспорта (IATA) заявляет, что груз считается скоропортящимся, если его содержимое со временем портится под воздействием неблагоприятных факторов окружающей среды. Это описание включает фармацевтические препараты. Важно, чтобы в процессе логистики выделялись ресурсы для установления, поддержания и улучшения контроля температуры. Температура большинства фармацевтических товаров остается в пределах 2-8 градусов по Цельсию (36-46 градусов по Фаренгейту), но есть расширения, когда на складах используется температура -20 градусов по Цельсию для поддержания продуктов, соответствующих этой температуре. Существует определенный уровень квалификации и контроля, который необходимо соблюдать для обеспечения надлежащего контроля температуры фармацевтических товаров Внешние факторы играют роль в потребностях в доставке и зонах контроля температуры.Они варьируются в зависимости от времени года и климата, в который отправляются товары. Производителям необходимо доставлять большие объемы материалов на большие расстояния, так как во всем мире растет спрос на новые лекарства. Эти товары часто являются более ценными, в больших количествах или более чувствительными к температуре, чем в прошлом. PCM имеют решающее значение для цепочки поставок фармацевтической продукции, поскольку они могут дольше сохранять продукты в стабилизированном температурном диапазоне. Действительно, при транспортировке и хранении фармацевтических препаратов важно поддерживать постоянную температуру, независимо от внешних факторов. Часто основной проблемой при температуре от 2 до 8°C является то, что продукты должны храниться при очень низких температурах, но не при замерзании.

Рисунок 6: Компания Novartis потеряла свой патент на Диован в 2012 году, и, как вы можете видеть, это стоило ей около 5 миллиардов долларов в год упущенной выгоды. Прибыль без инноваций
 Этот процесс называется «вечнозеленым» патентом. Например, они могут подать заявку на новое показание для старого лекарства непосредственно перед истечением срока действия его патента.Они могут изменить систему доставки, скажем, на ингалятор. Они могут немного изменить рекомендуемые дозы препарата — у них есть много уловок для сохранения эксклюзивности, и эти уловки часто могут отсрочить конкуренцию дженериков на несколько лет.
Этот процесс называется «вечнозеленым» патентом. Например, они могут подать заявку на новое показание для старого лекарства непосредственно перед истечением срока действия его патента.Они могут изменить систему доставки, скажем, на ингалятор. Они могут немного изменить рекомендуемые дозы препарата — у них есть много уловок для сохранения эксклюзивности, и эти уловки часто могут отсрочить конкуренцию дженериков на несколько лет. Это более чем в два раза больше, чем эти компании заплатили в виде скидок и возвратных платежей в 2011 году. Эти финансовые стимулы побуждают PBM одобрять более дорогие лекарства при определении покрытия рецептурных препаратов для своих страхователей. Вместо того, чтобы пытаться сдержать стоимость отпускаемых по рецепту лекарств, PBM поощряется покрывать лекарства, которые дают более высокие скидки.
Это более чем в два раза больше, чем эти компании заплатили в виде скидок и возвратных платежей в 2011 году. Эти финансовые стимулы побуждают PBM одобрять более дорогие лекарства при определении покрытия рецептурных препаратов для своих страхователей. Вместо того, чтобы пытаться сдержать стоимость отпускаемых по рецепту лекарств, PBM поощряется покрывать лекарства, которые дают более высокие скидки. Лекарства и дозы Индикация октябрь 2012 г. Цена Июль 2018 Цена Повышение цены Абилифай 20 мг Депрессия 26,35 $ за таблетку 40,40 $ за таблетку 54% Advair 250/50 Астма 3 доллара.  97 на вдох
97 на вдох $6,28 за вдох 58% Беникар 40 мг Артериальное давление 4,26 доллара за таблетку $9,35 за таблетку 119% Байетта 10 мкг Диабет $128,58 за дозу-ручка $283,34 за дозу-ручку 120% Сиалис 20 мг Антиквариат
Секс в ванне $23,64 за таблетку 64 доллара.05 за таблетку 171% Крестор 20 мг Холестерин $4,99 за таблетку $8,35 за таблетку 67% Диован 160 мг Артериальное давление $3,43 за таблетку 7,64 $ за таблетку 123% Эффективность 10 мг Болезнь сердца $6,80 за таблетку $14,68 за таблетку 116% Геодон 60 мг Психоз 9 долларов.  85 за капсулу
85 за капсулу $24,67 за капсулу 150% Гливек 400 мг Лейкемия $189,91 за таблетку $328,10 за таблетку 73% Янувия 50 мг Диабет $7,30 за таблетку $13,75 за таблетку 88% Лирика 50 мг Боль 3 доллара США за капсулу 7,43 $ за капсулу 148% Пристик ER 50 мг Депрессия 4 доллара.84 за таблетку $12,18 за таблетку 152% Виторин 10/40 Холестерин 4,70 доллара за таблетку $10,92 за таблетку 132% Ксарелто 20 мг Мерцательная аритмия $7,59 за таблетку $13,44 за таблетку 77%  Он показывает среднюю стоимость этих лекарств в октябре 2012 года по сравнению со средней стоимостью тех же лекарств в июле 2018 года.Всего за 6 лет большинство перечисленных лекарств подорожали в среднем более чем на 100%. Это повышение цен продолжалось для каждого из этих лекарств, несмотря на то, что 9 из этих 15 лекарств потеряли свои патенты в последние годы.
Он показывает среднюю стоимость этих лекарств в октябре 2012 года по сравнению со средней стоимостью тех же лекарств в июле 2018 года.Всего за 6 лет большинство перечисленных лекарств подорожали в среднем более чем на 100%. Это повышение цен продолжалось для каждого из этих лекарств, несмотря на то, что 9 из этих 15 лекарств потеряли свои патенты в последние годы. Заключение: невыполненное обещание отрасли в упадке
 Многие ужасные болезни прошли путь от длительного мучения в больнице до быстрого излечения в домашних условиях.Тогда цены были ниже, экономика быстро росла, и мало кто будет возражать против того, чтобы продолжать кормить этого золотого гуся.
Многие ужасные болезни прошли путь от длительного мучения в больнице до быстрого излечения в домашних условиях.Тогда цены были ниже, экономика быстро росла, и мало кто будет возражать против того, чтобы продолжать кормить этого золотого гуся. также.
также. Совершенно очевидно, что почти два десятилетия назад промышленность решила, что лучше оставить себе большую часть этих денег, чем продолжать революционизировать здравоохранение.Поскольку фармацевтические компании мало что сделали для выполнения своей части этой сделки, не пора ли нам перестать уступать их требованиям? Все остальные страны мира придумали их много лет назад. Когда мы будем готовы открыть глаза и начать делать то же самое?
Совершенно очевидно, что почти два десятилетия назад промышленность решила, что лучше оставить себе большую часть этих денег, чем продолжать революционизировать здравоохранение.Поскольку фармацевтические компании мало что сделали для выполнения своей части этой сделки, не пора ли нам перестать уступать их требованиям? Все остальные страны мира придумали их много лет назад. Когда мы будем готовы открыть глаза и начать делать то же самое? Качественный анализ продвижения фармацевтической продукции в Бангладеш: насколько этичны методы? | BMC Medical Ethics
Медицинские представители (MR): стратегическая связь между фармацевтическими компаниями и врачами
 В основном это были выпускники естественных наук, набранные на конкурсной основе. После найма они прошли структурированную программу обучения, которая помимо технических подробностей о соответствующих продуктах также включала в себя то, как наблюдать и оценивать личности и предпочтения врачей.Таким образом, они собирали личную информацию врачей, такую как сведения о семье и образе жизни, хобби, личные интересы и т. д., которые МР называют «сбором анамнеза».
В основном это были выпускники естественных наук, набранные на конкурсной основе. После найма они прошли структурированную программу обучения, которая помимо технических подробностей о соответствующих продуктах также включала в себя то, как наблюдать и оценивать личности и предпочтения врачей.Таким образом, они собирали личную информацию врачей, такую как сведения о семье и образе жизни, хобби, личные интересы и т. д., которые МР называют «сбором анамнеза».

Динамика посещений МРТ: стирание профессиональных границ
.
Достижение целей: мониторинг назначений
.
Подарки, подарки, подарки: от блокнота и ручки, до заграничной поездки по работе или для удовольствия!
Сегментация рынка
Осведомленность о Кодексе практики фармацевтического маркетинга (CPMP)
.
Взгляд руководителей фармацевтических компаний
Life Science & Med Device (Insight)
Ch. 3: Фармацевтика и материалы с фазовым переходом
Как фармацевтическая промышленность использует PCM
. Склад, холодильная камера и прицеп должны пройти квалификацию на основе тестов, чтобы выявить, есть ли какие-либо области, которые
подвержены воздействию внешних температурных диапазонов. Тест проводится, когда склад пуст, и снова, когда он заполнен продуктами, для подтверждения температурных квалификаций.
ФАРМАЦЕВТИЧЕСКОЕ ОХЛАЖДЕНИЕ С ФАЗОВЫМ МАТЕРИАЛОМ



 Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Италии.
Такие рекламодатели могут осуществлять рекламу только для целевой аудитории в Италии.


 Посоветуйтесь с врачом».
Посоветуйтесь с врачом».






