Производство спирт этиловый – Производство этилового спирта
Оборудование + Технология изготовления 2019

Спиртовая промышленность занимается производством этилового спирта из пищевого или не пищевого сырья.
Этиловый спирт, который производится из пищевых сырья, далее идет в производство алкогольных напитков, на изготовление автомобильного топлива и нужд радиоэлетроники.
В качестве сырья для получения пищевого спирта используется картофель, зерновые, корнеплоды, сахарная патока или меласса, плодово-ягодное сырье и виноградные продукты – материал, который богат углеводами.
В качестве сырья для получения технического спирта используются отходы деревоперерабатывающей или нефтеперерабатывающей отраслей. Последнее время все больше внимание уделяется использованию растительной биомассы в качестве исходного материала для получения спирта. Их подвергают кислотному гидролизу. Полученный продукт содержит большое количество вредных примесей и поэтому в пищевой промышленности технический спирт категорически запрещен к использованию.
Оборудование для производства спирта
Оборудование для производства состоит из трех отделов – бражной колонны, эпюрационной колонны и ректификационной колонны.
Основная линия производства состоит из следующего оборудования: нория, бункер надвесовой, весы дозатор, бункер подвесовой, шнековый дозатор, дробилка, смесители, чанок замеса, краны трехходовые, краны шаровые, вентиля, задвижки, трубопроводы ,насос центробежный, контактная головка, варочный аппарат, (низкотемпературное разваривание), насосы для перекачки сусла, насос дозатор, теплообменник сусла, краны трехходовые и шаровые с обратными клапанами, бродильные аппараты, дрожжанки, ловушка и маточник, насос для подачи бражки и дрожжевой, мерник серной кислоты, спиртоловушку, емкость промывных вод, подогреватель бражки, водяная секция подогревателя, конденсаторы, сепаратор, бардорегулятор, спиртоловушка, дефлегматор, конденсатор и холодильник, пеноловушка, вакуумпрерыватель, гидрозатвор, маслоотделитель, сборник сивушного масла, фонарь спиртовой.
Технология производства спирта + видео как делают
«Технология производства, в целом, состоит из трех последовательностей:
- Очистки сырья от различных примесей, подготовка солода или культуры специально подобранных плесневых грибов;
- Разваривания крахмалосодержащего сырья, процесс осахаривания крахмала, далее идет сбраживание осахаренного продукта и перегонка полученной бражки – это будет сырой спирт.
- И затем сырой спирт подвергается ректификации.
Ректификация – это очистка полученного первоначального сырого спирта. Содержание примесей в сыром спирте настолько высоко, что непосредственное его использование в пищевой промышленности недопустимо.
Вредные примеси, которые образуются в процессе производства этилового спирта – метиловый спирт — как продукт распада пектина, содержащегося в растительных тканях; сивушные масла – или смесь высших спиртов – их провоцирует изначально гидролиз белка, и последующее дезаминирование аминокислот, плюс некоторые промежуточные продукты спиртового брожения также могут провоцировать появление сивушных масел; сложные эфиры, фурфурол. Сложные эфиры также появляются в результате процессов брожения, когда этиловый спирт взаимодействует с сивушными маслами и органическими кислотами.
Все примеси классифицируются как промежуточные, хвостовые или головные.
Во время очистки используется разница кипения спиртов и эфиров. У этилового спирта температура кипения выше по сравнению с головными примесями – уксусным альдегидом, сложными эфирами. И в то же время у этилового спирта температура кипения ниже по сравнению с хвостовыми примесями – сивушными маслами и метиловым спиртом. Самую большую сложность представляют в процессе очистки именно промежуточные примеси.
Во время ректификации готовый продукт насыщается спиртом с восьмидесяти восьми процентов до 90-90,5%.
Кроме сивушных масел, в процессе производства этилового спирта получают еще барду и углекислый газ.
Сивушные масла перегоняют и получают высшие спирты, которые в дальнейшем будут использоваться в различных отраслях промышленности – медицинской, парфюмерной или лакокрасочной.
Углекислый газ очищается и сжижается или идет на производство сухого льда.
Послеспиртовая барда просушивается и идет на производство кормовых дрожжей, которые применяются в животноводстве в качестве кормовой добавки.
Классификация первоначального спирта-сырца идет в зависимости от содержания в нем посторонних примесей: Альфа, Люкс, Экстра, базис, высшей очистки, 1 сорт.
Технология гидролиза получила распространение по причине сокращения ископаемого органического сырья. Гидролиз позволяет получать спирт из растительной биомассы, которая является возобновляемым биоресурсом. Кроме гидролизного спирта выделяют еще и синтетический спирт. Его производство основывается на смешивании газа этана с водой под высоким давлением. При этом вода и газ не очищаются, в результате реакции образовываются побочные продукты, которые токсичны для организма человека.
Для того чтобы выделить технический спирт и сделать его непригодным для использования в пищевых целях, в его состав добавляют ингредиенты, которые изменяют его вкус и цвет с запахом – цвет чаще получается с синефиолетовым оттенком. К добавкам, которые используются в качестве денатурата, предъявляются определенные требования – низкая токсичность, чтобы снизить риск отравления и смертельного исхода, специфичность вкуса и цвета, стойкость в качестве маркера, чтобы его было сложно отделить от этилового спирта с применением современных технологических процессов и оборудования.
Видео как делают на водочном производстве:
На сегодняшний день большинство гидролизных заводов на территории России входят в состав министерства медицинской и микробиологической промышленности.
moybiznes.org
Технология производства и получения этилового спирта (более 40%)
Внимание: данная статья носит ознакомительный характер. Всегда помните о вреде алкоголя.
Производство спирта состоит из нескольких этапов, выполнять которые нужно обязательно в последовательном порядке. Для получения чистого этилового спирта (более 40%), необходима перегонка и очистка исходного сырья. Основным преимуществом данной технологии является отсутствие значительных инвестиций на приобретение оборудования и многообразия исходного сырья.
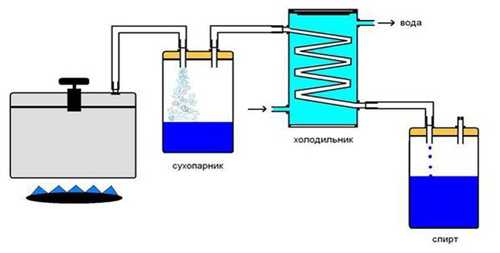
Технология получения спирта включает в себя следующие этапы:
- подготовка сырья;
- разваривание зерна водой;
- охлаждение и осахаривание;
- сбраживание;
- отгонка спирта;
- ректификация.
В качестве зерна могут быть использованы ячмень, рожь, овес и другие зерновые. Не допускается затхлый и плесенный запахи. Строгой регламентации зерна, которое будет подвергнуто развариванию, не существует. Рекомендуется выбирать сырье с влажностью до 17% и небольшой засоренностью. Зерно очищают от пыли, земли, мелких камней, семян сорных растений и других посторонних примесей.

Мелкие металлические примеси подлежат удалению посредством магнитных сепараторов.

Разваривание зерна происходит с целью разрушения их клеточных стенок. В результате этого крахмал высвобождается и переходит в растворимую форму. В таком состоянии он намного легче осахаривается ферментами. Зерно обрабатывается паром при избыточном давлении 500 кПа. Когда разваренная масса выходит из
Подобное увеличение в объеме разрывает клеточные стенки и превращает зерно в однородную массу. На сегодняшний день разваривание крахмалосодержащего сырья производят одним из трех способов: периодическим, полунепрерывным или непрерывным. Наибольшую популярность получил непрерывный метод. Температура разваривания составляет 172°С, а продолжительность варки около 4 минут. Для получения более качественного результата исходное сырье рекомендуется измельчать.
Сам процесс разваривания включает операции:
- Строгая дозировка зерна и воды;
- Нагрев замеса до температуры варения;
- Выдержка массы при заданной температуре.
Измельченное зерно следует смешать с водой в количестве 3 литра на 1 кг. зерна. Зерновой замес нагревается паром (75°С) и подается насосом в контактное отверстие установки. Именно здесь происходит мгновенный нагрев кашицы до температуры 100°С. После этого подогретый замес помещается в варочный аппарат.
В процессе осахаривания в охлажденную массу добавляют солодовое молоко для расщепления крахмала. Активное химическое взаимодействие приводит к тому, что продукт становится абсолютно пригодным для дальнейшего процесса сбраживания. В результате получается сусло, которое содержит 18% сухого сахара с кислотностью 0,3 град. Когда из массы делается проба на йод, то окрас сусла должен оставаться неизменным.
Сбраживание сусла начинается при введении в осахаренную массу производственных дрожжей. Мальтоза расщепляется до глюкозы, которая в свою очередь сбраживается в спирт и диоксид углерода. Также начинают образовываться вторичные продукты брожения (эфирные кислоты и т.д.). Данный процесс должен проходить в закрытой бродильной установке, которая предотвратит потери спирта и выделение диоксида углерода в производственный цех.

Выделяющийся в процессе брожения диоксид углерода и пары спирта из бродильной установки поступают в специальные отсеки, где происходит отделение водно-спиртовой жидкости и диоксида углерода. Содержание этилового спирта в бражке должно равняться до 9,5 об.%.
Далее приступают к отгонке спирта из бражки и его ректификации. Спирт начинает выделяться из бражки в результате кипения при разных температурах. Сам механизм перегонки основан на следующей закономерности: спирту и воде свойственны разные температуры кипения (вода — 100 градусов, спирт — 78°С). Выделенный пар начинает конденсироваться и собираться в отдельную емкость. Очистку спирта от примесей производят на ректификационной установке.

При подогревании браги до 90°С пары начинают подниматься по колоне в конденсатор, где они полностью охлаждаются. После этого чистый спирт поступает в специализированную колонну, имея крепость 50-55 об.%
Поделитесь статьей с друзьями:
vproizvodstvo.ru
Производство этилового спирта из непищевого сырья
Производство спирта из картофеля, зерна, мелассы, сахарной свеклы требует расхода больших количеств этих ценных видов сырья. Замена такого сырья более дешевым является одним из источников экономии пищевых продуктов и снижения себестоимости спирта. Поэтому в последнее время значительно увеличилось производство технического этилового спирта из непищевого сырья: древесины, сульфитных щелоков и синтетическим путем из этиленсодержащих газов.
Производство спирта из древесины
Гидролизная промышленность выпускает из растительных отходов, содержащих целлюлозу, в частности из древесных отходов, ряд продуктов: этиловый спирт, кормовые дрожжи, глюкозу и др.
На гидролизных заводах целлюлозу гидролизуют минеральными кислотами до глюкозы, которая используется для сбраживания в спирт, выращивания дрожжей и выпуска в кристаллическом виде. Существуют гидролизные заводы различного профиля: гидролизно-спиртовые, гидролизно-дрожжевые, гидролизно-глюкозные. Гидролизная промышленность имеет большое народнохозяйственное значение; оно обусловлено тем, что из малоценных растительных отходов получают ценные продукты. В частности, из 1 т абсолютно сухой хвойной древесины получают 170-200 л этилового спирта, для выработки которого потребовалось бы 0,7 т зерна или 2 т картофеля.
Гидролизная промышленность комплексно перерабатывает древесину, в результате чего на гидролизно-спиртовых заводах получают, кроме этилового спирта, и другие ценные продукты: фурфурол, лигнин, жидкую углекислоту, кормовые дрожжи.
Сырье гидролизного производства
Сырьем гидролизного производства служит древесина в виде различных отходов лесной и деревообрабатывающей промышленности: опилки, щепа, стружка и др. Влажность древесины колеблется от 40 до 60%. Опилки, перерабатываемые гидролизными заводами, обычно имеют влажность 40- 48%. В состав сухих веществ древесины входят целлюлоза, гемицеллюлозы, лигнин и органические кислоты.
Гемицеллюлозы древесины состоят из гексозанов: маннана, галактане и пентозанов: ксилана, арабана и их метилированных производных. Лигнин представляет собой сложное вещество ароматического ряда, химический состав и строение его еще не установлены.
Химический состав абсолютно сухой древесины приведен в таблице 1.
Таблица 1 — Химический состав абсолютно сухой древесиныКроме древесины, в качестве сырья для гидролизной промышленности применяются и растительные отходы сельского хозяйства: подсолнечная лузга, кукурузная кочерыжка, хлопковая шелуха, солома зерновых злаков.
Химический состав растительных отходов сельского хозяйства представлен в таблице 2.
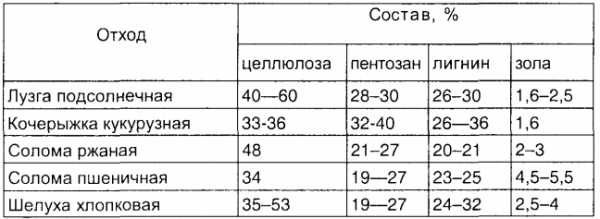 Таблица 2 — Химический состав растительных отходов сельского хозяйства
Таблица 2 — Химический состав растительных отходов сельского хозяйстваТехнологическая схема комплексной переработки древесины
Технологическая схема комплексной переработки древесины состоит из следующих стадий: гидролиз древесины, нейтрализация и очистка гидролизата; сбраживание гидролизного сусла, перегонка гидролизной бражки.
Измельченную древесину подвергают гидролизу разбавленной серной кислотой при нагревании под давлением. При гидролизе гемицеллюлозы и целлюлоза разлагаются. Гемицеллюлозы превращаются в гексозы: глюкозу, галактозу, маннозу и пентозы: ксилозу и арабинозу; целлюлоза — в глюкозу. Лигнин при гидролизе остается в виде нерастворимого остатка.
Гидролиз древесины осуществляют в гидролизном аппарате — стальном цилиндрическом сосуде. В результате гидролиза получают гидролизат, содержащий около 2-3% сбраживаемых моносахаридов и нерастворимый остаток-лигнин. Последний можно использовать непосредственно в производстве строительных плит, в кирпичном производстве, при помоле цемента, в качестве топлива; после соответствующей обработки лигнин может применяться в производстве пластмасс, резиновой промышленности и др.
Полученный гидролизат направляют в испаритель, где пар отделяется от жидкости. Выделяющийся пар конденсируют и используют для выделения из него фурфурола, скипидара и метилового спирта. Затем гидролизат охлаждают до 75-80°С, нейтрализуют в нейтрализаторе известковым молоком до pH 4-4,3 и добавляют питательные соли для дрожжей (сернокислый аммоний, суперфосфат). Полученный нейтрализат отстаивают для освобождения от выпавшего осадка сернокислого кальция и других взвешенных частиц. Осевший осадок сернокислого кальция отделяют, сушат, обжигают и получают алебастр, используемый в строительной технике. Нейтрализат охлаждают до 30-32°С и направляют на брожение. Подготовленный таким образом к брожению гидролизат называется суслом. Брожение гидролизного сусла производят непрерывным способом в бродильных чанах. При этом дрожжи непрерывно циркулируют в системе; дрожжи отделяют от бражки на сепараторах. Выделяющийся при брожении углекислый газ используют для выпуска жидкой или твердой углекислоты. Зрелую бражку, содержащую 1,0-1,5% спирта, направляют для перегонки и ректификации на брагоректификационный аппарат и получают этиловый спирт, метиловый спирт и сивушное масло. Барда, полученная после перегонки, содержит пентозы и ее используют для выращивания кормовых дрожжей.
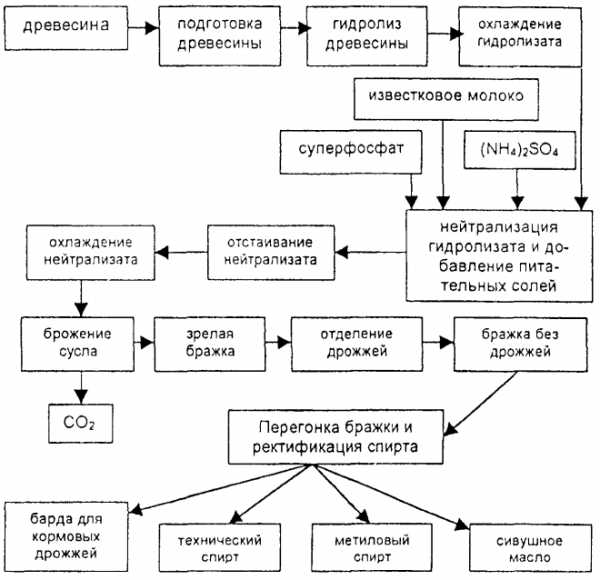 Рисунок 1 — Технологическая схема комплексной переработки древесины на гидролизно-спиртовых заводах
Рисунок 1 — Технологическая схема комплексной переработки древесины на гидролизно-спиртовых заводахПри переработке по указанной схеме из 1 т абсолютно сухой хвойной древесины можно получить следующие количества товарных продуктов:
- Спирта этилового, л ………………….. 187
- Жидкой углекислоты, кг …………….. 70
- или твердой углекислоты, кг ……… 40
- Дрожжей кормовых, кг…………….. .. 40
- Фурфурола, кг …………………………….9,4
- Скипидара, кг ……………………………0,8
- Термоизоляционных и строительных лигно-плит, м2 …. 75
- Алебастра строительного, кг ……..225
- Сивушного масла, к г ………………..0,3
Производство спирта из сульфитных щелоков
При производстве целлюлозы из древесины по сульфитному способу в качестве отхода получают сульфитный щелок — коричневую жидкость с запахом сернистого газа. Химический состав сульфитного щелока (%): вода — 90, сухие вещества — 10, в том числе производные лигнина — лигносульфонаты — 6, гексозы — 2, пентозы -1 , летучие кислоты, фурфурол и другие вещества — около 1. Длительное время сульфитные щелока спускали в реки, они загрязняли воду и уничтожали рыбу в водоемах. В настоящее время у нас имеется ряд заводов по комплексной переработке сульфитного щелока на этиловый спирт, кормовые дрожжи и сульфитно-бардяные концентраты. Производство спирта из сульфитных щелоков состоит из следующих стадий: подготовка сульфитного щелока к брожению, сбраживание сульфитнощелокового сусла, перегонка зрелой сульфитной бражки.
Подготовку сульфитного щелока к сбраживанию осуществляют по непрерывной схеме. Щелок продувают воздухом для удаления летучих кислот и фурфурола, задерживающих процесс брожения. Продутый щелок нейтрализуют известковым молоком и затем выдерживают для укрупнения выпавших кристаллов сернокислого и сернистокислого кальция; при этом добавляют питательные соли для дрожжей (сернокислый аммоний и суперфосфат). Затем щелок отстаивают. Осевший осадок- шлам — спускают в канализацию, а осветленный щелок охлаждают до 30-32°С. Подготовленный таким образом щелок называется суслом. Сусло направляют в бродильное отделение и сбраживают так же, как гидролизаты древесины, или применяют метод с подвижной насадкой. Подвижной насадкой называются волокна целлюлозы, остающиеся в щелоке. Метод брожения с подвижной насадкой основан на свойстве некоторых рас дрожжей сорбироваться на поверхности целлюлозных волокон и образовывать хлопья волокнисто-дрожжевой массы, которая в зрелой бражке быстро и полно оседает на дно чана. Брожение проводят в бродильной батарее, которая состоит из головного и хвостового чанов. В бродящем сусле волокна целлюлозы с сорбированными дрожжами находятся в непрерывном движении под влиянием выделяющегося углекислого газа. Отбродившая бражка поступает из головного чана в хвостовой, где заканчивается процесс брожения, и волокна с дрожжами оседают на дно. Осевшую дрожжеволокнистую массу насосом возвращают в головной чан, куда одновременно подают сусло, а зрелую бражку, содержащую 0,5-1% спирта, направляют в брагоректификационный аппарат и получают этиловый спирт, метиловый спирт и сивушное масло. Полученная после перегонки барда содержит пентозы и служит питательной средой для выращивания кормовых дрожжей, которые затем отделяют, высушивают и выпускают в виде сухих дрожжей. Барду после отделения дрожжей, содержащую лигносульфонаты, упаривают до содержания сухих веществ 50-80%. Полученный продукт называется сульфитно-бардяным концентратом и применяется в производстве пластических масс, строительных материалов, синтетических дубителей для получения кожи, в литейном производстве и дорожном строительстве.
Из сульфитно-бардяных концентратов можно получить ценное ароматическое вещество — ванилин.
Технологическая схема комплексной переработки сульфитных щелоков на этиловый спирт, кормовые дрожжи и сульфитно-бардяные концентраты показана на рисунке 2.
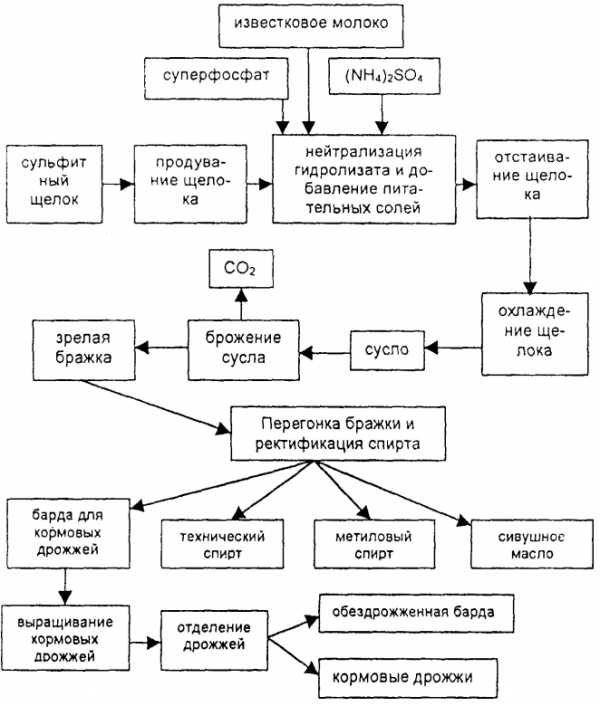 Рисунок 2 — Технологическая схема переработки сульфитных щелоков на спирт
Рисунок 2 — Технологическая схема переработки сульфитных щелоков на спиртПри переработке сульфитных щелоков получают в пересчете на 1т еловой древесины:
- Спирта этилового, л ……………….. 30-50
- Спирта метилового, л …………………… 1
- Жидкой углекислоты, л ………….. 19-25
- Сухих кормовых дрожжей, кг …. 15
- Сульфитно-бардяных концентратов влажностью 20%, кг …. 475
Производство спирта синтетическим методом
Сырьем для производства синтетического этилового спирта служат газы нефтеперерабатывающих заводов, которые содержат этилен. Кроме того, можно использовать и другие этиленсодержащие газы: коксовый газ, получаемый при коксовании угля, и попутные нефтяные газы.
В настоящее время синтетический этиловый спирт получают двумя способами: сернокислотной гидратацией и прямой гидратацией этилена.
Сернокислая гидратация этилена
Производство этилового спирта этим способом состоит из следующих процессов: взаимодействия этилена с серной кислотой, при котором образуются этилсерная кислота и диэтилсульфат; гидролиз полученных продуктов с образованием спирта; отделение спирта от серной кислоты и очистка его.
Сырьем для сернокислой гидратации служат газы, содержащие 47-50% вес. этилена, а также газы с меньшим содержанием этилена. Процесс осуществляется по схеме, приведенной ниже.
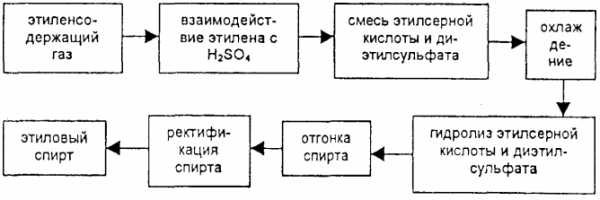 Рисунок 3 — Технологическая схем а получения синтетического спирта способом сернокислотной гидратации
Рисунок 3 — Технологическая схем а получения синтетического спирта способом сернокислотной гидратацииЭтилен взаимодействует с серной кислотой в реакционной колонне, представляющей собой вертикальный цилиндр. Внутри колонны находятся колпачковые тарелки с переливными стаканами. В нижнюю часть колонны компрессором подают этиленосодержащий газ, сверху в колонну подводят для орошения 97-98%-ная серная кислота. Газ, поднимаясь вверх, на каждой тарелке барботирует через слой жидкости. Этилен с серной кислотой взаимодействует по реакциям:
Из реакционной колонны непрерывно вытекает смесь этилсерной кислоты, диэтилсульфата и непрореагировавшей серной кислоты. Эту смесь охлаждают в холодильнике до 50°С и направляют на гидролиз, при котором протекают такие реакции:
Моноэтилсульфат, полученный в результате второй реакции, подвергают дальнейшему разложению с образованием еще одной молекулы спирта.
Прямая гидратация этилена
Технологическая схема производства этилового спирта способом прямой гидратации этилена представлена ниже.
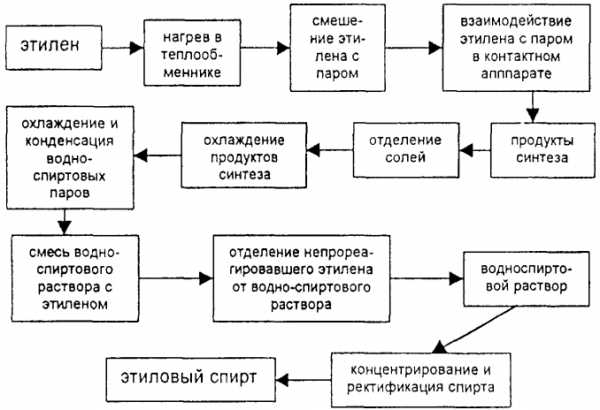 Рисунок 4 — Технологическая схема прямой гидратации этилена при производстве этилового спирта
Рисунок 4 — Технологическая схема прямой гидратации этилена при производстве этилового спиртаСырьем для способа прямой гидратации служит газ с высоким содержанием этилена (94-96%). Этилен сжимают компрессором до 8-9 КПа. Сжатый этилен смешивают с водяным паром в определённых соотношениях. Взаимодействие этилена с водяным паром производят в контактном аппарате — гидрататоре, представляющим собой вертикальную стальную полую цилиндрическую колонну, в которой находится катализатор (фосфорная кислота, нанесенная на алюмосиликат).
Смесь этилена и водяного пара при 280-300°С под давлением около 8,0 КПа подают в гидрататор, в котором поддерживают такие же параметры. При взаимодействии этилена с водяным паром, кроме основной реакции образования этилового спирта, протекают побочные реакции, в результате которых получаются диэтиловый эфир, уксусный альдегид и продукты полимеризации этилена. Продукты синтеза уносят из гидрататора небольшое количество фосфорной кислоты, которая может в дальнейшем оказывать коррозийное действие на аппаратуру и трубопроводы. Чтобы избежать этого, кислоту, содержащуюся в продуктах синтеза, нейтрализуют щелочью. Продукты синтеза после нейтрализации пропускают через солеотделитель, а затем охлаждают в теплообменнике и производят конденсацию водно-спиртовых паров. Получают смесь водно-спиртовой жидкости и непрореагировавшего этилена. Непрореагировавший этилен отделяют от жидкости в сепараторе. Он представляет собой вертикальный цилиндр, в котором установлены перегородки, резко изменяющие скорость и направление газового потока. Этилен из сепаратора отводят во всасывающую линию циркуляционного компрессора и направляют на смешение со свежим этиленом. Водно-спиртовой раствор, вытекающий из сепаратора, содержит 18,5-19% об. спирта. Его концентрируют в отпарной колонне и в виде паров направляют для очистки в ректификационную колонну. Спирт получают крепостью 90,5% об. На заводах синтетического спирта применяется способ прямой гидратации этилена.
Производство синтетического спирта, независимо от способа его получения, значительно более эффективно, чем производство спирта из пищевого сырья. Для получения 1 т этилового спирта из картофеля или зерна необходимо затратить 160-200 чел -дней , из газов нефтепереработки только 10 чел -дней . Себестоимость синтетического спирта примерно в четыре раза меньше себестоимости спирта из пищевого сырья.
nomnoms.info
Абсолютный спирт. Промышленное производство спирта из биологического сырья
Абсолютный этиловый спирт нашел себе применение в промышленности. Это вещество необходимо для обеспечения реакции органического синтеза. Такую жидкость в настоящее время нередко используют в лабораториях. Впервые технические условия, посвященные этому веществу, были изданы в 37-ом году. В настоящее время действуют специализированные ГОСТы и стандарты, регламентирующие качество жидкости и нюансы ее приготовления.
Общая информация
Как было определено в 1937 году, абсолютный спирт – это такая жидкость, крепость которой оценивается в 99,7 % или больше. Допускается наличие в каждых 100 граммах до 5 мг альдегидов. При исследовании вещества на органические кислоты все такие соединения нужно пересчитать на уксусную. Концентрация не может превышать миллилитра на 100 мл готовой продукции.
Отличительная особенность абсолютного спирта – отсутствие какого-либо сухого остатка. В этом веществе не может быть щелочных соединений, минеральных кислот. Не допускается включение фурфурола. Спирт должен быть прозрачным, без какого-либо оттенка и окраски. Ему не присущи посторонние запахи, не допускается наличие специфического вкуса.

Нюансы терминологии
Современным химикам известен не только абсолютный спирт, но и безводный. Эти два термина нельзя приравнивать. В абсолютной разновидности, как можно заключить из сказанного выше, вода может быть, но в малом количестве.
Рассматриваемое химическое соединение способно формировать стойкие связи при химической реакции с бензином. За счет этого абсолютный спирт в ряде стран используется для производства моторного топлива. Как показали исследования, если эту жидкость примешать к бензину, становятся существеннее антидетонационные качества топлива, используемого для работы мотора. Следовательно, возможно большее сжатие.
Особенности и формы
О том, чем отличается дистиллят от ректификата, может рассказать квалифицированный химик. Дистиллят получают путем брожения и перегонки, а ректификат — продукт, очищенный от примесей. Кроме того, при использовании методики ректификации можно добиться готового этилового спирта, концентрация основного вещества в котором – до 95,7 %. Такие параметры обусловлены наличием этилового спирта в азеотропных соединениях, появляющихся при химическом взаимодействии с водой в условиях нормального атмосферного давления.
Обычно в настоящее время используется советующий ГОСТу 5964-93 этиловый спирт. Именно он наиболее востребован в народном хозяйстве. В такой жидкости вода содержится в концентрации 4,43 % или немногим более. В определенных случаях для протекания реакции необходимо обеспечить наличие спирта, в котором практически нет воды, тогда прибегают к абсолютной разновидности. Это необходимо при изготовлении фармацевтической продукции, лаков и красок. Абсолютная разновидность востребована в изготовлении косметики, парфюмерии. Для изготовления вещества были разработаны реакции абсолютирования.

Ошибки и заблуждения
Так сложилось, что представленный в аптеках спирт – это тот самый продукт, который первым приходит в голову, стоит упомянуть хоть какой-нибудь спирт. Если обыватели разговаривают об этиловом спирте, как правило, тема сводится к обсуждению крепости жидкости, и некоторые сожалеют, что нет абсолютного, настоящего спирта, то есть такого, который бы на 100 % состоял из собственно спирта, не имея специальных разбавителей и добавок. Многие убеждены, что максимальная крепость – 95,6 %. На самом деле абсолютный спирт существует, просто знают об этом преимущественно химики, так как именно в этой сфере промышленности ему нашлось применение.
Некоторые раздумывают: скажем, какой-нибудь «Иткульский спиртзавод» использует ли в своей работе абсолютный продукт? Не стоит заблуждаться на этот счет: абсолютная жидкость не предназначена для пищевых целей, ее применяют в производственной промышленности, но не для изготовления напитков.
О терминах и явлениях
Прежде чем разбираться, чем отличается продукция того же упомянутого «Иткульского спиртзавода» от промышленного продукта, разумно сориентироваться в термине «крепость» применительно к спиртосодержащим жидкостям. Этот параметр был введен для отражения наличия этанола в смеси спирта и воды. То, что люди привыкли именовать спиртом, в норме представляет собой соединение с водой, и любой спирт, используемый в продуктовой промышленности, обязательно имеет воду в своем составе. Содержание этого вещества варьируется.
Концентрация абсолютного этилового спирта, как следует из действующих стандартов, должна составлять 99,7 % или быть еще больше, то есть в общем объеме на воду выделяются тысячные доли процента. Для реального использования такой продукт обычно не требуется, применять его неоправданно в силу сложности изготовления. Даже для медицинских целей хватает крепости 95 %, не говоря уже о пищевом применении. В редких случаях необходимо использовать гидролизный спирт.

Откуда взять?
О том, как сделать спирт, могут рассказать опытные химики. Специализированные предприятия, ответственные за этот процесс, ежедневно изготавливают большие объемы продукта разной степени концентрации. Известно несколько методик приготовления спирта, и самый популярный вариант – естественная реакция брожения. Для ее реализации необходимо иметь в своем распоряжении растительную продукцию, обогащенную углеводами. Еще один подход – реакция гидролиза с использованием целлюлозы, добываемой из соломы, древесины.
Исходя из того, гидролизный спирт нужен или нет, можно прибегнуть к реакции гидратации этилена. Этим словом обозначается газ. Для реакции задействуют ортофосфорную либо серную кислоту. Химическое взаимодействие, протекающее при комбинации этих веществ, довольно сложное, реакция требует участия катализатора, но ее эффективность достаточно высока, чтобы метод получил промышленное распространение.
Реакции и продукты
Прибегая к описанным ранее методам того, как сделать спирт, можно получить в свое распоряжение продукт относительно невысокой концентрации. В готовой жидкости будут содержаться разнообразные примеси. Чтобы очистить вещество и увеличить процент содержания спирта, необходимо организовать перегонку. Для этого можно использовать традиционную перегоночную установку или ректификационную колонну. Аналогичную установку применяют при необходимости обработать нефть. По итогам таких мероприятий можно изготовить спирт, крепость которого – до 95,6 %.
Представленный в аптеке спирт – это именно такой продукт, но для некоторых операций и реакций его недостаточно, и нужно изготовить абсолютный. Есть несколько известных методов, но все они довольно сложны. Можно связывать воду, включенную в состав спирта, глицерином. Еще один вариант – химические реакции с металлами. Иногда прибегают к гипсу или калиевым солям. Определенной эффективностью обладает реакция с негашеной известью. Можно использовать хлористый кальций. На практике все эти методы встречаются редко, так как реализовать их в промышленных масштабах сложно, несмотря на хороший итог взаимодействия.

Что делать?
Из описанного выше ясно, почему на абсолютный спирт цена высока. Чтобы получить этот непростой продукт, приходится применять установки для азеотропного обезвоживания. Для работы системы необходимо использовать высокопроцентный раствор спирта в воде. Вещество смешивают с бензолом в жидкой форме, затем перегоняют полученные соединения в предназначенных для этого колоннах. Разработано несколько азеотропных методик. Результат процесса – довольно большой объем этилового спирта, крепость которого варьируется в пределах 99,9-100 %.
Хотя на абсолютный спирт цена высока, необходимость использования этого соединения в ряде химических процессов обуславливает немалый спрос, поэтому отечественные и иностранные предприятия изготавливают довольно большие объемы абсолютного продукта. Готовую жидкость включают в топливо для космического транспорта, используют в автомашинах и при изготовлении ряда продукции, используемой обывателями в повседневности. А вот в обычной жизни встретиться с абсолютным спиртом человеку, далекому от химии и производства, вряд ли придется.
Нюансы получения
В настоящее время этиловый спирт получил широкое распространение в биологии. Это вещество необходимо для консервирования разнообразных препаратов. Зачастую биологи применяют именно абсолютную форму. При этом учитывают, что обычной перегонкой нельзя очистить продукт до необходимого уровня, так как формируется кипящая смесь, не поддающаяся разделению при применении классической перегоночной установки. Температура кипения спирта крепостью 95,6 % составляет 78,15 градуса по шкале Цельсия, а для абсолютного этот показатель – 78,37 градуса.
Отмечается, что практически лишенный воды спирт для биологических целей иногда получают, продолжительное время настаивая ректификат на медном сернокислом порошке, – такой продукт изготавливают, прокаливая медный купорос. Благодаря соли вода практически полностью уходит из основной смеси, при этом порошок не растворяется в спирте. Если взять прокаленную известь и несколько часов кипятить ее в спирте, результат реакции будет еще более качественным. Заключительным этапом такого процесса становится отгонка, в ходе которой необходимо исключить взаимодействие с воздухом, содержащим влагу.
Технические моменты
Этанол представляет собой жидкость без запаха и цвета. Ей присущ жгучий вкус и своеобразный запах. Этанол кипит при нагревании до 78,4 по шкале Цельсия, плавится при -114,15 по той же шкале измерения. Плотность вещества оценивается в 0,794 т/м.
Не составит труда перемешать этиловый спирт и воду, глицерин и разнообразные иные спирты, некоторые эфиры и растворители органической природы. Вещества можно смешивать в любых концентрациях и соотношениях. С определенными веществами метилкарбинол формирует азеотропную смесь. Это наблюдается при взаимодействии не только с водой, но и с хлороформом. Азеотропное соединение генерируется, если этиловый спирт смешать с этилацетатом, бензолом. Этанолу присуща способность формировать алкоголяты, если вещество взаимодействует с магниевыми, кальциевыми солями.

Спирт: а какой бывает?
Принято делить спирт на пищевой, технический. Определение принадлежности к категории зависит от того, что было применено для получения жидкости. О том, чем отличается дистиллят от ректификата, об особенностях разных категорий хорошо знают химики, ответственные за изготовление вещества. Ректификат — более чистый продукт, в отличие от дистиллята, имеющего характерный запах.
Возможности применения спирта определяются его крепостью, качеством ректификации. Выше был рассмотрен абсолютный спирт, необходимый для технических целей, но довольно любопытная тема – пищевой. Такую жидкость изготавливают из растительной продукции, продуктов питания. Для получения этилового спирта используется картофель, некоторые ягоды и фрукты. Можно применять зерновые культуры. Наиболее дешевый вариант – спирт, полученный из картофеля.
Для технического спирта в качестве сырья можно брать древесину. Иногда его получают при работе с продуктами трансформации нефти. При изготовлении технического спирта исходное сырье помещают в установку, где протекает гидролиз. В техническом спирте в обилии представлены опасные для человеческого здоровья примеси. По этой причине его нельзя использовать в пищевой промышленности.
Особенности производственного процесса
Качественный спирт получают, если рабочий процесс протекает с использованием надежного сырья, если соблюдается технология и качественно исполняется перегонка, во время которой изымаются вредоносные соединения. Степень очистки – основание причисления продукции к конкретному сорту.

Чем сорт спирта выше, тем меньше в нем вредных соединений. Кроме того, это показывает его крепость. Используемый в пищевой промышленности этиловый спирт получают, разбавляя ректификат, прошедший процедуру очистки высокоэффективными методиками. Для разбавления применяют умягченную воду.
fb.ru
Технология и оборудование для производства спирта
С давних пор популярны напитки, изготовленные на основе этанола. На Руси гнали самогон самыми разными способами, некоторые из которых применяются до сих пор. Существуют и более совершенные методы, есть современное оборудование.
В настоящее время производство и сбыт алкогольной продукции не находятся под запретом государства. Они доступны любому желающему.
Что такое этанол
Этанол — это всем известный из химии одноатомный этиловый спирт, имеющий формулу С2Н5ОН.
В составе алкогольных напитков он является психоактивным веществом, оказывающим угнетающее действие на центральную нервную систему человека.
Этиловый спирт применяется ещё в спиртовых термометрах, в качестве растворителя, как дезинфицирующее средство, при изготовлении косметических средств.

Как образуется этанол
Этиловый спирт получается в результате брожения продуктов, содержащих углеводы, под влиянием дрожжей и бактерий. Содержание этанола в получаемом растворе (бражке) не превышает 15%, при большей концентрации дрожжи гибнут.
Для увеличения концентрации этанола и его очистки производят дистилляцию — испарение спиртовой жидкости и охлаждение паров с целью их конденсации.
Сырьём для получения бражки может служить любой пищевой продукт, содержащий сахар или крахмал. Чем больше сахара или крахмала содержит продукт, тем плотнее получается бражка, и тем больше спирта можно из неё получить.
Самый большой выход спирта получается из сахара, затем идёт с уменьшением:
- пшеница;
- патока;
- сахарная свёкла;
- яблоки.
Сырьё сбраживают с помощью обычных хлебопекарных дрожжей, для ускорения процесса добавляют ферменты.
В полученной бражке содержится некоторый процент сивушных масел и альдегидных спиртов. Они отделяются от чистого спирта в процессе ректификации. Меньше всего сивушных масел и альдегидов получается при использовании пшеницы в качестве сырья.
Особенности процесса производства
Процесс изготовления спирта несложный, но надо иметь представление о технологии его изготовления, чтобы знать, какие аппараты потребуются на том или ином этапе производства.
Основное оборудование состоит из следующих элементов.
Нержавеющая ёмкость для приготовления браги — бражной бак. В бак загружается сырьё. Он имеет:
- сливной кран;
- гидрозатвор.

Перегонная установка, в которую входят:
- бражная колонна, в которой происходит перегонка браги;
- ректификационная спиртовая колонна, в которой происходит очищение спирта.

К вспомогательному оборудованию относятся:
Определённые требования предъявляются к помещениям, в которых располагаются перегонные установки. Эти требования минимальны.

Производство этилового спирта
Помещение должно быть отапливаемым, иметь принудительную вентиляцию, водопровод и канализацию. Высота помещения должна соответствовать высоте оборудования.
Большинство спиртовых заводов используют аппараты для ректификации браги, которые работают бесперебойно и сразу отделяют примеси от спирта-сырца. На выходе получается готовый очищенный этиловый спирт.
Спиртовая жидкость перегоняется с целью разделения фракций. При этом используется тот факт, что жидкости кипят при разных температурах.
Спирт является более летучим, чем вода, он имеет температуру кипения 78 градусов, поэтому его пары, образующиеся при нагреве, являются более концентрированными, чем спиртовая жидкость.
Оборудование для производства спирта
Спиртовое оборудование представлено двумя видами:
- С одной колонной. В этой установке бражка и флегма, которая подаётся из дефлегматора, вывариваются в одной колонне. Сама колонна поделена на две секции: бражную и спиртовую.
- С двумя колоннами, установленными раздельно. Одна из них — бражная, другая — спиртовая.

Способ производства спирта этилового
В этой установке флегма подаётся из дефлегматора во вторую колонну. Бражная колонна предназначена для образования водно-спиртовых паров. Спиртовая колонна собирает эти пары в верхней части колонны, а в нижней её части завершается процесс вываривания флегмы (лютера).
За счёт использования двух колонн брага получается более концентрированной.
Спиртовое оборудование с одной колонной содержит в своём составе:
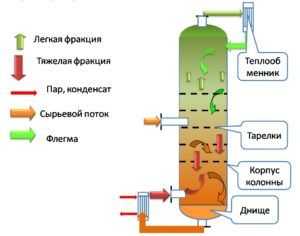
Схема спиртового оборудования с одной колонной
- колонну;
- двухбарабанный дефлегматор;
- холодильник для спирта;
- регулятор барды;
- прочее оборудование.
Колонна является основой этого аппарата и служит для извлечения спирта из браги путём сложной перегонки. Внутри колонну разделяют на секции колпачки или ситчатые тарелки в количестве 16–18 штук. Они служат для обеспечения тесного соприкосновения пара с жидкостью, которые движутся навстречу друг другу.
Нижнюю часть колонны называют истощающей (бражной), а верхнюю — укрепляющей (спиртовой).
В самой нижней части колонны, называемой выварной камерой, завершается процесс вываривания спирта из бражки, а также происходит вывод остатков (барды) из колонны.
Назначение дефлегматора — конденсация части проходящей паровой смеси и направление полученного конденсата (флегмы) обратно в аппарат навстречу пару.

Материал для производства
Сырьё для производства этилового спирта нужно выбирать с учётом конечного продукта, который необходимо получить. Для изготовления этанола класса Экстра и Люкс необходимы зерновые культуры, для высшего и первого сорта возможно использование любого продукта с содержанием крахмала.
Получение гидролизного спирта
Виды сырья для переработки довольно разнообразны. Самым продуктивным из них является сахар, из 10 кг этого сырья получают 5 и более кг чистого спирта. Однако сахар — дорогой продукт.
Можно использовать зерновые культуры, в том числе рис и кукурузу. Из пшеницы получают до трёх литров спирта.
Сахарная свёкла, картошка и фрукты (виноград, сливы, яблоки) являются наименее производительным сырьём, они дают всего один литр спирта.
Можно использовать разное сырьё, но нужно учесть, что бражки разных видов нельзя смешивать при изготовлении питьевого спирта.
Технология производства спирта
Подготовительные операции включают промывку, очистку, разваривание сырья, приготовление солода.
Первая стадия производства спирта заключается в переработке сырья, содержащего сахар или крахмал, в бражку — содержащую спирт жидкость. Сахар, содержащийся в бражке, преобразуется в алкоголь под действием дрожжей.
Бродильные ёмкости из нержавейки лучшего всего подойдут для приготовления спирта
Для проведения этого процесса используют бродильные ёмкости. Они могут быть:
- стальными;
- пластиковыми;
- деревянными;
- алюминиевыми.
Лучшим вариантом является ёмкость из нержавеющей стали.
Процесс брожения длится в течение недели.
Перегонка и ректификация браги
Вторая стадия предусматривает перегонку и ректификацию браги. Из неё выделяется спирт в процессе нагревания, который проходит через ректификационную колонну, где от него отделяются сивушные масла и альдегиды.
Перегонкой называют процесс выделения этанола из готовой браги, а получаемый продукт называется спиртом-сырцом. После этого процесса остаётся барда.
Большинство спиртзаводов имеют оборудование, позволяющее сразу отделять все примеси от спирта-сырца и получать готовый продукт — чистый этанол.
Рассмотрим, как функционирует спиртовая колонна:

Аппарат для перегонки спирта — схема
- в трубы дефлегматора подаётся насосом бражка. Здесь она подогревается до 75–90ºС за счёт конденсата спирто-водяных паров, образовавшегося в межтрубном пространстве дефлегматора;
- смесь подходит через смотровой фонарь к верхней тарелке бражной колонны вместе с флегмой из верхней спиртовой колонны;
- пройдя через все тарелки, брага спускается в выварную камеру;
- проходящий снизу вверх пар подогревает брагу до кипения при контакте с ней, и ещё больше насыщается спиртом, в то время как брага теряет его;
- остатки выпаренной браги (барда) содержат всего лишь 0.015% спирта;
- из бражной части колонны пары попадают в спиртовую часть. В результате контакта с флегмой, спускающейся навстречу, пары ещё больше обогащаются спиртом из закипевшей флегмы;
- в дефлегматоре, на выходе из спиртовой колонны, происходит частичное конденсирование паров, затем они в качестве флегмы поступают на верхнюю тарелку;
- оставшиеся пары направляются в холодильник, где происходит их конденсирование и охлаждение в змеевиках. Образовавшийся готовый продукт направляется в спиртохранилище.
Спирт-сырец должен иметь крепость не ниже 88%.

Спирт-сырец с хорошим показателем крепости
Особенности бизнеса по производству спирта
Для обеспечения собственных нужд не нужно какого-то сложного оборудования и лицензии. Небольшую установку можно поместить в гараж.
А для развития бизнеса нужно и помещение больше, и оборудование посолиднее.
Прежде чем предпринять шаги по организации собственного производства, необходимо выяснить следующие вопросы:

Процессы брожения и гниения
- источники снабжения сырьевыми материалами;
- возможности сбыта готовой продукции;
- возможности приобретения оборудования;
- получение лицензии.
Только после анализа всех вопросов можно приступать к поиску помещения, закупке оборудования, сырья, начинать изготовление пробной продукции.
Продукция пользуется широким спросом. Спирт используется не только для изготовления алкогольных напитков. Он нужен фармацевтическим, химическим и другим заводам, производителям парфюмерии и косметики.
Видео по теме: Бизнес-план по производству спирта
promzn.ru
Производство этилового спирта
Производство этилового спирта
Федеральное агентство по образованию
Томский государственный университет (ТГУ)
Химический факультет
Реферат
Тема: Производство этилового спирта
Выполнила:
Солтыс Е.В.
Томск 2013
План
Введение
. Характеристика целевого продукта
. Транспортировка и хранение
. Экологическая безопасность
. Характеристика исходного сырья
. Физико-химическое обоснование основных процессов производства этилового спирта
.1 Спиртовое брожение
.2 Сернокислая гидратация этилена
. Описание технологической схемы процесса производства этилового спирта
.1 Структурная схема процесса
.2 Операторская схема процесса
. Расчет материального баланса ХТС
.1 Блок-схема
.2 Пересчет единиц
.3 Условная постоянная информация
.4 Балансовая математическая модель
.5 Соответствие переменных потокам
.6 Упорядочение переменных
.7 Материальный баланс ХТС производства этанола на 7900 кг этиленэтановой фракции
.8 Расчет основных технологических показателей процесса
.9 Поточная диаграмма
Заключение
Список используемой литературы
Введение
Спиртами называются органические вещества, молекулы которых содержат одну или несколько функциональных гидроксильных групп, соединенных с углеводородным радикалом.
Этиловый спирт широко используют в различных областях промышленности и прежде всего в химической. Из него получают синтетический каучук, уксусную кислоту, красители, эссенции, фотопленку, порох, пластмассы. Спирт является хорошим растворителем и антисептиком. Поэтому он находит применение в медицине, парфюмерии. В больших количествах этиловый спирт идет для получения спиртоводочных изделий.
Таким образом, этиловый спирт относится к числу многотоннажных продуктов основного органического синтеза, мировое производство этилового спирта составляет свыше 2,5 млн. т/г (по объему производства занимает первое место в мире среди всех органических продуктов).
1. Характеристика целевого продукта
Этанол C2H5OH (метилкарбинол, этиловый спирт) — бесцветная подвижная жидкость с жгучим вкусом и характерным запахом, температура кипения 78,39°С, температура плавления -114,15°С, плотность 0,794 т/м3. Этанол смешивается во всех отношениях с водой, спиртами, глицерином, диэтиловым эфиром и другими органическими растворителями. С некоторыми из них (водой, бензолом, этилацетатом, хлороформом) он образует азеотропные смеси различного состава. С водой дает азеотропную смесь, содержащую 95,6% спирта и, кипящую при температуре 78,1°С. В виде такого ректификата этиловый спирт обычно и употребляют в технике. Температура самовоспламенения этанола составляет 422,8°С. С воздухом образует взрывоопасные смеси в пределах концентраций 20% (по объему). Температура вспышки 13,0°С.
А спирт содержащий только доли процента воды — абсолютным спиртом. Такой спирт получают химической обработкой в присутствии водоотнимающих средств (например, свежепрокаленного СаО). Этанол образует алкоголяты с солями кальция и магния, например: CaCl2*4C2H5OH и MgCl2*6C2H5OH.
2. Транспортировка и хранение
Этиловый спирт перевозится в железнодорожных цистернах, автоцистернах, в бочках, бутылях и во флягах автомобильным транспортом в соответствии с Правилами перевозки опасных грузов. Этиловый спирт хранят на складах в специально оборудованных и предназначенных для него металлических резервуарах в соответствии с правилами приемки, хранения, отпуска, транспортирования и учета этилового спирта. Допускается хранить этиловый спирт на складах, предназначенных для хранения огнеопасных продуктов, в упаковке изготовителя.
3. Экологическая безопасность
Этиловый спирт — сильный наркотик. Попадая в организм, он быстро всасывается в кровь и приводит организм в возбужденное состояние, при котором человеку трудно контролировать свое поведение. Употребление спирта часто является основной причиной тяжелых дорожно-транспортных аварий, несчастных случаев на производстве и бытовых преступлений. Спирт вызывает тяжелые заболевания нервной и сердечно-сосудистой систем, а также желудочно-кишечного тракта. Спирт опасен в любой концентрации (водка, настойки, вино, пиво и т.д.). Этиловый спирт, применяемый для технических целей, специально загрязняют дурно пахнущими веществами. Такой спирт называют денатуратом (для этого спирт подкрашивают, чтобы отличить его от
чистого спирта).
4. Характеристика исходного сырья
В качестве исходного сырья в производстве этилового спирта используется этилен. В настоящее время основным способом его получения является пиролиз (высокотемпературный крекинг) углеводородов. Пиролизу подвергают фракции прямой перегонки нефти, состоящие алканов, циклоалканов, аренов, природные и попутные нефтяные газы, содержащие алканы. Этилен образуется в результате реакций распада тяжелых алканов и дегидрирования низкомолекулярных алканов. Потенциальный выход этилена зависит от вида исходного сырья. Виды сырья, используемые в мировом производстве этилена, и их доля в общем балансе производства следующие:
СырьеЭтанПропанБутанБензинГазойльДоля, %36113473
Лучшим сырьем являются парафины, поскольку с повышением содержания водорода в исходных углеводородах выход алкенов возрастает.
5. Физико-химическое обоснование основных процессов производства этилового спирта
.1 Спиртовое брожение
Известный с давних времён способ получения этанола — спиртовое брожение органических продуктов, содержащих углеводы (виноград, плоды и т. п.) под действием ферментов дрожжей и бактерий. Аналогично выглядит переработка крахмала, картофеля, риса, кукурузы, источником получения топливного спирта является вырабатываемый из тростника сахар-сырец и проч. Реакция эта довольно сложна, её схему можно выразить уравнением:
C6h22O6 ? 2C2H5OH + 2CO2
В результате брожения получается раствор, содержащий не более 15 % этанола, так как в более концентрированных растворах дрожжи обычно гибнут. Полученный таким образом этанол нуждается в очистке и концентрировании, обычно путем дистилляции.
Современная промышленная технология получения спирта этилового из пищевого сырья включает следующие стадии:
Подготовка и измельчение крахмалистого сырья — зерна (прежде всего — ржи, пшеницы), картофеля, кукурузы и т.п.
Ферментация. На этой стадии происходит ферментативное расщепление крахмала до сбраживаемых сахаров. Для этих целей применяются рекомбинантные препараты альфа-амилазы, полученные биоинженерным путем — глюкамилаза, амилосубтилин.
Брожение. Благодаря сбраживанию дрожжами сахаров происходит накопление в бражке спирта.
Брагоректификация. Осуществляется на разгонных колоннах (например, «Комсомолец»).
Отходами бродильного производства являются углекислый газ, барда, эфиро-альдегидная фракция, сивушный спирт и сивушные масла.
Спирт, поступающий из брагоректификационной установки (БРУ) не является безводным, содержание этанола в нем до 96,6 %. В зависимости от содержания в нем посторонних примесей, его разделяют на следующие категории:
сорт
высшей очистки
базис
Экстра
Люкс
Альфа
Производительность современного спиртового завода около 30000-100000 литров безводного спирта в сутки. Этот способ сохранился и до сих пор, но он связан с большими затратами пищевого сырья и не может удовлетворить промышленность.
В промышленных масштабах этиловый спирт получают из сырья, содержащего целлюлозу (древесина, солома), которую предварительно гидролизуют. Образовавшуюся при этом смесь пентоз и гексоз подвергают спиртовому брожению. В странах Западной Европы и Америки эта технология не получила распространения, но в СССР (ныне в России) существовала развитая промышленность кормовых гидролизных дрожжей и гидролизного этанола.
5.2 Сернокислая гидратация этилена
Сернокислый способ, предложенный А.М. Бутлеровым, получил промышленное осуществление только в послевоенные годы. Он состоит из следующих четырех стадий: 1) абсорбция этилена серной кислотой с образованием сернокислых эфиров; 2) гидролиз эфиров; 3) выделение спирта и его ректификация; 4) концентрирование серной кислоты.
Взаимодействие между этиленом и серной кислотой состоит из двух этапов: первый — физическое растворение этилена в серной кислоте и второй — гомогенное взаимодействие обоих компонентов с образованием алкилсульфатов по уравнениям:
C2h5 + h3SO4 = C2H5OSO3HH5OSO3H + C2h5 = (C2H5O)2SO2.
Поглощение (абсорбция) этилена серной кислотой — процесс обратимый, экзотермический (DH=-50232 кДж/моль), протекает с уменьшением объема.
Скорость абсорбции этилена описывается уравнением:
dG/dt = K*F*P*f(с),
где G — количество поглощаемого этилена, t — время, К — коэффициент, зависящий от интенсивности диффузии, и, следовательно, от интенсивности контакта реагентов (барботаж, перемешивание и т.д.), F — поверхность контакта реагентов, Р — парциальное давление этилена, f(c) — множитель, зависящий от концентрации серной кислоты.
Так, абсорбция этилена 93%-ной кислотой протекает в 10 раз медленнее, чем при концентрации 97,5%. Однако, применение для абсорбции этилена олеума нецелесообразно, т.к. при этом снижается выход этанола из-за образования побочных продуктов — сульфосоединений и повышенного образования полимеров.
При прочих равных условиях скорость абсорбции этилена увеличивается с ростом температуры и парциального давления, однако, при температуре выше 900С начинается интенсивное образование полимеров. Увеличение парциального давления этилена выше 2 МПа становится тоже малоэффективным.
Фактором, ускоряющим процесс абсорбции, является наличие в исходной серной кислоте этилсульфатов, которые, обладая свойствами эмульгаторов, увеличивают поверхность контакта вследствие пенообразования, и тем самым способствуют более быстрому и полному растворению этилена.
В настоящее время в промышленных установках приняты следующие условия абсорбции этилена: концентрация серной кислоты 97-98%, температура 80-850С, парциальное давление этилена на входе в абсорбер 1-1,5МПа, содержание пропилена и высших олефинов в исходной этилен-этановой фракции <0,1%. В ходе второй стадии идет гидролиз этил — и диэтилсульфата по уравнениям:
C2H5OSO3H + h3O à C2H5OH + h3SO4,
(C2H5O)2SO2 + 2h3O à 2 C2H5OH + h3SO4
Эта стадия также обратима, для обеспечения ее протекания необходим избыток воды, и, по возможности, быстрое удаление спирта из зоны реакции, т.к. кроме основной реакции идет образование диэтилового эфира:
(C2H5O)2SO2 + C2H5OH à C2H5OC2H5 + C2H5OSO3H,
(C2H5O)2SO2 + h3O à C2H5OC2H5 + h3SO4.
Главным преимуществом сернокислой гидратации по сравнению с прямой гидратацией является возможность применения неконцентрированного этилена, т.к. его концентрирование связано с большими капитальными и эксплуатационными затратами.
Однако, метод сернокислой гидратации имеет ряд недостатков. Среди них можно отметить следующие:
применение сложных и громоздких конструкций;
малоэффективное удаление полимеров однократным экстрагированием. При принятом методе экстрагирования в экстракт переходит 70-75% полимеров, значит, до 30% полимеров остается в разбавленной кислоте;
концентрирование отработанной серной кислоты. Эта часть технологического процесса является самым слабым звеном во всем методе сернокислой гидратации. Во-первых, концентрировать кислоту удается лишь до 88-90%, а, во-вторых, такой процесс концентрирования из-за высокой температуры топочных газов приводит к ощутимым потерям серной кислоты от раскисления, сопровождающегося выбросом вредного SO2 в атмосферу;
неиспользованные возможности экономии энергетических средств.
.3 Парофазная гидратация этилена
Наиболее разработанным применительно к имеющимся промышленным установкам в настоящее время является процесс газофазной гидратации:
Ch3=Ch3(г.) + h3O(г.) = C2H5OH(г.) + 41868Дж/моль.
Механизм:
Ch3=Ch3 + Н+ « СН3-СН2+,
СН3-СН2+ + Н2О « СН3-СН2-ОН2+,
СН3-СН2-ОН2+ « СН3-СН2-ОН + Н+.
Но наряду с основной реакцией идут параллельные и последовательные побочные реакции:
C2h5 + h3O = C2H5OC2H5,(C2h5) = (-Ch3-Ch3-)n.
Таким образом, процесс сложный, обратимый, несмещенный (таблица 1), экзотермический, протекает с уменьшением объема.
Таблица 1. Равновесный выход этанола.
Отношение количеств веществ: Мh3O/MC2h5Равновесный выход за один проход при давлении 8Мпа при температуре:2800С2900С0,615,48,530,818,310,15
Следует обратить внимание на два физико-химических фактора, которые определяют основные технологические параметры процесса. Прежде всего, это активность катализатора, которая имеет решающее значение для определения температуры процесса. Катализаторами прямой гидратации могут служить фосфорная кислота и ее соли. Чаще всего используется фосфорная кислота концентрацией 85-87% на таких носителях, как алюмосиликаты, силикагели, пемза и др.; значительная часть кислоты (до 35%) находится в свободном состоянии. Активность этого катализатора является невысокой. Только при температуре 280-3000С ее можно считать более или менее приемлемой для промышленных условий. При более высокой температуре в значительной мере развиваются побочные процессы: полимеризация этилена, усиленное образование эфира и т.д.
Другим отправным фактором в газофазном процессе выступает весьма низкая по сравнению с этиленом летучесть воды, которая имеет решающее значение для определения давления процесса. Последнее, при прочих равных условиях, зависит от парциального давления паров воды, т.е. тоже от температуры.
Таким образом, температура становится важнейшим параметром, определяющим не только скорость, но и общее давление процесса. Так, в соответствии со стехиометрическим уравнением реакции, для эквимолярной смеси этилена и паров воды, парциальное давление последних должно составлять примерно половину от общего давления. Однако с целью предотвращения конденсации водяного пара в самом реакторе, что приводит к разбавлению фосфорной кислоты и парализует действие катализатора, парциальное давление паров воды, а, значит, и общее давление, должно быть несколько ниже. И действительно, в промышленности применяют общее давление около 8,0МПа.
Имеются и другие пути, предотвращающие появление водяного конденсата. Во-первых, это повышение температуры. Однако, в силу экзотермичности процесса, этот путь принципиально непригоден, т.к. приводит к снижению конверсии этилена и интенсификации побочных процессов. Во-вторых, это снижение парциального давления паров водяного пара за счет повышения парциального давления этилена. Однако, этот путь тоже непригоден. Он также приводит к снижению выхода этанола, т.к. оптимальным соотношением между реагирующими компонентами является эквимолярное. Мольное соотношение, используемое в промышленности, этилен — пары воды равно 1 : 0,6-0,8.
Выбранное соотношение компонентов диктует выбор общего давления:
Робщ = РС2Н4 + РН2О + Ринерт.
Известно, что давление паров воды над 85%-ной фосфорной кислотой при температуре 2800С составляет 2,7МПа. Принимая во внимание мольное соотношение между компонентами, видно, что давление паров этилена составляет около 4,7МПа. В таком случае концентрация инертных примесей должна быть порядка 15% (Ринерт = РС2Н4*0,15/0,85). Давление больше 8МПа нежелательно т.к. происходит конденсация водяного пара.
В настоящее время процесс гидратации этилена реализуется в промышленности при следующих условиях: t = 280-3000С; Р = 8,0МПа; мольное соотношение пары воды: этилен = 0,6 : 0,8; катализатор — фосфорная кислота и фосфаты на алюмосиликате или силикагеле при содержании Н3РО4 до 35% в свободном состоянии, объемная скорость циркулирующего газа 1800-2000ч-1, что соответствует продолжительности контакта 18-20с и производительности 180-200кг этанола с 1м3 катализатора в 1 ч.
При этих условиях этилен расходуется примерно следующим образом: 95% — на образование этанола; 2-3% — этилового эфира; 1-2% — ацетальдегида; 1-2% — полимеров и др. продуктов.
В приведенных условиях гидратации максимальный выход (равновесный) за один проход может составить только 10%; практически он достигает лишь 5%, что приводит к необходимости многократной циркуляции реакционной газовой смеси через слой катализатора.
Увеличение объемной скорости является методом интенсификации рециркуляционного процесса, поэтому процесс синтеза этанола ведут с большими объемными скоростями.
Малая конверсия этилена и низкая производительность катализатора обусловили необходимость работы не с разбавленным, а с концентрированным 98-99% этиленом. Даже при таком концентрированном этилене, т.е. при содержании в нем до 2% инертных примесей, они накапливаются в рециркулирующем газе, что приводит к снижению содержания этилена. Нижний предел концентрации этилена принят сегодня 85%, что соответствует содержанию инертных примесей до 15%. Поэтому необходим отвод последних с частью рециркулирующего газа (отдувка), которая составляет 13% от подачи свежего 98%-ного этилена.
Из рециркулирующей реакционной газовой смеси необходим непрерывный отвод получаемого этанола. Практически удаление этанола производится обычным методом конденсации, при этом вода как менее летучий компонент конденсируется с большей полнотой. Это приводит к огромным затратам тепла (учитывая крупнотоннажность производства этанола) на получение водяного пара, из которого только 5% расходуется на конденсацию этанола, а остальные 95% — на конденсацию воды. Поэтому возникает острая необходимость в утилизации тепла непрореагировавшего водяного пара путем эффективного теплообмена между потоками выходящего из реактора и входящего в него газовых смесей, а также путем генерации вторичного водяного пара в котлах-утилизаторах. Относительно низкий температурный потенциал тепла (250-3000С) приводит к громоздкой системе теплообмена и теплоиспользующих аппаратов.
Однако интенсивная циркуляция реакционной газовой смеси, кратность которой (при выходе этанола около5%) достигает 20, и сравнительно невысокая теплота реакции позволяет весьма просто реализовать процесс в адиабатическом реакторе колонного типа. Выделяющаяся теплота реакции повышает температуру реагирующего газового потока лишь на 15-200С, что допустимо.
Несмотря на весьма малую летучесть фосфорной кислоты, унос ее в виде паров при такой значительной рециркуляции реакционной газовой смеси и высокой температуре достигает 0,4-0,5кг/ч с 1м3 катализатора, что может вызвать коррозию аппаратуры и ограничивает длительность нормальной работы катализатора до 500-600 часов. В связи с этим была разработана технология непрерывной подачи свободной фосфорной кислоты в реакционную газовую смесь на входе в реактор, нейтрализации ее щелочью на выходе из реактора и регенерация из полученных при нейтрализации солей. Это позволило увеличить длительность работы катализатора до 1500 часов, заметно сократить расход фосфорной кислоты и значительно уменьшить коррозию оборудования. Такой процесс можно проводить в стальной аппаратуре.
Из приведенной физико-химической характеристики процесса можно вывести основные положения, которые были приняты при разработке существующей технологической схемы.
Необходимо построить схему по принципу многократной циркуляции реакционной газовой смеси через реактор с отводом целевого продукта — этанола — конденсацией;
В качестве исходного продукта следует применять чистый этилен с минимальным содержанием инертных примесей, которые накапливаются в реакционной смеси и частично отводятся с рециркулирующей газовой смесью в виде «отдувки»;
Повышение давления процесса ограничено из-за опасности конденсации воды, снижающей активность катализатора;
Процесс необходимо проводить при эквимолярном или близком к нему соотношении этилен / водяной пар;
Необходимо наиболее полно регенерировать тепло, расходуемое на получение водяного пара;
Возможно применение адиабатического реактора простейшей конструкции;
Целесообразно подпитывать поступающую в реактор реакционную газовую смесь свежей фосфорной кислотой, необходима нейтрализация паров кислоты на выходе из реактора, включая регенерацию ее из выпавших солей.
6. Описание технологической схемы процесса производства этилового спирта
Технологические схемы синтеза этанола различаются способами получения водяного пара и системами утилизации тепла. В наиболее совершенных схемах водяной пар для синтеза получают путем рецикла воды после отделения этанола и использованием парового конденсата.
.1 Структурная схема процесса
Свежий и оборотный этилен сжимается в компрессорах (1), (2) до 8,0 Мпа, смешивается с водяным паром, поступающим обычно с ТЭЦ, подогревается в теплообменнике (4) теплом отходящей из реактора смеси и перегревается в трубчатой печи (3) до 275°С, после чего подается в реактор-гидратор (5). Перед входом в реактор в поток «вбрызгивается» фосфорная кислота для подпитки катализатора, что продлевает срок его службы (реакционная газовая смесь смешивается с подаваемой фосфорной кислотой при температуре 280-3000С).
Реактор представляет собой полую колонну высотой 10 м и диаметром 1,5 м, работающую в режиме идеального вытеснения. Для исключения влияния коррозии от фосфорной кислоты он выложен листами красной меди.
Реакционные газы содержат пары унесенной фосфорной кислоты, которая нейтрализуется гидроксидом натрия, а образующиеся соли выделяются в солеотделителе (6). Отток фосфорной кислоты составляет 0,4 — 0,5 т/час с 1 м3 катализатора.
Теплота отходящих реакционных газов регенерируется в теплообменнике (4) для нагрева входящей смеси. В холодильнике (7) происходит конденсация продуктов реакции, а в сепараторе (8) разделяются жидкие и газовые потоки. Вода, как менее летучий компонент, конденсируется с большей полнотой. Поэтому для дополнительного выделения спирта производится его отмывка водой в абсорбере (9). Непрореагировавший газ, содержащий 90 — 92% этилена, рециркулируют компрессором (2), а часть его сбрасывают, чтобы избежать накопления примесей в системе.
Отдувка составляет примерно 20% от введенного этилена и направляется на установку газоразделения для выделения этилена.
Водный конденсат после сепаратора (8) и жидкость из абсорбера (9) дросселируют, в результате чего выделяются растворенные газы, отделяемые в сепараторе низкого давления (10) и направляемые в топливную линию.
Жидкая фаза из сепаратора (10) представляет собой 15%-ный водный раствор этанола, содержащий примеси диэтилового эфира, ацетальдегида и низкомолекулярных полимеров этилена. Этот раствор подвергают ректификации в ректификационных колоннах (11) и (12). В первой отгоняют наиболее летучие диэтиловый эфир и ацетальдегид, а во второй — этиловый спирт в виде азеотропной смеси, содержащей 95% этанола и 5% воды. Обогрев колонны осуществляется острым паром. В кубе колонны (12) остается вода, которую очищают от соли в ионообменной установке (13) и возвращают на гидратацию, организуя замкнутый цикл по технологической воде. Это позволяет значительно снизить расход свежей воды, исключить сброс отработанной воды в стоки и сократить потери этанола.
При необходимости получения безводного спирта этанол-ректификат направляют в дегидратор. Расход этилена на производство 1 т этилового спирта составляет 0,7 т (теоретический расходный коэффициент 0,61 т C2h5). В структуре себестоимости спирта 30% приходится на стоимость сырья.
.2. Операторная схема процесса:
7. Расчет материального баланса ХТС
.1 Блок-схема
.2 Пересчет единиц
Доля по объему доля по массе;
h5 = 0,96*MC2h5 = 0,96*28 = 26,88 г,H6 = 0,04*MC2H6 = 0,04*30 = 1,2 г,? = mC2h5 + mC2H6 = 26,88 + 1,2 = 28,08 г,
Тогда 26,88/28,08 = 0,958 масс долей или 95,8 % масс.,
,2/28,08 = 0,042 масс долей или 4,2 % масс.
7.3 Условная постоянная информация
№Содержание информацииУсловное обозначениеЕдиница измеренияПринятые значения1.Содержание С2Н4 в этиленовой фракцииg011доля по объему0,962.Содержание С2Н5ОН в ректификатеg401доля по массе0,9453.Норма расхода параКмоль Н2О / моль С2Н40,74.Конверсия этиленаcдоля единицы0,0555.Селективностьj1доля единицы0,9556.Степень превращения конвертированного этилена в — диэтиловый эфир — ацетальдегид j2 j3доля единицы 0,035 0,017.Содержание инертов в циркуляционном газеg51идоля по объему0,168.Количество свежей этиленэтановой фракции (базис расчета)Пкг79009.Доля отдуваемого газа, выходящего из сепаратораg35идоля по объему0,15
.4 Балансовая математическая модель
Баланс по этилену по первому узлу:
N12 = П*g011/Мэтилена + N51*(1-g51и)\
Количество воды, пошедшее на образование этанола:
(N012 + N41)/N12 = K
Баланс по этилену по третьему и пятому узлам:
N12*(1-c) = N51*(1-g51и) + N501*(1-g35и)
Баланс по этанолу по четвертому узлу:
N12*c*j1*Mэтанола = G401*g401
Баланс по диэтиловому эфиру:
G402 = 0,5* N12*c*j2*Mэфира
Баланс по ацетальдегиду:
G403 = N12*c*j3*Mацетальдегида
Баланс по воде по всей схеме:
N012= G401*g401/*Mэтанола + G401*(1-g401)/Мводы + G402/ Mэфира + G403/ Mацетальдегида
Отдувка
П*(1-g011)/Мэтана + G403/Mацетальдегид = N50*g35
.5 Соответствие переменных потокам
№Наименование потокаУсловное обозначениеciРазмерностьЗначение по расчету1.Циркул. поток этиленаN51c1кмоль39882.Поток этиленаN12c2кмоль36203.Свежий поток водяного параN012c3кмоль228,034.Циркул. поток водяного параN51c4кмоль23065.ОтдувкаN501c5кмоль83,4316.Поток этанола на выходе из блока разделенияG401c6Кг92697.Поток диэтилового эфира на выходе из блока разделенияG402c7Кг253,3798.Поток ацетальдегида на выходе из блока разделенияG403c8Кг87,597
.6 Упорядочение переменных
c2 = (1 — 0,16)c1 + 7900*0,957/28 = 0,84c1 + 270
c2 — 0,84c1= 270
(c3 + c4)/c2 = 0,7
c3 + c4 — 0,7c2 = 0
c2*(1 — 0,055) = c1*(1 — 0,16) + c5*(1 — 0,15)
,945c2 — 0,84c1 — 0,85c5 = 0
c2*0,055*0,955*46 = c6*0,945
,42c2 — 0,945c6 = 0
c7 = 0,5*0,055*0,035*74*c2
,07c2 — c7 = 0
c8 = 0,055*0,01*44*c2
,0242c2 — c8 = 0
c3 = c6*0,945/46 + c6*(1 — 0,945)/18 + c7/74 + c8/44
c3 — 0,024*c6 — 0,014*c7 — 0,023*c8 = 0
*(1 — 0,96)/30 + c8/44 = 0,15*c5
,023*c8 — 0,15*c5 = — 10,5
ciСв. членc1c2c3c4c5c6c7c8-0,84 0 -0,84 0 0 0 0 01 -0,7 0,945 2,42 0,07 0,0242 0 00 1 0 0 0 0 1 00 1 0 0 0 0 0 00 0 -0,85 0 0 0 0 -0,150 0 0 -0,945 0 0 -0,024 00 0 0 0 -1 0 -0,014 00 0 0 0 0 -1 -0,023 0,023270 0 0 0 0 0 0 -10,5
.7 Материальный баланс ХТС производства этанола на 7900 кг
этиленэтановой фракции
этилена = П*0,958 = 7900*0,958 = 7568 кгводы = N012*Мводы = 228,03*18 = 4104,54 кг (приход)этана= П*0,042 = 7900*0,042 = 332 кгспирта = G401*0,945 = 9269*0,945 =8759,2 кгпарар = N51*Мводы =2306*18 = 41508 кг воды = G401 — Gспирта = 9269 — 8759,2 = 509,8 кг (расход)диэтилового эфира = G402 = 253,379 кгацетальдегида = G403= 87,597 кг
Приходрасходнаименованиекг% массНаименованиекг% масс.1.Этиленовая фракция: этилен этан 2.Водяной пар (рец.) 3. Вода 7568 332 41508 4104,54 14 0,6 77,6 7,8Этанол Вода, введенная со спиртом Водяной пар (рец.) Диэтиловый эфир Отдувка Ацетальдегид Невязка8759,2 509,8 41508 253,38 2336,1 87,597 58,49416,4 0,9 77,6 0,5 4,3 0,2 0,1Всего53512,54100Всего53512,54100
.8 Расчет основных технологических показателей процесса
Расходные коэффициенты по сырью:
gпрактэтилена = G0этилена/ Gспирта = 7568/8759,2= 0,864
gпрактводы = G0воды/ Gспирта = 4204,54/8759,2 = 0,48
gтеорэтилена = Мэтилена/ Мспирта = 28/46 = 0,609
gтеорводы = Мводы/ Мспирта = 18/46 = 0,391
Выход этанола:
h = G спирта/Gспиртастех= Gспирта/(G этилена*(Mспирта /Мэтилена)) = 8759,2/7568*(46/28)*100% = 70,4 %
Конверсия этилена:
Х = (G спирта/Mспирта +Gдиэтилового эфира/Mдиэтилового эфира *2/1)/ (G этилена/ Мэтилена) = (8759,2/46+253,379/74*2)/(7568/28)=0,728=72,8%
7.9 Поточная диаграмма
Заключение
В заключении хотелось бы сказать, что в настоящее время находится широкое применение спиртов. На многих производствах спирты применяются в качестве растворителей. В химической промышленности они используются для различных синтезов. Метиловый спирт в больших количествах «идёт» на получение формальдегида, используемого в производстве пластмасс уксусной кислоты и других органических веществ. В настоящее время разрабатывается много новых технологических процессов на основе использования метилового спирта как исходного продукта, поэтому значение его в промышленном производстве нужных народному хозяйству, веществ и материалов будет всё более возрастать.
Перспективным считается использование метилового спирта в качестве моторного топлива т.к. добавка его к бензину повышает октановое число горючей смеси и снижает образование вредных веществ в выхлопных газах.
Этиловый спирт в больших количествах идёт на производство синтетического каучука. Окислением спирта получают пищевую уксусную кислоту. Путём его дигидратации готовят диэтиловый (медицинский) эфир, с взаимодействием с хлороводородом получают хлорэтан, для местной анестезии. Спирт применяется при изготовлении многих лекарств. В парфюмерии он идёт на изготовление духов и одеколонов.
Но также спирты могут оказывать негативное воздействие на организм. Особенно ядовит метиловый спирт: 5 -10 мл спирта вызывают слепоту и сильное отравление организма, а 30 мл могут привести к смертельному исходу.
Этиловый спирт — наркотик. При приеме внутрь он вследствие высокой растворимости быстро всасывается в кровь и возбуждающе действует на организм. Под влиянием спиртного у человека ослабевает внимание, затормаживается реакция, нарушается координация, появляется развязность, грубость в поведении и т. д. Все это делает его неприятным и неприемлемым для общества. Но следствия употребления алкоголя могут быть и более глубокими. При частом потреблении появляется привыкание, пагубное пристрастие к нему, и в конце концов тяжелое заболевание — алкоголизм. Спиртом поражаются слизистые оболочки желудочно-кишечного тракта, что может вести к возникновению гастрита, язвенной болезни желудка, двенадцатиперстной кишки. Печень, где должно происходить разрушение спирта, не справляясь с нагрузкой, начинает перерождаться, в результате возникает цирроз. Проникая в головной мозг, спирт отравляюще действует на нервные клетки, что проявляется в нарушении сознания, речи, умственных способностей, в появлении психических расстройств и ведет к деградации личности.
Особенно опасен алкоголь для молодых людей, так как в растущем организме интенсивно протекают процессы обмена веществ, а они особенно чувствительны к токсическому воздействию. Поэтому у молодежи быстрее, чем у взрослых, может появиться алкоголизм.
Список использованной литературы
Общая химическая технология: Учебник для химико-технологических специальностей. Т. 2.
Важнейшие химические производства. / Мухленов И.П., Авербух А.Я., Кузнецов Д.А. и др. Под редакцией И.П. Мухленова. — М.: Высш. шк.,1984.
Лебедев Н.Н. Химия и технология основного органического и нефтехимического синтеза. — М.: Химия, 1981.
Тимофеев В.С., Серафимов Л.А. Принципы технологии основного органического и нефтехимического синтеза. — М.: Химия, 1992.
Кононова Г.Н., Сафонов В.В. Учебно-методическое пособие « Производство этилового спирта прямой гидратацией этилена».
Сборник заданий курсовых и домашних работ для студентов 4 курса. В двух частях. Ч. 1./ Егорова Е.В., Игумнов М.С., Кононова Г.Н. и др. Под ред. Кононовой Г.Н., Сафонова В.В., Смирновой С.Н. — М.: ИПЦ МИТХТ им. М.В. Ломоносова, 2002.
diplomba.ru
Производство этилового спирта
Московская Государственная Академия
Тонкой Химической Технологии
им. М.В. Ломоносова
Кафедра общей химической технологии
Курсовая работа
на тему: «Производство этилового спирта»
Москва
Содержание
1. Введение
2. Исходное сырьё
3. Характеристика целевого продукта
4. Физико-химическое обоснование основных процессов производства этилового спирта
5. Описание технологической схемы процесса производства этилового спирта
6. Материальный баланс ХТС производства этанола на 9000кг 100% С2 Н5 ОН
7. Расчет основных технологических показателей процесса
8. Литература
1. Введение
Этиловый спирт находит широкое применение в народном хозяйстве в качестве растворителя, также применяется в производстве дивинила, в пищевой и медицинской промышленности, в качестве горючего для ракетных двигателей, антифриза и т.д., является важным промежуточным продуктом органического синтеза (в производстве сложных эфиров, целлулоида, искусственного шелка, ацетальдегида, уксусной кислоты, хлороформа, хлораля, диэтилового эфира и других продуктов).
Таким образом, этиловый спирт относится к числу многотоннажных продуктов основного органического синтеза, мировое производство этилового спирта составляет свыше 2,5 млн. т/г (по объему производства занимает первое место в мире среди всех органических продуктов).
2. Характеристика исходного сырья
В качестве исходного сырья в производстве этилового спирта используется этилен. В настоящее время основным способом его получения является пиролиз (высокотемпературный крекинг) углеводородов. Пиролизу подвергают фракции прямой перегонки нефти, состоящие алканов, циклоалканов, аренов, природные и попутные нефтяные газы, содержащие алканы.
Этилен образуется в результате реакций распада тяжелых алканов и дегидрирования низкомолекулярных алканов. Потенциальный выход этилена зависит от вида исходного сырья. Виды сырья, используемые в мировом производстве этилена, и их доля в общем балансе производства следующие:
Лучшим сырьем являются парафины, поскольку с повышением содержания водорода в исходных углеводородах выход алкенов возрастает.
3. Характеристика целевого продукта
Этанол C2 H5
4.Физико-химическое обоснование основных процессов производства этилового спирта
До недавнего времени производство этилового спирта основывалось на пищевом сырье – сбраживание крахмала из некоторых зерновых культур и картофеля с помощью ферментов, вырабатываемых дрожжевыми грибками. Этот способ сохранился и до сих пор, но он связан с большими затратами пищевого сырья и не может удовлетворить промышленность. Другой метод, также основанный на переработке растительного сырья, заключается в переработке древесины (гидролизный спирт). Древесина содержит до 50% целлюлозы, и при ее гидролизе водой в присутствии серной кислоты образуется глюкоза, которую подвергают затем спиртовому брожению:
(C6 H10 O5 )x + xH2 O — xC6 H12 O6 ,
C6 H12 O6 — 2C2 H5 OH + 2CO2 .
Синтетический этиловый спирт получают гидратацией этилена.
Гидратация этилена осуществляется двумя методами: при помощи серной кислоты (сернокислая гидратация) и непосредственным взаимодействием этилена с водяным паром в присутствии катализатора (парофазная каталитическая гидратация).
Сернокислая гидратация этилена
Сернокислый способ, предложенный А.М. Бутлеровым, получил промышленное осуществление только в послевоенные годы. Он состоит из следующих четырех стадий: 1) абсорбция этилена серной кислотой с образованием сернокислых эфиров; 2) гидролиз эфиров; 3) выделение спирта и его ректификация; 4) концентрирование серной кислоты.
Взаимодействие между этиленом и серной кислотой состоит из двух этапов: первый – физическое растворение этилена в серной кислоте и второй — гомогенное взаимодействие обоих компонентов с образованием алкилсульфатов по уравнениям:
C2 H4 + H
C2 H5 OSO3 H + C2 H4 = (C2 H5 O)2 SO2.
Поглощение (абсорбция) этилена серной кислотой – процесс обратимый, экзотермический (DH=-50232 кДж/моль), протекает с уменьшением объема.
Скорость абсорбции этилена описывается уравнением:
dG/dt = K*F*P*f(с),
где G – количество поглощаемого этилена, t – время, К – коэффициент, зависящий от интенсивности диффузии, и, следовательно, от интенсивности контакта реагентов (барботаж, перемешивание и т.д.), F – поверхность контакта реагентов, Р – парциальное давление этилена, f(c) – множитель, зависящий от концентрации серной кислоты.
Так, абсорбция этилена 93%-ной кислотой протекает в 10 раз медленнее, чем при концентрации 97,5%. Однако, применение для абсорбции этилена олеума нецелесообразно, т.к. при этом снижается выход этанола из-за образования побочных продуктов – сульфосоединений и повышенного образования полимеров.
При прочих равных условиях скорость абсорбции этилена увеличивается с ростом температуры и парциального давления, однако, при температуре выше 900 С начинается интенсивное образование полимеров. Увеличение парциального давления этилена выше 2 МПа становится тоже малоэффективным.
Фактором, ускоряющим процесс абсорбции, является наличие в исходной серной кислоте этилсульфатов, которые, обладая свойствами эмульгаторов, увеличивают поверхность контакта вследствие пенообразования, и тем самым способствуют более быстрому и полному растворению этилена.
В настоящее время в промышленных установках приняты следующие условия абсорбции этилена: концентрация серной кислоты 97-98%, температура 80-850 С, парциальное давление этилена на входе в абсорбер 1-1,5МПа, содержание пропилена и высших олефинов в исходной этилен-этановой фракции <0,1%. В ходе второй стадии идет гидролиз этил — и диэтилсульфата по уравнениям:
C2 H5 OSO3 H + H2 O — C2 H5 OH + H2 SO4 ,
(C2 H5 O)2 SO2 + 2H2 O — 2 C2 H5 OH + H2 SO4
Эта стадия также обратима, для обеспечения ее протекания необходим избыток воды, и, по возможности, быстрое удаление спирта из зоны реакции, т.к. кроме основной реакции идет образование диэтилового эфира:
(C2 H5 O)2 SO2 + C2 H5 OH — C2 H5 OC2 H5 + C2 H5 OSO3 H,
(C2 H5 O)2 SO2 + H2 O — C2 H5 OC2 H5 + H2 SO4.
Главным преимуществом сернокислой гидратации по сравнению с прямой гидратацией является возможность применения неконцентрированного этилена, т.к. его концентрирование связано с большими капитальными и эксплуатационными затратами.
Однако, метод сернокислой гидратации имеет ряд недостатков. Среди них можно отметить следующие:
— применение сложных и громоздких конструкций;
— малоэффективное удаление полимеров однократным экстрагированием. При принятом методе экстрагирования в экстракт переходит 70-75% полимеров, значит, до 30% полимеров остается в разбавленной кислоте;
— концентрирование отработанной серной кислоты. Эта часть технологического процесса является самым слабым звеном во всем методе сернокислой гидратации. Во-первых, концентрировать кислоту удается лишь до 88-90%, а, во-вторых, такой процесс концентрирования из-за высокой температуры топочных газов приводит к ощутимым потерям серной кислоты от раскисления, сопровождающегося выбросом вредного SO2 в атмосферу;
— неиспользованные возможности экономии энергетических средств.
Парофазная гидратация этилена
Наиболее разработанным применительно к имеющимся промышленным установкам в настоящее время является процесс газофазной гидратации:
CH2 =CH2(г.) + H2 O(г.) = C2 H5 OH(г.) + 41868Дж/моль.
Механизм:
CH2 =CH2 + Н+ « СН3 -СН2+ ,
СН3 -СН2+ + Н2 О « СН3 -СН2 -ОН2+ ,
СН3 -СН2 -ОН2+ « СН3 -СН2 -ОН + Н+ .
Но наряду с основной реакцией идут параллельные и последовательные побочные реакции:
C2 H4 + H2 O = C2 H5 OC2 H5 ,
n(C2 H4 ) = (-CH2 -CH2 -)n .
Таким образом, процесс сложный, обратимый, несмещенный (см. таблицу), экзотермический, протекает с уменьшением объема.
Таб. Равновесный выход этанола.
Следует обратить внимание на два физико-химических фактора, которые определяют основные технологические параметры процесса. Прежде всего, это активность катализатора, которая имеет решающее значение для определения температуры процесса. Катализаторами прямой гидратации могут служить фосфорная кислота и ее соли. Чаще всего используется фосфорная кислота концентрацией 85-87% на таких носителях, как алюмосиликаты, силикагели, пемза и др.; значительная часть кислоты (до 35%) находится в свободном состоянии. Активность этого катализатора является невысокой. Только при температуре 280-3000 С ее можно считать более или менее приемлемой для промышленных условий. При более высокой температуре в значительной мере развиваются побочные процессы: полимеризация этилена, усиленное образование эфира и т.д.
mirznanii.com
