Промышленное получение водорода – Получение водорода
Водород
| Водород | |
|---|---|
| Атомный номер | 1 |
| Внешний вид простого вещества | газ без цвета, вкуса и запаха |
| Свойства атома | |
|
Атомная масса (молярная масса) |
1,00794 а.е.м. (г/моль) |
| Радиус атома | 79 пм |
|
Энергия ионизации (первый электрон) |
1311,3 кДж/моль (эВ) |
| Электронная конфигурация | 1s1 |
|
|
|
| Ковалентный радиус | 32 пм |
| Радиус иона | 54 (−1 e) пм |
|
Электроотрицательность (по Полингу) |
2,20 |
| Электродный потенциал | |
| Степени окисления | 1, −1 |
| Термодинамические свойства простого вещества | |
|
Плотность вещества |
0,0000899 (при 273K (0 °C)) г/см³ |
| Молярная теплоёмкость | 14,235 Дж/(K·моль) |
| Теплопроводность | 0,1815 Вт/(м·K) |
| Температура плавления | 14,01K |
| Теплота плавления | 0,117 кДж/моль |
| Температура кипения | 20,28K |
| Теплота испарения | 0,904 кДж/моль |
| Молярный объём | 14,1 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная |
| Параметры решётки | a=3,780 c=6,167 Å |
| Отношение c/a | 1,631 |
| Температура Дебая | 110 K |
| H | 1 |
|
|
|
| 1s1 | |
| Водород | |
Водород является первым элементом периодической системы элементов. Широко распространён в природе. Катион (и ядро) самого распространённого изотопа водорода 1H— протон. Свойства ядра 1H позволяют широко использовать ЯМР-спектроскопию в анализе органических веществ.
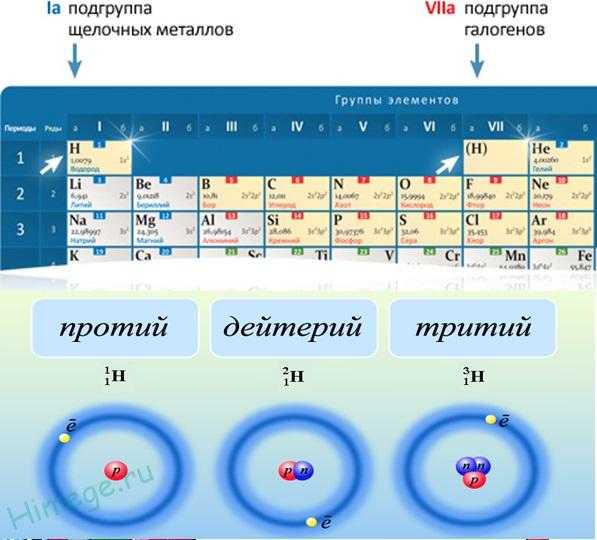
Трое из пяти изотопов водорода имеют собственные названия: 1H— протий (Н), 2H— дейтерий (D) и 3H— тритий (радиоактивен) (T).
Простое вещество водород— H
История водорода
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в XVI и XVII веках на заре становления химии как науки. Прямо указывал на выделение его и М. В. Ломоносов, но уже определённо сознавая, что это не флогистон. Английский физик и химик Г. Кавендиш в 1766 году исследовал этот газ и назвал его «горючим воздухом». При сжигании «горючий воздух» давал воду, но приверженность Кавендиша теории флогистона помешала ему сделать правильные выводы. Французский химик А. Лавуазье совместно с инженером Ж. Менье, используя специальные газометры, в 1783г. осуществил синтез воды, а затем и её анализ, разложив водяной пар раскалённым железом. Таким образом он установил, что «горючий воздух» входит в состав воды и может быть из неё получен.
Происхождение названия водород
Лавуазье дал водороду название hydrogène (отὕδωρ— «вода» и γενναω— «рождаю»)— «рождающий воду». Русское наименование «водород» предложил химик М.Ф.Соловьев в 1824 году— по аналогии с ломоносовским «кислородом».
Распространённость водорода
Во Вселенной
Водород — самый распространённый элемент во Вселенной. На его долю приходится около 92% всех атомов (8% составляют атомы гелия, доля всех остальных вместе взятых элементов — менее 0,1%). Таким образом, водород — основная составная часть звёзд и межзвёздного газа. В условиях звёздных температур (например, температура поверхности Солнца ~6000 °C) водород существует в виде плазмы, в межзвёздном пространстве этот элемент существует в виде отдельных молекул, атомов и ионов и может образовывать молекулярные облака, значительно различающиеся по размерам, плотности и температуре.
Земная кора и живые организмы
Массовая доля водорода в земной коре составляет 1%— это десятый по распространённости элемент. Однако его роль в природе определяется не массой, а числом атомов, доля которых среди остальных элементов составляет 17% (второе место после кислорода, доля атомов которого равна ~52%). Поэтому значение водорода в химических процессах, происходящих на Земле, почти так же велико, как и кислорода. В отличие от кислорода, существующего на Земле и в связанном, и в свободном состояниях, практически весь водород на Земле находится в виде соединений; лишь в очень незначительном количестве водород в виде простого вещества содержится в атмосфере (0,00005% по объёму).
Водород входит в состав практически всех органических веществ и присутствует во всех живых клетках. В живых клетках по числу атомов на водород приходится почти 50%.
Получение Водорода
Промышленные способы получения простых веществ зависят от того, в каком виде соответствующий элемент находится в природе, то есть что может быть сырьём для его получения. Так, кислород, имеющийся в свободном состоянии, получают физическим способом— выделением из жидкого воздуха. Водород же практически весь находится в виде соединений, поэтому для его получения применяют химические методы. В частности, могут быть использованы реакции разложения. Одним из способов получения водорода служит реакция разложения воды электрическим током.
Основной промышленный способ получения водорода— реакция с водой метана, который входит в состав природного газа. Она проводится при высокой температуре (легко убедиться, что при пропускании метана даже через кипящую воду никакой реакции не происходит):
СН4 +2Н2O =CO2↑ +4Н2 −165 кДж
В лаборатории для получения простых веществ используют не обязательно природное сырьё, а выбирают те исходные вещества, из которых легче выделить необходимое вещество. Например, в лаборатории кислород не получают из воздуха. Это же относится и к получению водорода. Один из лабораторных способов получения водорода, который иногда применяется и в промышленности,— разложение воды электротоком.
Обычно в лаборатории водород получают взаимодействием цинка с соляной кислотой.
Получение водорода в промышленности
1.Электролиз водных растворов солей:
2.Пропускание паров воды над раскаленным коксом при температуре около 1000°C:
H2O +C ⇄ H2↑ +CO↑
3.Из природного газа.
Конверсия с водяным паром:
CH4 +H2O ⇄ CO↑ +3H2↑ (1000°C)
Каталитическое окисление кислородом:
2CH4 +O2 ⇄ 2CO↑ +4H2↑
4. Крекинг и риформинг углеводородов в процессе переработки нефти.
Получение водорода в лаборатории
1.Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и разбавленную соляную кислоту:
2.Взаимодействие кальция с водой:|
Ca +2H2O → Ca(OH)2 +H2↑
3.Гидролиз гидридов:
NaH +H2O → NaOH +H2↑
4.Действие щелочей на цинк или алюминий:
2Al +2NaOH +6H2O → 2Na[Al(OH)4] +3H2↑
Zn +2KOH +2H2O → K2[Zn(OH)4] +H2↑
5.С помощью электролиза. При электролизе водных растворов щелочей или кислот на катоде происходит выделение водорода, например:
2H3O+ +2e— → H2↑ +2H
Дополнительная информация про Водород
Биореактор для производства водорода
Физические свойства Водорода
Спектр излучения водорода
Эмиссионный спектр водорода
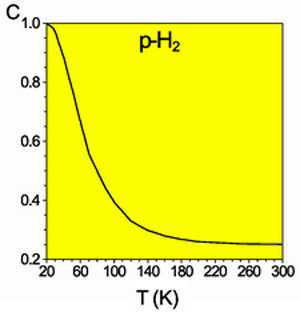
Равновесная мольная концентрация пара-водорода
Разделить модификации водорода можно адсорбцией на активном угле при температуре жидкого азота. При очень низких температурах равновесие между ортоводородом и параводородом почти нацело сдвинуто в сторону последнего. При 80 К соотношение форм приблизительно 1:1. Десорбированный параводород при нагревании превращается в ортоводород вплоть до образования равновесной при комнатной температуре смеси (орто-пара: 75:25). Без катализатора превращение происходит медленно (в условиях межзвездной среды— с характерными временами вплоть до космологических), что даёт возможность изучить свойства отдельных модификаций.
Водород — самый лёгкий газ, он легче воздуха в 14,5 раз. Очевидно, что чем меньше масса молекул, тем выше их скорость при одной и той же температуре. Как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха.
Молекула водорода двухатомна — Н2. При нормальных условиях — это газ без цвета, запаха и вкуса. Плотность 0,08987 г/л (н.у.), температура кипения −252,76 °C, удельная теплота сгорания 120.9·106 Дж/кг, малорастворим в воде — 18,8 мл/л. Водород хорошо растворим во многих металлах (Ni, Pt, Pd и др.), особенно в палладии (850 объёмов на 1объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре.
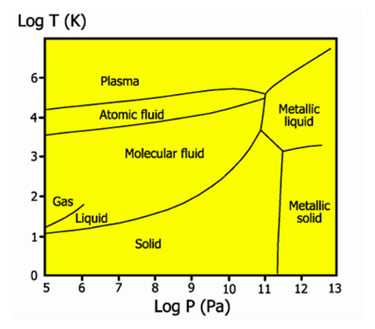
Фазовая диаграмма водорода
Жидкий водород существует в очень узком интервале температур от −252,76 до −259,2 °C. Это бесцветная жидкость, очень лёгкая (плотность при −253 °C 0,0708 г/см3) и текучая (вязкость при −253 °C 13,8 спуаз). Критические параметры водорода очень низкие: температура −240,2 °C и давление 12,8 атм. Этим объясняются трудности при ожижении водорода. В жидком состоянии равновесный водород состоит из 99,79% пара-Н2, 0,21% орто-Н2.
Твердый водород, температура плавления −259,2 °C, плотность 0,0807 г/см3 (при −262 °C) — снегоподобная масса, кристаллы гексогональной сингонии, пространственная группа P6/mmc, параметры ячейки a=3,75 c=6,12. При высоком давлении водород переходит в металлическое состояние.
Изотопы
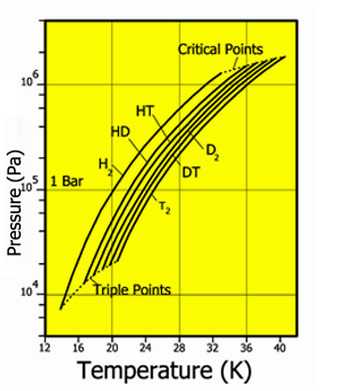
Давление пара для различных изотопов водорода
Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия: 1H— протий (Н), 2Н— дейтерий (D), 3Н— тритий (радиоактивный) (T).
Протий и дейтерий являются стабильными изотопами с массовыми числами 1и 2. Содержание их в природе соответственно составляет 99,9885±0,0070% и 0,0115 ± 0,0070%. Это соотношение может незначительно меняться в зависимости от источника и способа получения водорода.
Изотоп водорода 3Н (тритий) нестабилен. Его период полураспада составляет 12,32 лет. Тритий содержится в природе в очень малых количествах.
В литературе также приводятся данные об изотопах водорода с массовыми числами 4— 7и периодами полураспада 10−22— 10−23 с.
Природный водород состоит из молекул H2 и HD (дейтероводород) в соотношении 3200:1. Содержание чистого дейтерийного водорода D2 ещё меньше. Отношение концентраций HD и D2, примерно, 6400:1.
Из всех изотопов химических элементов физические и химические свойства изотопов водорода отличаются друг от друга наиболее сильно. Это связано с наибольшим относительным изменением масс атомов.
|
Температура плавления, K |
Температура кипения, K |
Тройная точка, K /kPa |
Критическая точка, K /kPa |
Плотность жидкий /газ, кг/м³ |
|
|---|---|---|---|---|---|
| H2 | 13.95 | 20,39 | 13,96 /7,3 | 32,98 /1,31 | 70,811 /1,316 |
| HD | 16,60 | 22,13 | 16,60 /12,8 | 35,91 /1,48 | 114,80 /1,802 |
| HT | 22,92 | 17,63 /17,7 | 37,13 /1,57 | 158,62 /2,310 | |
| D2 | 18,62 | 23,67 | 18,73 /17,1 | 38,35 /1,67 | 162,50 /2,230 |
| DT | 24.38 | 19,71 /19,4 | 39,42 /1,77 | 211,54 /2,694 | |
| T2 | 25,04 | 20,62 /21,6 | 40,44 /1,85 | 260,17 /3,136 |
Дейтерий и тритий также имеют орто- и пара- модификации: p-D2, o-D2, p-T2, o-T2. Гетероизотопный водород (HD, HT, DT) не имеют орто- и пара- модификаций.
Химические свойства
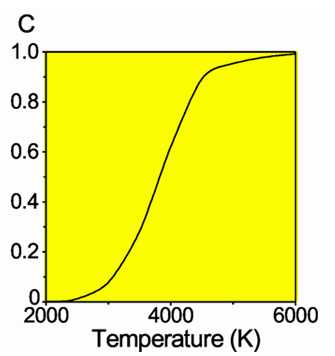
Доля диссоциировавших молекул водорода
Молекулы водорода Н2 довольно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия:
- Н2 =2Н − 432 кДж
Поэтому при обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя гидрид кальция:
- Ca +Н2 =СаН2
и с единственным неметаллом— фтором, образуя фтороводород:
- F2 +H2 =2HF
С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например при освещении:
- О2 +2Н2 =2Н2О
Он может «отнимать» кислород от некоторых оксидов, например:
- CuO +Н2 =Cu +Н2O
Записанное уравнение отражает восстановительные свойства водорода.
- N2 +3H2 → 2NH3
С галогенами образует галогеноводороды:
- F2 +H2 → 2HF, реакция протекает со взрывом в темноте и при любой температуре,
- Cl2 +H2 → 2HCl, реакция протекает со взрывом, только на свету.
С сажей взаимодействует при сильном нагревании:
- C +2H2 → CH4
Взаимодействие со щелочными и щёлочноземельными металлами
При взаимодействии с активными металлами водород образует гидриды:
- 2Na +H2 → 2NaH
- Ca +H2 → CaH2
- Mg +H2 → MgH2
Гидриды— солеобразные, твёрдые вещества, легко гидролизуются:
- CaH2 +2H2O → Ca(OH)2 +2H2↑
Взаимодействие с оксидами металлов (как правило, d-элементов)
Оксиды восстанавливаются до металлов:
- CuO +H2 → Cu +H2O
- Fe2O3 +3H2 → 2Fe +3H2O
- WO3 +3H2 → W+3H2O
Гидрирование органических соединений
Молекулярный водород широко применяется в органическом синтезе для восстановления органических соединений. Эти процессы навзывают реакциями гидрирования. Эти реакции проводят в присутствии катализатора при повышенных давлении и температуре. Катализатор может быть как гомогенным (напр. Катализатор Уилкинсона), так и гетерогенным (напр. никель Ренея, палладий на угле).
Так, в частности, при каталитическом гидрировании ненасыщенных соединений, таких как алкены и алкины, образуются насыщенные соединения — алканы.
Геохимия водорода
На Земле содержание водорода понижено по сравнению с Солнцем, гигантскими планетами и первичными метеоритами, из чего следует, что во время образования Земля была значительно дегазирована и водород вместе с другими летучими элементами покинул планету во время аккреции или вскоре после неё.
Свободный водород H2 относительно редко встречается в земных газах, но в виде воды он принимает исключительно важное участие в геохимических процессах.
В состав минералов водород может входить в виде иона аммония, гидроксил-иона и кристаллической воды.
В атмосфере водород непрерывно образуется в результате разложения воды солнечным излучением. Имея малую массу, молекулы водорода обладают высокой скоростью диффузионного движения (она близка ко второй космической скорости) и, попадая в верхние слои атмосферы, могут улететь в космическое пространство.
Особенности обращения
|
Водород при смеси с воздухом образует взрывоопасную смесь— так называемый гремучий газ. Наибольшую взрывоопасность этот газ имеет при объёмном отношении водорода и кислорода 2:1, или водорода и воздуха приближённо 2:5, так как в воздухе кислорода содержится примерно 21%. Также водород пожароопасен. Жидкий водород при попадании на кожу может вызвать сильное обморожение. Взрывоопасные концентрации водорода с кислородом возникают от 4% до 96% объёмных. При смеси с воздухом от 4% до 75(74)% объёмных. |
Применение водорода
Атомарный водород используется для атомно-водородной сварки.
Химическая промышленность
При производстве аммиака, метанола, мыла и пластмасс
Пищевая промышленность
При производстве маргарина из жидких растительных масел.
Зарегистрирован в качестве пищевой добавки E949 (упаковочный газ)
Авиационная промышленность
Водород очень лёгок и в воздухе всегда поднимается вверх. Когда-то дирижабли и воздушные шары наполняли водородом. Но в 30-х гг. XXв. произошло несколько катастроф, когда дирижабли взрывались и сгорали. В наше время дирижабли наполняют гелием.
Топливо
Водород используют в качестве ракетного топлива. Ведутся исследования по применению водорода как топлива для легковых и грузовых автомобилей. Водородные двигатели не загрязняют окружающей среды и выделяют только водяной пар.
В водородно-кислородных топливных элементах используется водород для непосредственного преобразования энергии химической реакции в электрическую.
Водород, Hydrogenium, Н (1)
Как горючий (воспламеняемый) воздух водород известен довольно давно. Его получали действием кислот на металлы, наблюдали горение и взрывы гремучего газа Парацельс, Бойль, Лемери и другие ученые XVI— XVIII вв. С распространением теории флогистона некоторые химики пытались получить водород в качестве «свободного флогистона». В диссертации Ломоносова «О металлическом блеске» описано получение водорода действием «кислотных спиртов» (например, «соляного спирта», т. е. соляной кислоты) на железо и другие металлы; русский ученый первым (1745) выдвинул гипотезу, о том что водород («горючий пар»— vapor inflammabilis) представляет собой флогистон. Кавендиш, подробно исследовавший свойства водорода, выдвинул подобную же гипотезу в 1766 г. Он называл водород «воспламеняемым воздухом», полученным из «металлов» (Inflammable air from metals), и полагал, как и все флогистики, что при растворении в кислотах металл теряет свой флогистон. Лавуазье, занимавшийся в 1779 г. исследованием состава воды путем ее синтеза и разложения, назвал водород Hydrogine (гидроген), или Hydrogene (гидрожен), от греч. гидор— вода и гайноме— произвожу, рождаю.
Номенклатурная комиссия 1787 г. приняла словопроизводство Hydrogene от геннао, рождаю. В «Таблице простых тел» Лавуазье водород (Hydrogene) упомянут в числе пяти (свет, теплота, кислород, азот, водород) «простых тел, относящихся ко всем трем царствам природы и которые следует рассматривать как элементы тел»; в качестве старых синонимов названия Hydrogene Лавуазье называет горючий газ (Gaz inflammable), основание горючего газа. В русской химической литературе конца XVIII и начала XIX в. встречаются два рода названий водорода: флогистические (горючий газ, горючий воздух, воспламенительный воздух, загораемый воздух) и антифлогистические (водотвор, водотворное существо, водотворный гас, водородный гас, водород). Обе группы слов представляют собой переводы французских названий водорода.
Изотопы водорода были открыты в 30-x годах текущего столетия и быстро приобрели большое значение в науке и технике. В конце 1931 г. Юри, Брекуэдд и Мэрфи исследовали остаток после длительного выпаривания жидкого водорода и обнаружили в нем тяжелый водород с атомным весом 2. Этот изотоп назвали дейтерием (Deuterium, D) от греч.— другой, второй. Спустя четыре года в воде, подвергнутой длительному электролизу, был обнаружен еще более тяжелый изотоп водорода 3Н, который назвали тритием (Tritium, Т), от греч.— третий.
himsnab-spb.ru
Водород. Физические и химические свойства, получение » HimEge.ru
 Водород H — самый распространённый элемент во Вселенной (около 75 % по массе), на Земле — девятый по распространенности. Наиболее важным природным соединением водорода является вода.
Водород H — самый распространённый элемент во Вселенной (около 75 % по массе), на Земле — девятый по распространенности. Наиболее важным природным соединением водорода является вода.
Водород занимает первое место в периодической системе (Z = 1). Он имеет простейшее строение атома: ядро атома – 1 протон, окружено электронным облаком, состоящим из 1 электрона.
В одних условиях водород проявляет металлические свойства (отдает электрон), в других — неметаллические (принимает электрон).
В природе встречаются изотопы водорода: 1Н — протий (ядро состоит из одного протона), 2Н — дейтерий (D — ядро состоит из одного протона и одного нейтрона), 3Н — тритий (Т — ядро состоит из одного протона и двух нейтронов).
Простое вещество водород
Молекула водорода состоит из двух атомов, связанных между собой ковалентной неполярной связью.
Физические свойства. Водород — бесцветный нетоксичный газ без запаха и вкуса. Молекула водорода не полярна. Поэтому силы межмолекулярного взаимодействия в газообразном водороде малы. Это проявляется в низких температурах кипения (-252,6 0С) и плавления (-259,2 0С).
Водород легче воздуха, D (по воздуху) = 0,069; незначительно растворяется в воде (в 100 объемах h3O растворяется 2 объема h3). Поэтому водород при его получении в лаборатории можно собирать методами вытеснения воздуха или воды.
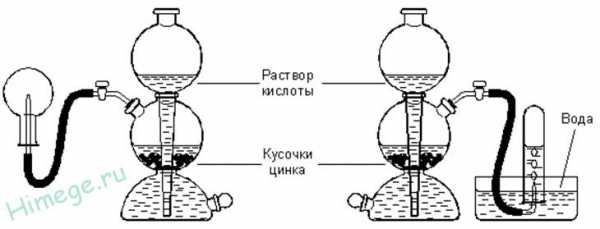
Получение водорода
В лаборатории:
1.Действие разбавленных кислот на металлы:
Zn +2HCl → ZnCl2 +H2↑
2.Взаимодействие щелочных и щ-з металлов с водой:
Ca +2H2O → Ca(OH)2 +H2↑
3.Гидролиз гидридов: гидриды металлов легко разлагаются водой с образованием соответствующей щелочи и водорода:
NaH +H2O → NaOH +H2↑
СаH2 + 2Н2О = Са(ОН)2 + 2Н2↑
4.Действие щелочей на цинк или алюминий или кремний:
2Al +2NaOH +6H2O → 2Na[Al(OH)4] +3H2↑
Zn +2KOH +2H2O → K2[Zn(OH)4] +H2↑
Si + 2NaOH + H2O → Na2SiO3 + 2H2
5. Электролиз воды. Для увеличения электрической проводимости воды к ней добавляют электролит, например NаОН, Н2SO4 или Na2SO4. На катоде образуется 2 объема водорода, на аноде — 1 объем кислорода.
2H2O → 2H2+О2
Промышленное получение водорода
1. Конверсия метана с водяным паром, Ni 800 °С (самый дешевый):
CH4 + H2O → CO + 3 H2
CO + H2O → CO2 + H2
В сумме:
CH4 + 2 H2O → 4 H2 + CO2
2. Пары воды через раскаленный кокс при 1000оС:
С + H2O → CO + H2
CO +H2O → CO2 + H2
Образующийся оксид углерода (IV) поглощается водой, этим способом получают 50 % промышленного водорода.
3. Нагреванием метана до 350°С в присутствии железного или никелевого катализатора:
СH4 → С + 2Н2↑
4. Электролизом водных растворов KCl или NaCl, как побочный продукт:
2Н2О + 2NaCl→ Cl2↑ + H2↑ + 2NaOH
Химические свойства водорода
- В соединениях водород всегда одновалентен. Для него характерна степень окисления +1, но в гидридах металлов она равна -1.
- Молекула водорода состоит из двух атомов. Возникновение связи между ними объясняется образованием обобщенной пары электронов Н:Н или Н2
- Благодаря этому обобщению электронов молекула Н2 более энергетически устойчива, чем его отдельные атомы. Чтобы разорвать в 1 моль водорода молекулы на атомы, необходимо затратить энергию 436 кДж: Н2 = 2Н, ∆H° = 436 кДж/моль
- Этим объясняется сравнительно небольшая активность молекулярного водорода при обычной температуре.
- Со многими неметаллами водород образует газообразные соединения типа RН4, RН3, RН2, RН.
1) С галогенами образует галогеноводороды:
Н2 + Cl2 → 2НСl.
При этом с фтором — взрывается, с хлором и бромом реагирует лишь при освещении или нагревании, а с йодом только при нагревании.
2) С кислородом:
2Н2 + О2 → 2Н2О
с выделением тепла. При обычных температурах реакция протекает медленно, выше 550°С — со взрывом. Смесь 2 объемов Н2 и 1 объема О2 называется гремучим газом.
3) При нагревании энергично реагирует с серойь(значительно труднее с селеном и теллуром):
Н2 + S → H2S (сероводород),
4) С азотом с образованием аммиака лишь на катализаторе и при повышенных температурах и давлениях:
ЗН2 + N2 → 2NН3
5) С углеродом при высоких температурах:
2Н2 + С → СН4 (метан)
6) С щелочными и щелочноземельными металлами образует гидриды (водород – окислитель):
Н2 + 2Li → 2LiH
в гидридах металлов ион водорода заряжен отрицательно (степень окисления -1), то есть гидрид Na+H— построен подобно хлориду Na+Cl—
Со сложными веществами:
7) С оксидами металлов (используется для восстановления металлов):
CuO + H2 → Cu + H2O
Fe3O4 + 4H2 → 3Fe + 4Н2О
8) с оксидом углерода (II):
CO + 2H2 → CH3OH
Синтез — газ (смесь водорода и угарного газа) имеет важное практическое значение, тк в зависимости от температуры, давления и катализатора образуются различные органические соединения, например НСНО, СН3ОН и другие.
9)Ненасыщенные углеводороды реагируют с водородом, переходя в насыщенные:
СnН2n + Н2 → СnН2n+2.

himege.ru
Промышленные способы получения водорода.
Стр 1 из 9Следующая ⇒
Вторая стадия конверсии метана.
Поскольку полученный водород в дальнейшем пойдет в производствр аммиака, вторым окислителем служит кислород.
СН4 +0,5О2 = СО + 2Н2 +Q (1.2.)
Характеристика процесса: простой, обратимый, экзотермический, гетерогенно-каталитический.
Процесс конверсии метана кислородом проводят на никелевом катализаторе пари температуре 900-10000С.
В схемах с двухступенчатой конверсией метана сначала протекает экзотермическая реакция с кислородом. Затем, по мере повышения температуры, начинает идти реакция (1.1.) с паром, так как в газовой смеси содержание пара велико (первая стадия конверсии проводится с большим избытком пара).
В результате процесса необходимо достичь высокой степени конверсии метана, чтобы остаточное его содержание не превышало 0,5%.
Конверсия оксида углерода.
Конверсия оксида углерода протекает по следующей реакции:
СО + Н2О = Н2 + СО2 + Q (1.5.)
Характеристика реакции: сложная, экзотермическая, обратимая, гетерогенно-каталитическая.
Помимо основной, протекает побочная реакция разложения оксида углерода:
2СО = С + СО2 (9.6.)
В соответствии с условиями термодинамического равновесия повысить степень конверсии СО можно удалением диоксида углерода из газовой смеси, увеличением содержания водяного пара или проведением процесса при возможно низкой температуре. Конверсия оксида углерода, как видно из уравнения реакции, протекает без изменения объема, поэтому повышение давления не вызывает смещения равновесия. Вместе с тем проведение процесса при повышенном давлении оказывается экономически целесообразным (см. преимущества повышенного давления).
Концентрация водяного пара в газе обычно определяется количеством, дозируемым на конверсию метана и оставшимся после ее протекания.
Соотношение пар : газ перед конверсией СО в крупных агрегатах производства аммиака составляет 0,4-0,5.
Проведение процесса при низких температурах – рациональный путь повышения равновесной степени превращения СО, но возможный только при наличие высокоактивных катализаторов.
В случае проведения процесса под давлением 2-3 МПа нижний температурный предел составляет 180-2000С. Снижение температуры ниже точки росы вызывает конденсацию влаги, что нежелательно.
Реакция конверсии СО сильно экзотермична, т.е. идет с выделением значительного количества тепла. Это вызвало необходимость проведения процесса в два этапа при разных температурных режимах.
Температурный режим на каждой стадии конверсии определяется свойствами применяемых катализаторов.
На первой ступени используется железохромовый катализатор, который выпускается в таблетированном и формованном видах и является активным в области температур 450-5000С. Для железохромового катализатора ядами являются сернистые соединения, соединения фосфора, бора, кремния, хлора.
На высокотемпературном железохромовом катализаторе обеспечивается высокая скорость конверсии СО.
Низкотемпературные катализаторы содержат с своем составе соединения цинка, меди, хрома. На поверхности этого катализатора процесс конверсии проводят в пределах 200-2500С и получают высокую степень конверсии СО.
Срок службы низкотемпературных катализаторов обычно не превышает двух лет. Одной из причин их дезактивации является рекристаллизация под действием температуры и реакционной среды. При конденсации влаги на катализаторе происходит снижение его механической прочности и активности.
Глава 2.
Производство аммиака.
Аммиак – ключевой продукт различных азотсодержащих веществ, применяемых в промышленности и сельском хозяйстве.
Области применения: в производстве азотной кислоты, карбамида, взрывчатых веществ, минеральных удобрений, красителей, полимерных материалов и т.д.
Синтез аммиака из элементов осуществляется по уравнению реакции:
N2 + 3H2↔ 2NH3 + Q (2.1.)
Реакция обратимая, экзотермическая, характеризуется большим отрицательным энтальпийным эффектом (ΔН298 = — 91,96 кДж/моль) и при высоких температурах становится еще более экзотермической. Изменении энтропии в данном случае тоже отрицательно ( ΔS0298 =-198,13 кДж/моль.К) и не благоприятствует протеканию реакции. При отрицательном значении ΔS0 повышение температуры уменьшает вероятность протекания реакции, так как при этом ΔG0 становится все более положительной величиной.
Поэтому, чем выше температура, тем менее термодинамически вероятным будет процесс.
Поскольку процесс синтеза аммиака является обратимым, экзотермическим и идет с уменьшением числа молей, для смещения равновесия вправо необходимо снижать температуру и увеличивать давление.
Синтез аммиака не идет в газовой фазе даже при очень высоких температурах из-за высокой энергии активации. Для ее снижения процесс необходимо проводить на поверхности катализатора.
Наибольшей каталитической активностью обладают Fe, Os, W, Pt, Ru. В промышленности нашли применения железные катализаторы, получаемые сплавлением оксидов железа с активаторами (промоторами) и последующим восстановлением оксидов железа. В качестве активаторов применяют Al2O3 и K2O для уменьшения роста кристаллов железа и для облегчения диффузии образовавшегося аммиака с поверхности катализатора соответственно.
Катализатор из активированного железа необратимо отравляется сернистыми соединениями и обратимо –кислородосодержащими соединениями. Поэтому перед синтезом свежая АВС подвергается тщательной очистке.
Таким образом, процесс является гетерогенно-каталитическим. Лимитирующая стадия – хемсорбция азота на поверхности катализатора.
N2 + Z = ZN2 (2.2.)
ZN2 +3H2 = 2NH3 + Z (2.3.), где Z – свободный центр поверхности катализатора.
Так как синтез аммиака идет в кинетической области, то для увеличения скорости процесса необходимо увеличивать температуру.
Катализатор –активированное железо, работает в узком температурном интервале 420-5000С, что и будет определять температуру синтеза.
Выбор давления.
Осуществляются три режима работы:
1). Низкое 10-20 МПа
2) Среднее 28-35 МПа
3) Высокое 45 –100 МПа.
Установки низкого давления применяются редко, из-за их малой экономичности и сложности схемы.
Преимущества аппаратов высокого давления: увеличивается концентрация аммиака в газе, растет производительность установок, проще схема. Однако, наряду с позитивными моментами, существуют и недостатки: увеличивается концентрация инертных примесей, большой расход электроэнергии, уменьшается срок службы катализатора.
Большинство установок в промышленности работают при среднем давлении – 30 – 32 МПа.
Повышение давления оказывает положительное влияние как на выход, так и на скорость процесса, так как скорость прямой реакции зависит от давления в степени 1,5, а скорость обратной реакции – в степени 0,5.
Выбор соотношения исходных компонентов.
Так как процесс синтеза аммиака является обратимым несмещенным, то избыток компонента не сможет существенно сместить равновесие реакции. И с другой стороны, лимитирующая стадия – хемсорбция азота, поэтому для увеличения скорости процесса он должен быть выбран, как реагент, используемый в избытке. А это приведет к накоплению инертов и снижению давления в системе, что в свою очередь снизит выход и скорость процесса.
Таким образом, целесообразно поддерживать стехиометрическое соотношение исходных компонентов, т.е. N2 :H2=1:3
Для увеличения степени использования сырья процесс проводят по циркуляционной схеме вдали от положения равновесия с большими объемными скоростями. Повышение объемной скорости приводит к снижению выхода аммиака, но в целом ведет к увеличению интенсивности процесса.
Для предотвращения накопления инертов в циркуляционном газе проводят отдувку – часть циркуляционного газа выбрасывают в атмосферу с таким расчетом, чтобы количество инертов, поступающих со свежим газом, было равно количеству инертов, удаляемых из системы отдувкой.
Для разрешения противоречия между выходом и скоростью, процесс проводят по линии оптимальных температур. Для этого в колонне синтеза предусмотрена подача холодного байпасного газа после каждого слоя катализатора.
Технологическое оформление процесса синтеза аммиака.
В современных агрегатах синтеза аммиака большой единичной мощности процесс ведут на плавленых железных катализаторах при температурах 420-5000С, давлении 25-32 МПа, объемной скорости 15-20 тыс.ч-1.
На рис. 2.1. представлена упрощенная технологическая схема синтеза аммиака.
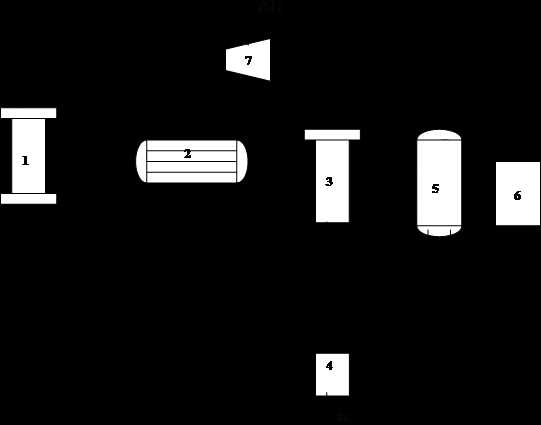
2.1.Упрощенная технологическая схема синтеза аммиака:
1 –колонна синтеза, 2 –теплообменник, 3 –сепаратор, 4 –сборник жидкого аммиака, 5 –конденсационная колонна, 6 –испаритель, 7 –компрессор.
Газообразная азото-водородная смесь поступает в компрессор (7) и сжимается до 30 МПа. Затем поступает в колонну синтеза (1), где при температуре 450—5000С идет реакция (2.1.). Из колонны синтеза выходит смесь, содержащая: азот, водород и аммиак.
Дальнейшие действия необходимо направить на отделение образовавшегося аммиака от непрореагировавшей азото-водородной смеси. Это можно сделать, превратив аммиак в жидкость.
Поэтому смесь направляют в теплообменник (2), где она охлаждается.
В сепараторе (3) жидкий аммиак отделяется и поступает в сборник жидкого аммиака (4).
Газообразная смесь: H2, N2, NH3 проходит конденсационную колонну (5) и поступает в испаритель жидкого аммиака (6). В межтрубном пространстве испарителя кипит автономный жидкий аммиак при температуре –50С. Газообразная смесь в испарителе охлаждается, в результате чего весь газообразный аммиак превращается в жидкий. Для отделения жидкого аммиака от непрореагировавшего азота и водорода смесь возвращают в нижнюю часть конденсационной колонны (5), где расположено сепарационное устройство. Жидкий аммиак отделяется и стекает в сборник жидкого аммиака (4). Непрореагировавшая азото-водородная смесь идет на рециркуляцию.
Для поддержания в циркуляционном газе постоянного содержания инертов производится отдувка. Часть циркуляционного газа выбрасывается в атмосферу с таким расчетом, чтобы количество инертных примесей, поступающее со свежим газом, было равно количеству инертов, удаляемых из системы отдувкой.
На рис. (2.2) и (2.3.) представлены основные аппараты технологической схемы синтеза аммиака.
Оборудование агрегата.
Колонна синтеза. В агрегатах мощностью 1360 т/сут получили распространение аксиальные четырехполочные насадки с предварительным теплообменником и трехполочные с выносным теплообменником. На рис.2.2. показана четырехполочная колонна с аксиальными насадками.
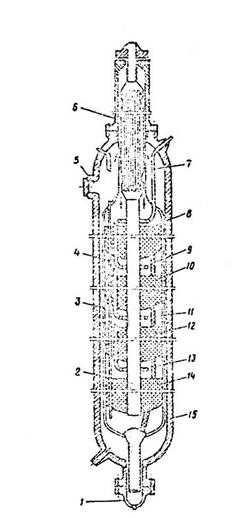 Рис.2.2. Четырехполочная колонна синтеза аммиака:
Рис.2.2. Четырехполочная колонна синтеза аммиака:
1 –люк для выгрузки катализатора, 2 –центральная труба, 3 –корпус катализаторной коробки, 4 –термопарный чехол, 5 –загрузочный люк, 6 –теплообменник, 7, 9, 11, 13 –ввод байпасного газа, 15 –корпус колонны.
Основной поток газа поступает в колонну снизу, проходит по кольцевой щели между корпусом колонны 15 и кожухом катализаторной коробки 3 и поступает в межтрубное пространство теплообменника 6. Здесь синтез газ нагревается конвертированным газом до 420-4400С и проходит последовательно четыре слоя катализатора 8, 10, 12, 14, между которыми подается холодный байпасный газ. После четвертого слоя катализатора газовая смесь при 500-5150С поднимается по центральной трубе 2, проходит по трубкам теплообменника 6, охлаждаясь при этом до 320-3500С, и выходит из колонны.
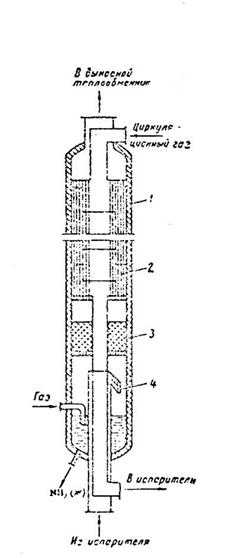 Конденсационная колонна. (Рис.2.3.). Представляет собой вертикальный цилиндрический аппарат, состоит из теплообменника и сепаратора, размещенного под теплообменником. Охлаждаемый газ идет по межтрубному пространству теплообменника, а газ после сепарации аммиака – по трубам.
Конденсационная колонна. (Рис.2.3.). Представляет собой вертикальный цилиндрический аппарат, состоит из теплообменника и сепаратора, размещенного под теплообменником. Охлаждаемый газ идет по межтрубному пространству теплообменника, а газ после сепарации аммиака – по трубам.
Рис.2.3. Конденсационная колонна:
1 –корпус, 2- теплообменник, 3 –отбойник, 4 –сепарационное устройство.
Газ, охлажденный в испарителе, через нижний штуцер поступает в сепарационное устройство 4, в котором создается вращательное движение, при этом частицы жидкости отделяются от газового потока, собираются в нижней части аппарата и непрерывно выводятся. Газ поднимается вверх, проходит отбойник 3 и, проходя трубное пространство, отдает свой холод. Свежий газ, входящий через боковой штуцер в нижней части аппарата, барботирует через слой жидкого аммиака, освобождаясь от паров воды и СО2
Катализатор.
Реакция (11.1) в объеме не идет даже при высоких температурах из-за большой величины энергии активации. Для реализации этой реакции необходимы катализаторы, активно адсорбирующие кислород. В промышленности чаще всего применяют платиново-родиевые катализаторы. Окисление аммиака на этих катализаторах протекает очень быстро, время контактирования – 10-4 сек, выход при этом составляет 98%.
Неплатиновые катализаторы, состоящие из оксидов железа и хрома, также дают высокие выходы (около 96%), но скорость реакции уменьшается в 100 раз.
Таким образом, процесс окисления аммиака до оксида азота (II) является гетерогенно-каталитическим, идет во внешнедиффузионной области. Лимитирующая стадия – диффузия аммиака к поверхности катализатора.
Помимо активности, катализатор должен обладать селективностью, так как состав конечных продуктов будет определяться соотношением скоростей реакций 3.1 – 3.3.
Температура.
На платиновом катализаторе зависимость выхода NO от температуры имеет максимум, рис. 3.1.
Рис. 3.1. Зависимость практического выхода оксида азота (II) от темепартуры:
1 –при давлении 0,1 МПа, 2 –п 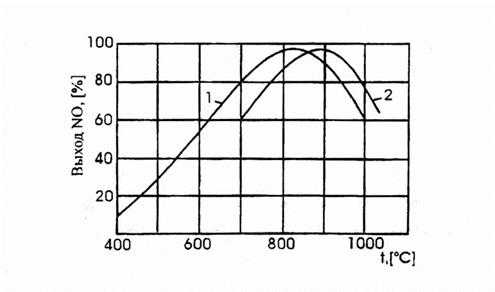
ри давлении 0,8 МПа.
Такой характер кривой определяется влиянием температуры на возможность протекания побочных реакций.
При низких температурах, примерно до 5000С, когда количество адсорбированного кислорода сравнительно невелико, окисление аммиака протекает в основном с образованием элементарного азота. С повышением температуры до 700-8000С выход NO возрастает, так как увеличивается доля активных центров катализатора, занятых кислородом, и растет скорость диффузии исходных веществ к поверхности катализатора. При дальнейшем повышении температуры происходит десорбция кислорода и резко возрастают скорости побочных реакций.
Давление.
Давление в процессе окисления аммиака связано с температурой. Чем выше давление, тем требуется более высокая температура для достижения одного и того же выхода (рис.11.1.).
Проведение процесса под давлением имеет ряд преимуществ: повышается скорость процесса, увеличивается интенсивность катализатора, значительно возрастает скорость реакции:
NO +0,5O2 =NO2 (3.6.),
которая является лимитирующей в производстве азотной кислоты.
В промышленности процесс окисления аммиака до оксида азота (II) проводят при давлении – 0,8 МПа.
4. Соотношение исходных компонентов.
При стехиометрическом соотношении кислорода к аммиаку равном 1,25 в смеси будет содержаться 14,4 об.% аммиака, что соответствует области взрывоопасных концентраций. Кроме этого, при таком соотношении часть активных центров катализатора не заполняется кислородом, что будет способствовать протеканию побочных реакций с образованием элементарного азота.
Глава 4
Глава 5.
Глава 6.
Глава 7.
Производство метанола.
Метанол по значению и объемам производства является одним из важнейших многотоннажных продуктов, выпускаемых современной химической промышленностью.
Области применения: для получения пластических масс, синтетических волокон, синтетического каучука, в качестве растворителя, для микробиологического синтеза и т.д.
Метанол впервые был обнаружен Р. Бойлем в 1661 году в продуктах сухой перегонки древесины (отсюда название метанола – древесный спирт). В чистом виде выделен в 18344 году Ж. Дюма и Э. Пелиго, установившими его формулу.
Промышленное производство метанола из водорода и оксида угдерода (II) впервые было осуществлено в 1923 году и с тех пор непрерывно совершенствуется.
В нашей стране производство метанола впервые организовано в 1934 году в объеме 30 т в сутки на Новомосковском химическом комбинате из водяного газа газификацией кокса.
В качестве сырья для получения метанола могут использоваться: природный газ, синтез-газ производства ацетилена, газы нефтепереработки, твердое топливо.
Твердое топливо сохраняет в качестве сырья определенное значение. Разработка процесса газификации угля с целью получения синтез-газа, содержащего Н2, СО, СО2, может изменить структуру сырьевой базы производства метанола, и неудобный для транспортировки уголь будет превращен в удобный для хранения, транспортировки и использования метанол.
Синтез метанола основан на обратимых реакциях, описываемых уравнениями:
СО + 2Н2 СН3ОН; ΔH = -90,8 кДж (7.4.)
СО2 +3Н2 СН3ОН + Н2О; ΔH = -49,6 кДж (7.5.)
Реакции (5.4.) и (5.5.) – обратимы, экзотермичны и протекают с уменьшением объема.
С термодинамической точки зрения для смещения равновесия в сторону образования метанола необходимо проводить процесс при низких температурах и высоком давлении. Однако, для увеличения скорости реакции необходимо повышение температуры. При этом выбирая температурный режим, следует учитывать образование побочных продуктов: метана, высших спиртов, кетонов и эфиров.
Приведем некоторые побочные реакции:
СО + 3Н2 = СН4 + Н2О (7.6.)
2СО + 4Н2 = (СН3)2О + Н2О (7.7.)
4СО + 8Н2 = С4Н9ОН + 3Н2О (7.8.)
2СО = СО2 + С (7.9.)
т.е. процесс получения метанола является сложным.
Побочные реакции обуславливают бесполезный расход синтез-газа и удорожают очистку метанола.
Применяемый для синтеза метанола катализатор должен обладать высокой селективностью, т.е. максимально ускорять образование метанола при одновременном подавлении побочных реакций. Для синтеза метанола предложено много катализаторов. Лучшими оказались катализаторы, основными компонентами которых являются оксид цинка или медь.
Катализаторы синтеза метанола весьма чувствительны к каталитическим ядам, поэтому первой стадией процесса является очистка газа от сернистых соединений. Сернистые соединения отравляют цинк-хромовые катализаторы обратимо, а медьсодержащие катализаторы – необратимо. Необходима также тщательная очистка газа от карбонила железа, который образуется в результате взаимодействия оксида углерода с железом аппаратуры. На катализаторе карбонил железа разлагается с выделением элементного железа, что способствует образованию метана.
Процесс получения метанола осуществляется либо на цинк-хромовом катализаторе при давлении 30 МПа, либо на низкотемпературном медьсодержащем катализаторе при давлении 5 МПа.
Цинк-хромовый катализатор работает в области температур 370-3900С, медьсодержащий – 220-2800С.
Таким образом, процесс получения метанола является гетерогенно-каталитическим. Лимитирующая стадия – адсорбция водорода на поверхности катализатора.
Для смещения равновесия реакции вправо процесс проводят с избытком водорода, при следующем соотношении исходных компонентов- Н2: СО= 2,15-2,30. Кроме того, водород ускоряет процесс, обладая высокой теплопроводностью, позволяет проводить процесс в узком температурном интервале, гидрирует продукты уплотнения на катализаторе, чем повышает срок его службы.
С возрастанием объемной скорости газа выход метанола падает. Такая закономерность основана на том, что с увеличением объемной скорости уменьшается время контакта газа с катализатором и, следовательно, концентрация метанола в газе, выходящем из реактора.
С увеличением объемной скорости подачи сырья содержание метанола в газе снижается, однако за счет большего объема газа, проходящего в единицу времени через тот же объем катализатора, производительность последнего увеличивается. На практике процесс синтеза метанола осуществляют при объемных скоростях 20 000-40 000 ч-1. Степень превращения СО за проход составляет 15-50%, при этом в контактных газах содержится только –4% метанола.
С целью возможно более полной переработки синтез-газа необходимо его возвращение в цикл после выделения метанола и воды.
При циркуляции в синтез-газе накапливаются инертные примеси, что приводит к снижению давления в системе и повлечет за собой снижение выхода и скорости процесса. Поэтому концентрацию инертных примесей регулируют частичной отдувкой циркуляционного газа. Отдувка проводится с таким расчетом, чтобы количество инертов, поступающих со свежем синтез-газом, было равно количеству инертов, удаляемых с отдувкой.
Глава 8.
Глава 9.
Производство этилбензола.
Области применения этилбензола: используется в производстве стирола, важного сырья для получения ряда полимеров, полистерола, применяемого в автомобилестроении, электро-радиотехнической промышленности, при изготовлении бытовых товаров и упаковок, при производстве ионообменных смол- катализаторов процесса получения кислородсодержащих добавок при производстве реформулированных бензинов и т.д.
В промышленности этилбензол получают взаимодействием бензола с этиленом:
C6H6 + C2H4 = C6H5C2H5 (9.1.)
Одновременно с основной протекает ряд побочных реакций. Наибольшее значение имеют реакции последовательного алкилирования:
C6H5C2H5 + C2H4 = C6H4(C2H5)2 (9.2.)
C6H4(C2H5)2 + C2H4 = C6H3(C2H5)3 (9.3.)
C6H3(C2H5)3 + C2H4 = C6H2(C2H5)4 (9.4.)
Для подавления побочных реакций (2-4) процесс проводят в избытке бензола (мольное отношение этилен:бензол = 0,4:1), при температуре около 1000С и давлении – 0,15 МПа.
Для ускорения основной реакции (1) процесс проводят в присутствии селективного катализатора. В качестве катализатора используют комплексное соединение AlCl3 и HCl с ароматическими углеводородами, который находится в жидкой фазе.
Процесс гетерогенно-каталитический, лимитирующая стадия:
диффузия этилена через пограничную пленку каталитического комплекса хлорида алюминия. Реакция алкилирования идет очень быстро.
При выбранных условиях конверсия этилена составляет 98-100%, основная реакция (1) –необратима, экзотермична.
Для увеличения степени использования сырья организован рецикл по бензолу.
Катализатор на основе хлорида алюминия способствует протеканию реакции переалкилирования диэтилбензола:
C6H4(C2H5)2 + C6H6 = 2C6H5C2H5 (9.5.)
Поэтому небольшие количества диэтилбензола возвращают в реактор-алкилатор на переалкилирование.
Реакция переалкилирования способствует практически полному превращению этилена и бензола в этилбензол.
На процессы алкилирования и переалкилирования оказывают влияния следующие главные факторы: концентрация катализатора (хлористый алюминий), промотора (соляная кислота), температура, время контактирования, мольное соотношение этилена и бензола, давление.
Список литературы.
1. Кутепов А.М., Бондарева Т.И., Беренгартен М.Г. Общая химическая технология. Учебник для вузов, — М.: ИКЦ “Академкнига”, 2002, 560 с.
2. Ксензенко В.И. Общая химическая технология и основы промышленной экологии. Учебник для вузов. – М.: “КолосС”, 2003, 328 с.
3. Соколов Р.С. Химическая технология. В двух томах. Учебное пособие для вузов, — М.: ГИЦ “Владос” , 2000, т.1- 367 с., т.2 – 449 с.
4. Кутепов А.М., Бондарева Т.И., Беренгартен М.Г., Общая химическая технология. Учебник для вузов, — М.: ИКЦ “Академкнига”, 2005, 524 с.
5. Баранов Д.А., Кутепов А.М. Процессы и аппараты. Учебник для студентов образовательных учреждений среднего профессионального образования. – М.: Академа, 2005, 302 с.
Содержание.
Стр.
Глава 1. Производство водорода……………………… 3……….
Глава 2. Производство аммиака…………………………16……..
Глава 3. Производство азотной кислоты…………… …24……
Глава 4. Производство серной кислоты из серы……… 37….
Глава 5. Производство аммиачной селитры……………48…….
Глава 6. Производство этанола………………………… 54…….
Глава 7. Производство метанола…………………… …57…….
Глава 8. Производство уксусной кислоты………………65…….
Глава 9. Производство этилбензола……………… ……68….
Список литературы…………………………… …………77.
Промышленные способы получения водорода.
1). Физический – извлечение водорода из коксового газа методом глубокого охлаждения фракционно-термическая конденсация).
2). Электрохимический метод – электролиз воды. Чистота получаемого водорода – 99,8%. Недостаток метода – большой расход электроэнергии.
3). Химический метод – конверсия углеводородных газов. В качестве исходного сырья применяются: углеводородный газ –метан или углеводороды бензиновой фракции нефти.
Конверсия метана – это окисление метана при высокой температуре кислородом или кислородосодержащими соединениями: Н2О или СО2.
По используемому окислителю и технологическому оформлению можно выделить следующие варианты процесса получения водорода: каталитическая парокислородная конверсия, высокотемпературная кислородная конверсия, каталитическая пароуглекислотная конверсия.
Окисление метана при получении синтез-газа протекает по следующим основным суммарным реакциям:
СН4 + Н2О СО +3Н2 -Q (1.1.)
СН4 + 0,5О2 = СО + 2Н2 + Q (1.2.)
СН4 + СО2 2СО + 2Н2 -Q (1.3.)
В реальных условиях ведения процесса реакции 1.1. и 1.3. являются обратимыми и эндотермическими, реакция 1.2. – необратимая и экзотермическая.
Первая ступень конверсии метана.
СН4 + Н2О СО + 3Н2 — Q (1.1.)
Помимо основной реакции возможно протекание побочной реакции разложения метана при температуре около 9500С:
СН4 = С + 2Н2 (1.4.)
Реакция (1.1.) в газовой фазе идет медленно (Е=62,2 кКал/моль). Для ее ускорения процесс проводят гетерогенно на поверхности твердого никелевого катализатора. Никель напыляет ся на твердый носитель Al2O3 или MgO. Катализатор изготавливается в виде гранул, таблеток или колец и состоит из пористого носителя и активного компонента. Наличие катализатора позволяет не только увеличить скорость основной реакции, но и при соответствующем избытке окислителей исключить протекание побочной реакции.
Срок службы катализаторов конверсии при правильной эксплуатации достигает трех лет и более. Их активность снижается при действии различных каталитических ядов. Никелевые катализаторы наиболее чувствительны к действию сернистых соединений. Отравление происходит вследствие образования на поверхности катализатора сульфидов никеля, совершенно неактивных по отношению к реакции конверсии метана. Отравленный серой катализатор удается почти полностью регенерировать в определенных температурных условиях при подаче в реактор чистого газа. Активность зауглероженного катализатора можно восстановить, обрабатывая его водяным паром. Поэтому перед конвектором метана газ подвергают сероочистке.
Никелевый катализатор работает в широком температурном интервале 600-10000С.
Выбор температуры.
С увеличением температуры увеличивается выход, но чем выше температура, тем больше затраты электроэнергии, выше требования к термической устойчивости материалов, и, соответственно, становится более дорогой аппаратура.
Так как часть метана конвертируется во второй ступени воздухом, реакцию (1.1.) не нужно доводить до конца. Поэтому оптимальная температура процесса определяется не условиями равновесия, а кинетикой реакции.
Кроме того, следует отметить, что при температуре 9500С начинает интенсивно проходить побочная реакция разложения метана с образованием сажи. Теряется активность катализатора.
Поэтому, наиболее оптимальной температурой проведения первой стадии конверсии метана является 8000С. В первой стадии конвертируется около 90% метана.
Выбор давления.
Для смещения равновесия в сторону образования продуктов необходимо давление снижать, так как процесс идет с увеличением числа молей. Однако, на практике процесс конверсии метана проводят при давлении 4 МПа. Отрицательное действие давления на выход компенсируют повышенной температурой и избытком водяного пара.
Преимущества повышенного давления:
1). Поскольку последующие процессы, в которых используют водород, ( производство аммиака и метанола) протекают при высоком давлении (30 МПа), то повышение давления при конверсии метана в целом позволяет снизить затраты на компримирование.
2). При повышенном давлении увеличивается скорость реакции, растет производительность.
3). Снижаются капитальные затраты на строительство водородной установки ( уменьшается объем водородной установки, объем трубопроводов, число компрессоров). Используется магистральное давление трубопроводов.
4). При повышенном давлении улучшается возможность использования скрытой теплоты водяного пара.
5). Улучшается очистка от СО2.
Выбор соотношения исходных компонентов.
Процесс конверсии метана проводят с избытком водяного пара. Избыток водяного пара выбирают с таким расчетом, чтобы скомпенсировать высокое давление, а также необходимостью его для последующего процесса конверсии СО.
Н2О/СН4 = (2-4)/1
Рекомендуемые страницы:
lektsia.com
|
www.wewees.ru
Производство водорода — Википедия. Что такое Производство водорода
Электролизёр — оборудование для производства водорода из водыПромышленное производство водорода — неотъемлемая часть водородной энергетики, первое звено в жизненном цикле употребления водорода. Водород практически не встречается в природе в чистой форме и должен извлекаться из других соединений с помощью различных химических методов.
Методы производства водорода
Разнообразие способов получения водорода является одним из главных преимуществ водородной энергетики, так как повышает энергетическую безопасность и снижает зависимость от отдельных видов сырья.
К ним относятся:[источник не указан 1171 день]
В данный момент наиболее доступным и дешёвым процессом является паровая конверсия. Согласно прогнозам, она будет использоваться в начальной стадии перехода к водородной экономике для упрощения преодоления проблемы «курицы и яйца», когда из-за отсутствия инфраструктуры нет спроса на водородные автомобили, а из-за отсутствия водородных автомобилей не строится инфраструктура. В долгосрочной перспективе, однако, необходим переход на возобновляемые источники энергии, так как одной из главных целей внедрения водородной энергетики является снижения выброса парниковых газов. Такими источниками может быть энергия ветра или солнечная энергия, позволяющая проводить электролиз воды.
Производство водорода может быть сосредоточено на централизованных крупных предприятиях, что понижает себестоимость производства, но требует дополнительных расходов на доставку водорода к водородным автозаправочным станциям. Другим вариантом является маломасштабное производство непосредственно на специально оборудованных водородных автозаправочных станциях.
Производство водорода из различных источников сырья
Из углеводородов
Паровая конверсия природного газа / метана
Водород можно получать разной чистоты: 95-98% или особо чистый. В зависимости от дальнейшего использования водород получают под различным давлением: от 1,0 до 4,2 МПа. Сырье (природный газ или легкие нефтяные фракции) подогревается до 350-400° в конвективной печи или теплообменнике и поступает в аппарат десульфирования. Конвертированный газ из печи охлаждается в печи-утилизаторе, где вырабатывается пар требуемых параметров. После ступеней высокотемпературной и низкотемпературной конверсии СО газ поступает на адсорбцию СО2 и затем на метанирование остаточных оксидов. В результате получается водород 95-98,5% чистоты с содержанием в нем 1-5% метана и следов СО и СО2.
В том случае, если требуется получать особо чистый водород, установка дополняется секцией адсорбционного разделения конвертированного газа. В отличие от предыдущей схемы конверсия СО здесь одноступенчатая. Газовая смесь, содержащая H2, CO2, CH4, H2O и небольшое количество СО, охлаждается для удаления воды и направляется в адсорбционные аппараты, заполненные цеолитами. Все примеси адсорбируются в одну ступень при температуре окружающей среды. В результате получают водород со степенью чистоты 99,99%. Давление получаемого водорода составляет 1,5-2,0 МПа.
В настоящее время данным способом производится примерно половина всего водорода. Себестоимость процесса $2-5 за килограмм водорода. В будущем возможно снижение цены до $2-$2,50, включая доставку и хранение.
Газификация угля
Старейший способ получения водорода. Уголь нагревают при температуре 800°—1300° Цельсия без доступа воздуха. Первый газогенератор был построен в Великобритании в 40-х годах XIX века. США предполагают построить электростанцию по проекту FutureGen, которая будет работать на продуктах газификации угля. Электричество будут вырабатывать топливные элементы, используя в качестве горючего водород, получающийся в процессе газификации угля.
В декабре 2007 г. была определена площадка для строительства первой пилотной электростанции проекта FutureGen. В Иллинойсе будет построена электростанция мощностью 275 МВт. Общая стоимость проекта $1,2 млрд. На электростанции будет улавливаться и храниться до 90 % СО2.
Себестоимость процесса $2-$2,5 за килограмм водорода. В будущем возможно снижение цены до $1,50, включая доставку и хранение.
Из биомассы
Водород из биомассы получается термохимическим, или биохимическим способом. При термохимическом методе биомассу нагревают без доступа кислорода до температуры 500°-800° (для отходов древесины), что намного ниже температуры процесса газификации угля. В результате процесса выделяется H2, CO и CH4.
Себестоимость процесса $5-$7 за килограмм водорода. В будущем возможно снижение до $1,0-$3,0.
В биохимическом процессе водород вырабатывают различные бактерии, например, Rodobacter speriodes.
Возможно применение различных энзимов для ускорения производства водорода из полисахаридов (крахмал, целлюлоза), содержащихся в биомассе. Процесс проходит при температуре 30° Цельсия при нормальном давлении. Себестоимость водорода около $2 за кг.
Из цепочки сахар-водород-водородный топливный элемент можно получить[1] в три раза больше энергии, чем из цепочки сахар-этанол-двигатель внутреннего сгорания.
Из мусора
Разрабатываются различные новые технологии производства водорода. Например, в октябре 2006 года Лондонское Водородное Партнёрство опубликовало исследование (недоступная ссылка) о возможности производства водорода из муниципального и коммерческого мусора. Согласно исследованию, в Лондоне можно ежедневно производить 141 тонну водорода как пиролизом, так и анаэробным сбраживанием мусора. Из муниципального мусора можно производить 68 тонн водорода.
141 тонны водорода достаточно для работы 13750 автобусов с двигателями внутреннего сгорания, работающими на водороде. В Лондоне в настоящее время эксплуатируется более 8000 автобусов.
Химическая реакция воды с металлами
В 2007 году Университет Purdue (США) разработал метод производства водорода из воды при помощи алюминиевого сплава.
Сплав алюминия с галлием формируется в пеллеты. Пеллеты помещают в бак с водой. В результате химической реакции производится водород. Галлий создаёт вокруг алюминия плёнку, предотвращающую окисление алюминия. В результате реакции создаётся водород и оксид алюминия.
Из одного фунта (≈453 г) алюминия можно получать более 2 кВт·ч энергии от сжигания водорода и более 2 кВт·ч тепловой энергии во время реакции алюминия с водой. В будущем, при использовании электроэнергии атомных реакторов 4-го поколения, себестоимость водорода, получаемого в ходе реакции, станет эквивалента цене бензина $3 за галлон (≈3,8 л).
Автомобиль среднего размера с двигателем внутреннего сгорания с 350 фунтами (158 кг) алюминия на борту может проехать 350 миль (560 км). В будущем стоимость такой поездки составит $63 (0,11 $/км), включая стоимость восстановления оксида алюминия на атомной электростанции 4-го поколения.[2]
С использованием водорослей
Учёные калифорнийского университета в Беркли (UC Berkeley) 1999 году обнаружили[источник не указан 1052 дня], что если водорослям не хватает кислорода и серы, то процессы фотосинтеза у них резко ослабевают, и начинается бурная выработка водорода.
Водород может производить группа зелёных водорослей, например, Chlamydomonas reinhardtii. Водоросли могут производить водород из морской воды, или канализационных стоков.
Домашние системы производства водорода
Вместо строительства водородных заправочных станций водород можно производить в бытовых установках из природного газа, или электролизом воды. Honda испытывает свою бытовую установку под названием Домашняя энергетическая станция Honda. Установка в бытовых условиях производит водород из природного газа. Часть водорода используется в топливных элементах для производства тепловой и электрической энергии для дома. Оставшаяся часть водорода используется для заправки автомобиля.
Британская компания ITM Power Plc разработала и испытала в 2007 г. бытовой электролизёр для производства водорода. Водород производится ночью, что позволит сгладить пики потребления электроэнергии. Электролизер мощностью 10 кВт производит из воды водород, и хранит его под давлением 75 бар. Произведённого водорода достаточно для 40 км пробега битопливного (водород/бензин) Ford Focus. Компания планирует начать производство бытовых электролизеров в начале 2008 года. ITM Power уже достигла уровня себестоимости электролизеров $164 за 1кВт.
Крупнейшие производители водорода
См. также
Примечания
Ссылки
wiki.sc
Промышленное получение — водород — Большая Энциклопедия Нефти и Газа, статья, страница 1
Промышленное получение — водород
Cтраница 1
Промышленное получение водорода не может быть основано на реакции цинка с разбавленными кислотами, поскольку такой процесс неэкономичен. [1]
Промышленное получение водорода из метана и высших углеводородов может базироваться на коксовом и природном газе и на газах гидрогенизации топлива. [2]
Для промышленного получения водорода было предложено большое количество различных способов. Однако перечислять все способы и патенты по производству водорода нет нужды; это представляет главным образом исторический интерес, поскольку большинство из предложенных способов вообще не было осуществлено в промышленном масштабе, а в практических условиях оправдали себя лишь некоторые из них. [3]
Основным сырьем для промышленного получения водорода служат природные горючие газы, коксовый газ, газы нефтепереработки, продукты газификации угля и воды. [4]
Основными видами сырья для промышленного получения водорода служат природные газы — коксовый газ и продукты газификации различных видов топлива. [5]
Однако использование этого процесса для промышленного получения водорода и кислорода было предложено русским физиком Д. А. Лачиновым [7] намного позже ( в 1888 г.), после того как промышленности стали доступны механические генераторы постоянного тока. [6]
Конверсия водяного газа является основным методом промышленного получения водорода. [7]
Эта реакция имеет важное значение при промышленном получении водорода. [8]
Теперь укажем третий способ, который имеет большое значение для промышленного получения водорода. При пропускании пара над докрасна раскаленным коксом образуется смесь водорода и оксида углерода. Из-за своего происхождения эта газовая смесь называется водяной газ. [9]
Каталитическая конверсия метана водяным паром лежит в основе одного из методов промышленного получения водорода. [11]
В технологии неорганических веществ большое значение имеет конверсия метана, лежащая в основе процесса промышленного получения водорода. При температуре около 0 С и более низкой СН4 образует гидрат со льдом, являющийся клатратом. Возможность образования данного соединения следует учитывать при эксплуатации газопроводов — если газ содержит влагу, то при низкой температуре происходит закупорка газопровода гидратом. [12]
В настоящее время установлено, что равновесное превращение углеводородов достигается только на никелевом катализаторе, особенно с добавкой окиси алюминия. Поэтому для промышленного получения водорода каталитической конверсией жидких углеводородов используют преимущественно катализатор на основе никеля. Содержание никеля, составы носителя и промоторов, способы приготовления никелевых катализаторов весьма разнообразны. [13]
Богатые метаном природные газы являются очень хорошим топливом, 1 м3 которого дает при сгорании 33 ч — 37 МДж. Кроме того, они служат основным сырьем для промышленного получения водорода. Получаемый газ подвергается затем вторичной обработке водяным паром ( доп. [14]
Процесс паровой каталитической конверсии природного газа является наиболее распространенным способом промышленного получения водорода. Этот эндотермический процесс обычно осуществляют в трубчатых реакторах с внешним газовым обогревом, Наиболее перспективным и экономичным считается процесс паровой конверсии под давлением 20 — 30 атм. [15]
Страницы: 1 2
www.ngpedia.ru
Производство водорода — Википедия
Электролизёр — оборудование для производства водорода из водыПромышленное производство водорода — неотъемлемая часть водородной энергетики, первое звено в жизненном цикле употребления водорода. Водород практически не встречается в природе в чистой форме и должен извлекаться из других соединений с помощью различных химических методов.
Методы производства водорода
Разнообразие способов получения водорода является одним из главных преимуществ водородной энергетики, так как повышает энергетическую безопасность и снижает зависимость от отдельных видов сырья.
К ним относятся:[источник не указан 1171 день]
В данный момент наиболее доступным и дешёвым процессом является паровая конверсия. Согласно прогнозам, она будет использоваться в начальной стадии перехода к водородной экономике для упрощения преодоления проблемы «курицы и яйца», когда из-за отсутствия инфраструктуры нет спроса на водородные автомобили, а из-за отсутствия водородных автомобилей не строится инфраструктура. В долгосрочной перспективе, однако, необходим переход на возобновляемые источники энергии, так как одной из главных целей внедрения водородной энергетики является снижения выброса парниковых газов. Такими источниками может быть энергия ветра или солнечная энергия, позволяющая проводить электролиз воды.
Производство водорода может быть сосредоточено на централизованных крупных предприятиях, что понижает себестоимость производства, но требует дополнительных расходов на доставку водорода к водородным автозаправочным станциям. Другим вариантом является маломасштабное производство непосредственно на специально оборудованных водородных автозаправочных станциях.
Видео по теме
Производство водорода из различных источников сырья
Из углеводородов
Паровая конверсия природного газа / метана
Водород можно получать разной чистоты: 95-98% или особо чистый. В зависимости от дальнейшего использования водород получают под различным давлением: от 1,0 до 4,2 МПа. Сырье (природный газ или легкие нефтяные фракции) подогревается до 350-400° в конвективной печи или теплообменнике и поступает в аппарат десульфирования. Конвертированный газ из печи охлаждается в печи-утилизаторе, где вырабатывается пар требуемых параметров. После ступеней высокотемпературной и низкотемпературной конверсии СО газ поступает на адсорбцию СО2 и затем на метанирование остаточных оксидов. В результате получается водород 95-98,5% чистоты с содержанием в нем 1-5% метана и следов СО и СО2.
В том случае, если требуется получать особо чистый водород, установка дополняется секцией адсорбционного разделения конвертированного газа. В отличие от предыдущей схемы конверсия СО здесь одноступенчатая. Газовая смесь, содержащая H2, CO2, CH4, H2O и небольшое количество СО, охлаждается для удаления воды и направляется в адсорбционные аппараты, заполненные цеолитами. Все примеси адсорбируются в одну ступень при температуре окружающей среды. В результате получают водород со степенью чистоты 99,99%. Давление получаемого водорода составляет 1,5-2,0 МПа.
В настоящее время данным способом производится примерно половина всего водорода. Себестоимость процесса $2-5 за килограмм водорода. В будущем возможно снижение цены до $2-$2,50, включая доставку и хранение.
Газификация угля
Старейший способ получения водорода. Уголь нагревают при температуре 800°—1300° Цельсия без доступа воздуха. Первый газогенератор был построен в Великобритании в 40-х годах XIX века. США предполагают построить электростанцию по проекту FutureGen, которая будет работать на продуктах газификации угля. Электричество будут вырабатывать топливные элементы, используя в качестве горючего водород, получающийся в процессе газификации угля.
В декабре 2007 г. была определена площадка для строительства первой пилотной электростанции проекта FutureGen. В Иллинойсе будет построена электростанция мощностью 275 МВт. Общая стоимость проекта $1,2 млрд. На электростанции будет улавливаться и храниться до 90 % СО2.
Себестоимость процесса $2-$2,5 за килограмм водорода. В будущем возможно снижение цены до $1,50, включая доставку и хранение.
Из биомассы
Водород из биомассы получается термохимическим, или биохимическим способом. При термохимическом методе биомассу нагревают без доступа кислорода до температуры 500°-800° (для отходов древесины), что намного ниже температуры процесса газификации угля. В результате процесса выделяется H2, CO и CH4.
Себестоимость процесса $5-$7 за килограмм водорода. В будущем возможно снижение до $1,0-$3,0.
В биохимическом процессе водород вырабатывают различные бактерии, например, Rodobacter speriodes.
Возможно применение различных энзимов для ускорения производства водорода из полисахаридов (крахмал, целлюлоза), содержащихся в биомассе. Процесс проходит при температуре 30° Цельсия при нормальном давлении. Себестоимость водорода около $2 за кг.
Из цепочки сахар-водород-водородный топливный элемент можно получить[1] в три раза больше энергии, чем из цепочки сахар-этанол-двигатель внутреннего сгорания.
Из мусора
Разрабатываются различные новые технологии производства водорода. Например, в октябре 2006 года Лондонское Водородное Партнёрство опубликовало исследование (недоступная ссылка) о возможности производства водорода из муниципального и коммерческого мусора. Согласно исследованию, в Лондоне можно ежедневно производить 141 тонну водорода как пиролизом, так и анаэробным сбраживанием мусора. Из муниципального мусора можно производить 68 тонн водорода.
141 тонны водорода достаточно для работы 13750 автобусов с двигателями внутреннего сгорания, работающими на водороде. В Лондоне в настоящее время эксплуатируется более 8000 автобусов.
Химическая реакция воды с металлами
В 2007 году Университет Purdue (США) разработал метод производства водорода из воды при помощи алюминиевого сплава.
Сплав алюминия с галлием формируется в пеллеты. Пеллеты помещают в бак с водой. В результате химической реакции производится водород. Галлий создаёт вокруг алюминия плёнку, предотвращающую окисление алюминия. В результате реакции создаётся водород и оксид алюминия.
Из одного фунта (≈453 г) алюминия можно получать более 2 кВт·ч энергии от сжигания водорода и более 2 кВт·ч тепловой энергии во время реакции алюминия с водой. В будущем, при использовании электроэнергии атомных реакторов 4-го поколения, себестоимость водорода, получаемого в ходе реакции, станет эквивалента цене бензина $3 за галлон (≈3,8 л).
Автомобиль среднего размера с двигателем внутреннего сгорания с 350 фунтами (158 кг) алюминия на борту может проехать 350 миль (560 км). В будущем стоимость такой поездки составит $63 (0,11 $/км), включая стоимость восстановления оксида алюминия на атомной электростанции 4-го поколения.[2]
С использованием водорослей
Учёные калифорнийского университета в Беркли (UC Berkeley) 1999 году обнаружили[источник не указан 1052 дня], что если водорослям не хватает кислорода и серы, то процессы фотосинтеза у них резко ослабевают, и начинается бурная выработка водорода.
Водород может производить группа зелёных водорослей, например, Chlamydomonas reinhardtii. Водоросли могут производить водород из морской воды, или канализационных стоков.
Домашние системы производства водорода
Вместо строительства водородных заправочных станций водород можно производить в бытовых установках из природного газа, или электролизом воды. Honda испытывает свою бытовую установку под названием Домашняя энергетическая станция Honda. Установка в бытовых условиях производит водород из природного газа. Часть водорода используется в топливных элементах для производства тепловой и электрической энергии для дома. Оставшаяся часть водорода используется для заправки автомобиля.
Британская компания ITM Power Plc разработала и испытала в 2007 г. бытовой электролизёр для производства водорода. Водород производится ночью, что позволит сгладить пики потребления электроэнергии. Электролизер мощностью 10 кВт производит из воды водород, и хранит его под давлением 75 бар. Произведённого водорода достаточно для 40 км пробега битопливного (водород/бензин) Ford Focus. Компания планирует начать производство бытовых электролизеров в начале 2008 года. ITM Power уже достигла уровня себестоимости электролизеров $164 за 1кВт.
Крупнейшие производители водорода
См. также
Примечания
Ссылки
wiki2.red
